
在标准状况下,若VL甲烷中含有的氢原子个数为n,则阿伏加德罗常数可表示为()
A. 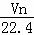 B.
B.  C.
C. 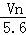 D.
D. 
 冲刺100分单元优化练考卷系列答案
冲刺100分单元优化练考卷系列答案科目:高中化学 来源: 题型:
重铬酸钠二水合物Na2Cr2O7·2H2O广泛用作氧化剂、金属表面精整、皮革制作等。以铬矿石(Cr2O3,含FeO、Al2O3、SiO2等杂质)为原料制取重铬酸钠的流程如下:
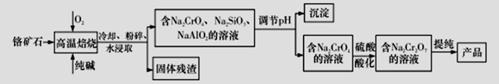
请回答下列问题:
(1)写出Cr2O3在高温焙烧生成Na2CrO4的化学方程式__________________________。
(2)调节pH后得到的沉淀主要是____________(填写化学式).
(3)写出用硫酸酸化使Na2CrO4转化为Na2Cr2O7的原理(写出离子方程式并加以文字说明):__________。
(4)氯化铬酸CrO2Cl2是红色液体,它可由Na2Cr2O7与NaCl的固体混合物和浓硫酸小心加热下制得,写出制备CrO2Cl2的化学反应方程式____________________________。
(5)某化工厂采用石墨作电极电解Na2CrO4溶液,实现Na2CrO4转化为Na2Cr2O7的生产,其原理如图所示。

①通电后阳极区溶液的颜色变化为__________________________________。
②写出电解Na2CrO4溶液制备Na2Cr2O7的化学反应方程式:_______________________________。
③在电流为I A.通电时间为t s后,两极共收集到3.36 L气体(标准状况下),则阿伏加德罗常数的表达式NA =_____mol-1(己知电子的电量为1.6* 10-19C)。
(6)Na2Cr2O7可用于测定废水的化学耗氧量(即COD,指每升水样中还原性物质被氧化所需要的O2的质量,单位:mg·L-1),现有某水样200.00 mL,酸化后加入c1 mol/L的Na2Cr2O7溶液V1 mL,使水中的还原性物质完全被氧化(还原产物为Cr3+ );再用c2 mol/L的FeSO4溶液滴定剩余的Cr2O72-,结果消耗FeSO4溶液V2 mL。则该水样的COD为_____________mg·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
氧化还原反应与四种基本类型反应的关系如下图所示,则下列化学反应属于区域3的是()
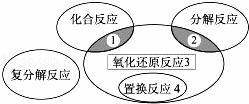
A. 2H2+O2 2H2O
2H2O
B. 2NaHCO3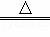 Na2CO3+H2O+CO2↑
Na2CO3+H2O+CO2↑
C. CuO+CO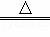 Cu+CO2
Cu+CO2
D. Zn+H2SO4=ZnSO4+H2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
根据下列反应的化学方程式:①Zn+CuSO4=ZnSO4+Cu、②Cu+2AgNO3=Cu(NO3)2+2Ag,判断三种金属的还原性强弱顺序是()
A. Zn>Cu>Ag B. Zn>Ag>Cu C. Cu>Ag>Zn D. Ag>Cu>Zn
查看答案和解析>>
科目:高中化学 来源: 题型:
鲜榨苹果汁是人们喜爱的饮料.由于此饮料中含有Fe2+,现榨的苹果汁在空气中会由淡绿色的Fe2+变为棕黄色Fe3+.这个变色的过程中的Fe2+被氧化 (填“氧化”或“还原”).若在榨汁的时候加入适量的维生素C,可有效防止这种现象的发生.这说明维生素C具有:B.
A、氧化性 B、还原性 C、酸性 D、碱性.
查看答案和解析>>
科目:高中化学 来源: 题型:
根据以下反应判断:Fe3+、Fe2+、Cu2+的氧化性强弱顺序是()
①Fe+CuCl2=Cu+FeCl2
②2FeCl3+Cu=CuCl2+2FeCl2.
A. Fe2+>Cu2+>Fe3+ B. Fe3+>Fe2+>Cu2+
C. Fe3+>Cu2+>Fe2+ D. Cu2+>Fe2+>Fe3+
查看答案和解析>>
科目:高中化学 来源: 题型:
在配制一定物质的量浓度的NaOH溶液时,下列哪个原因会造成所配溶液浓度偏高()
A. 所用NaOH已经潮解
B. 向容量瓶中加水未到刻度线
C. 有少量NaOH溶液残留在烧杯里
D. 定容时观察液面仰视
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com