
ЎҫМвДҝЎҝЈЁ12·ЦЈ©ПЦУРә¬NaClЎўNa2SO4әНNaNO3өД»мәПОпЈ¬СЎФсККөұөДКФјБҪ«ЖдЧӘ»ҜОӘПаУҰөДіБөн»т№ММеЈ¬ҙУ¶шКөПЦCl-ЎўSO42-ЎўәНNO3-өДПа»Ҙ·ЦАлЎЈПаУҰөДКөСй№эіМҝЙУГПВНјұнКҫЈә
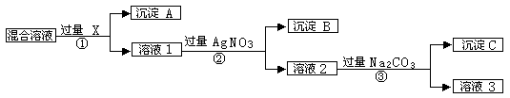
Зл»ШҙрПВБРОКМвЈә
ўЕРҙіцКөСйБчіМЦРПВБРОпЦКөД»ҜС§КҪЈә КФјБX Јә Ј¬іБөнAЈә
ўЖЙПКцКөСйБчіМЦРјУИл№эБҝөДNa2CO3өДДҝөДКЗ ЎЈ
ўЗ°ҙҙЛКөСй·Ҫ°ёөГөҪөДИЬТә3ЦРҝП¶Ёә¬УР ЈЁМо»ҜС§КҪЈ©ФУЦКЈ»ОӘБЛҪвҫцХвёцОКМвЈ¬ҝЙТФПтИЬТә3ЦРјУИлККБҝөД Ј¬Ц®әуИфТӘ»сөГ№ММеNaNO3РиҪшРРөДКөСйІЩЧчКЗ ЈЁМоІЩЧчГыіЖЈ©ЎЈ
Ўҫҙр°ёЎҝЈЁ1Ј©BaCl2[»тBaЈЁNO3Ј©2]Ј»ЈЁ2·ЦЈ© BaSO4Ј»ЈЁ2·ЦЈ©
ЈЁ2Ј©К№ИЬТәЦРөДAg+ЎўBa2+НкИ«іБөнЈЁ2·ЦЈ©
ЈЁ3Ј©Na2CO3ЈЁ2·ЦЈ©Ј»ПЎHNO3ЈЁ2·ЦЈ©Ј»Хф·ў(2·ЦЈ©
ЎҫҪвОцЎҝЈЁ1Ј©ёщҫЭ№эіМўЪҝЙЦӘЈ¬іБөнBКЗВИ»ҜТшЈ¬ЛщТФAКЗБтЛбСОЈ¬ТтҙЛXКЗВИ»Ҝұө»тПхЛбұөЈ¬ФтAКЗБтЛбұөіБөнЎЈ
ЈЁ2Ј©УЙУЪИЬТә2ЦРә¬УР№эБҝөДBa2Ј«әНAgЈ«Ј¬ЛщТФјУИл№эБҝөДNa2CO3өДДҝөДКЗК№ИЬТәЦРөДAg+ЎўBa2+НкИ«іБөнЎЈ
ЈЁ3Ј©УЙУЪМјЛбДЖКЗ№эБҝөДЈ¬ЛщТФИЬТә3ЦРТ»¶Ёә¬УРМјЛбДЖЈ¬ТӘіэИҘМјЛбДЖЈ¬ФтҝЙТФјУИлККБҝөДПхЛбЎЈТӘөГөҪПхЛбДЖ№ММеЈ¬НЁ№эХф·ўјҙҝЙЎЈ


 ҪрЕЖҪМёЁЕаУЕУЕСЎҫнЖЪД©іеҙМ100·ЦПөБРҙр°ё
ҪрЕЖҪМёЁЕаУЕУЕСЎҫнЖЪД©іеҙМ100·ЦПөБРҙр°ё
| Дкј¶ | ёЯЦРҝОіМ | Дкј¶ | іхЦРҝОіМ |
| ёЯТ» | ёЯТ»Гв·СҝОіМНЖјцЈЎ | іхТ» | іхТ»Гв·СҝОіМНЖјцЈЎ |
| ёЯ¶ю | ёЯ¶юГв·СҝОіМНЖјцЈЎ | іх¶ю | іх¶юГв·СҝОіМНЖјцЈЎ |
| ёЯИэ | ёЯИэГв·СҝОіМНЖјцЈЎ | іхИэ | іхИэГв·СҝОіМНЖјцЈЎ |
ҝЖДҝЈәёЯЦР»ҜС§ АҙФҙЈә МвРНЈә
ЎҫМвДҝЎҝПВБР№ШУЪСх»ҜјБУл»№ФӯјБөДЕР¶ПХэИ·өДКЗ(ЎЎЎЎ)
A. ·ҙУҰCH4Ј«2O2![]() CO2Ј«2H2OЦРЈ¬O2КЗСх»ҜјБЈ¬CH4КЗ»№ФӯјБ
CO2Ј«2H2OЦРЈ¬O2КЗСх»ҜјБЈ¬CH4КЗ»№ФӯјБ
B. ·ҙУҰCl2Ј«2NaOH===NaClOЈ«NaClЈ«H2OЦРЈ¬Cl2КЗСх»ҜјБЈ¬NaOHКЗ»№ФӯјБ
C. ·ҙУҰMnO2Ј«4HCl(ЕЁ)![]() MnCl2Ј«Cl2ЎьЈ«2H2OЦРЈ¬HClКЗСх»ҜјБЈ¬MnO2КЗ»№ФӯјБ
MnCl2Ј«Cl2ЎьЈ«2H2OЦРЈ¬HClКЗСх»ҜјБЈ¬MnO2КЗ»№ФӯјБ
D. ·ҙУҰ2NaЈ«2H2O===2NaOHЈ«H2ЎьЦРЈ¬H2OјИКЗСх»ҜјБУЦКЗ»№ФӯјБ
Ійҝҙҙр°ёәНҪвОц>>
ҝЖДҝЈәёЯЦР»ҜС§ АҙФҙЈә МвРНЈә
ЎҫМвДҝЎҝПВұнКЗФӘЛШЦЬЖЪұнЦР¶МЦЬЖЪөДТ»Іҝ·ЦЎЈТСЦӘAФӘЛШФӯЧУөДЧоНвІгөзЧУКэұИЖдөзЧУІгКэөД3ұ¶»№¶аЎЈПВБР№ШУЪұнЦРБщЦЦФӘЛШөДЛө·ЁХэИ·өДКЗ (ЎЎЎЎ)

A. XөДөҘЦКФЪҝХЖшЦРҝЙТФИјЙХ
B. XЎўYЎўZИэЦЦФӘЛШЦРYФӘЛШРОіЙөДөҘәЛТхАлЧУ°лҫ¶Чоҙу
C. ЧоёЯјЫСх»ҜОп¶ФУҰөДЛ®»ҜОпЛбРФЧоЗҝөДКЗAФӘЛШ
D. AөҘЦКНЁИлNaZИЬТәЦРЈ¬ёщҫЭ·ҙУҰПЦПуҝЙЦӨГчAЎўZ·ЗҪрКфРФөДПа¶ФЗҝИх
Ійҝҙҙр°ёәНҪвОц>>
ҝЖДҝЈәёЯЦР»ҜС§ АҙФҙЈә МвРНЈә
ЎҫМвДҝЎҝИзНјОӘКөСйКТЦРЕЁБтЛбКФјБЖҝұкЗ©ЙПөДІҝ·ЦДЪИЭЈ¬Зл»ШҙрОКМвЎЈ
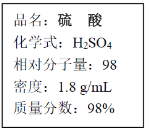
ЈЁ1Ј©ёГБтЛбөДОпЦКөДБҝЕЁ¶ИКЗ________mol/LЎЈ
ЈЁ2Ј©ДіКөСйРиТӘ90mL3.0mol/LПЎБтЛбЈ¬ЕдЦЖёГИЬТәЈ¬ҫӯјЖЛгЈ¬РиТӘУГБҝНІБҝИЎ___mLЕЁБтЛбЎЈ
ЈЁ3Ј©ФЪПВБРЕдЦЖ№эіМКҫТвНјЦРЈ¬УРҙнОуөДКЗЈЁМоРҙРтәЕЈ©________ЎЈ

ЈЁ4Ј©ПВБРЗйҝц»бТэЖрЛщЕдПЎБтЛбЕЁ¶ИЖ«ёЯөДКЗ________ЎЈ
A УГХфБуЛ®Ҫ«БҝНІЦРІРБфөДБтЛбПҙіцәПІў B ИЭБҝЖҝПҙөУәуЈ¬ОҙҫӯёЙФпҙҰАн
C ИЬТәОҙДЬАдИҙҫН¶ЁИЭ D ОҙПҙөУЙХұӯәНІЈБ§°ф
Ійҝҙҙр°ёәНҪвОц>>
ҝЖДҝЈәёЯЦР»ҜС§ АҙФҙЈә МвРНЈә
ЎҫМвДҝЎҝДіИЬТәЦРә¬УРҪПҙуБҝөДCl©ҒЎў![]() ЎўOH©ҒөИ3ЦЦТхАлЧУЈ¬Из№ыЦ»ИЎТ»ҙОёГИЬТәҫНДЬ№»·ЦұрҪ«3ЦЦТхАлЧУТАҙОјмСйіцАҙЈ¬ПВБРКөСйІЩЧчЛіРтХэИ·өДКЗЈЁЎЎЎЎЈ©
ЎўOH©ҒөИ3ЦЦТхАлЧУЈ¬Из№ыЦ»ИЎТ»ҙОёГИЬТәҫНДЬ№»·ЦұрҪ«3ЦЦТхАлЧУТАҙОјмСйіцАҙЈ¬ПВБРКөСйІЩЧчЛіРтХэИ·өДКЗЈЁЎЎЎЎЈ©
ўЩөОјУMgЈЁNO3Ј©2ИЬТәЈ»ўЪ№эВЛЈ»ўЫөОјУAgNO3ИЬТәЈ»ўЬөОјУBa(NO3)2ИЬТә
A.ўЩўЪўЬўЪўЫB.ўЬўЪўЩўЪўЫC.ўЩўЪўЫўЪўЬD.ўЬўЪўЫўЪўЩ
Ійҝҙҙр°ёәНҪвОц>>
ҝЖДҝЈәёЯЦР»ҜС§ АҙФҙЈә МвРНЈә
ЎҫМвДҝЎҝСх»Ҝұө№г·әУГУЪІЈБ§ЎўМХҙЙ№ӨТөЈ¬КЗЦЖИЎ№эСх»ҜұөәНұөСОөДФӯБПЎЈТ»ЦЦАыУГұөДа[ә¬BaCO3ЎўBaSO3ЎўBa(FeO2)2өИ]ЦЖИЎСх»ҜұөөДВМЙ«№ӨТХБчіМИзПВЈә

»ШҙрПВБРОКМвЈә
(1)ЛбИЬКұЈ¬Ba(FeO2)2УлПЎПхЛб·ҙУҰөД»ҜС§·ҪіМКҪОӘ_____________________ЎЈ
(2)ІъЙъВЛФь1өД·ҙУҰАлЧУ·ҪіМКҪКЗ____________________________________________ЎЈ
(3)ІЩЧчўсөчpH=4Ў«5өДДҝөДКЗ_________________________________________________ЎЈ
(4)№эВЛ3ЛщөГДёТәУҰ·ө»Ш______________№ӨРтСӯ»·К№УГЎЈ
(5)Ba(NO3)2ҝЙУГУЪЖыіөОІЖшЦР»№ФӯРФЖшМеөДҙЯ»ҜЧӘ»ҜЎЈҝЖјј№ӨЧчХЯУГH2ДЈДвОІЖшЦРөД»№ФӯРФЖшМеЈ¬СРҫҝBa(NO3)2өДҙЯ»Ҝ»№Фӯ№эіМЎЈёГ№эіМ·ЦБҪІҪҪшРРЈ¬ИзНјұнКҫёГ№эіМПа№ШОпЦКЕЁ¶ИЛжКұјдөДұд»Ҝ№ШПөЎЈөЪ¶юІҪ·ҙУҰПыәДөДNH3УлNO3ЈӯөДОпЦКөДБҝЦ®ұИКЗ_________ЎЈ

(6)Ў°ЖшМе2ЎұОӘ»мәПЖшМеЎЈұкЧјЧҙҝцПВa LЎ°ЖшМе2ЎұИЬУЪЛ®өГөҪbLИЬТәЈ¬ФтЛщөГИЬТәөДОпЦКөДБҝЕЁ¶ИОӘ_________________
Ійҝҙҙр°ёәНҪвОц>>
ҝЖДҝЈәёЯЦР»ҜС§ АҙФҙЈә МвРНЈә
ЎҫМвДҝЎҝПВБРНјКҫУл¶ФУҰөДРрКцПа·ыөДКЗ
A. ұнКҫФЪПаН¬өДГЬұХИЭЖчЦРЈ¬·ҙУҰA(g)+B(g)
ұнКҫФЪПаН¬өДГЬұХИЭЖчЦРЈ¬·ҙУҰA(g)+B(g) ![]() 2C(g)ФЪТ»¶ЁОВ¶ИПВCөДМе»э·ЦКэЛжКұјдөДұд»ҜЗйҝцЈ¬ФтёГ·ҙУҰөДҰӨH>0
2C(g)ФЪТ»¶ЁОВ¶ИПВCөДМе»э·ЦКэЛжКұјдөДұд»ҜЗйҝцЈ¬ФтёГ·ҙУҰөДҰӨH>0
B. ұнКҫ0.1000 molЎӨL-1NaOHИЬТәөО¶Ё20.00 mL 0.100 0 molЎӨL-1HXИЬТәөДөО¶ЁЗъПЯЈ¬ФтHXҝЙДЬОӘҙЧЛб
ұнКҫ0.1000 molЎӨL-1NaOHИЬТәөО¶Ё20.00 mL 0.100 0 molЎӨL-1HXИЬТәөДөО¶ЁЗъПЯЈ¬ФтHXҝЙДЬОӘҙЧЛб
C. ұнКҫAЎўBБҪОпЦКөДИЬҪв¶ИЛжОВ¶Иұд»ҜЗйҝцЈ¬Ҫ«T1 ЎжКұAЎўBөДұҘәНИЬТә·ЦұрЙэОВЦБT2 ЎжЈ¬ФтИЬЦКөДЦКБҝ·ЦКэЈәw(A)>w(B)
ұнКҫAЎўBБҪОпЦКөДИЬҪв¶ИЛжОВ¶Иұд»ҜЗйҝцЈ¬Ҫ«T1 ЎжКұAЎўBөДұҘәНИЬТә·ЦұрЙэОВЦБT2 ЎжЈ¬ФтИЬЦКөДЦКБҝ·ЦКэЈәw(A)>w(B)
D. ұнКҫ25 ЎжКұЈ¬·ЦұрјУЛ®ПЎКНМе»эҫщОӘ100 mL pH=2өДCH3COOHИЬТәәНHXИЬТәЈ¬Фт25 ЎжКұөзАлЖҪәвіЈКэЈәKa(HX)<Ka(CH3COOH)
ұнКҫ25 ЎжКұЈ¬·ЦұрјУЛ®ПЎКНМе»эҫщОӘ100 mL pH=2өДCH3COOHИЬТәәНHXИЬТәЈ¬Фт25 ЎжКұөзАлЖҪәвіЈКэЈәKa(HX)<Ka(CH3COOH)
Ійҝҙҙр°ёәНҪвОц>>
ҝЖДҝЈәёЯЦР»ҜС§ АҙФҙЈә МвРНЈә
ЎҫМвДҝЎҝёщҫЭТӘЗуМоҝХЈә
ЈЁ1Ј©РҙіцУР»ъОп![]() өДГыіЖ________ЎЈ
өДГыіЖ________ЎЈ
ЈЁ2Ј©өұТТЛб·ЦЧУЦРөДO¶јКЗ18OКұЈ¬ТТҙј·ЦЧУЦРөДO¶јКЗ16OКұЈ¬¶юХЯФЪТ»¶ЁМхјюПВ·ҙУҰЈ¬ЙъіЙОпЦРЛ®өДПа¶Ф·ЦЧУЦКБҝОӘ______ЎЈ
ЈЁ3Ј©»ҜС§УлЙъ»оПўПўПа№ШЎЈПВБРРрКцХэИ·өДКЗ___(МоЧЦДёҙъәЕ)ЎЈ
AЈ®ВшН·ФҪҪАФҪМр BЈ®ПКХҘіИЦӯУцөҪөвЛ®»бұдА¶
CЈ®УНЦ¬ҫӯЛ®ҪвҝЙұдіЙЖПМЗМЗ DЈ®НБ¶№ЦРөДөн·ЫҫӯЛ®ҪвҝЙұдіЙҫЖ
ЈЁ4Ј©Ді»ҜәПОпC3H6O2өДәЛҙЕ№ІХсЖЧ(NMR)ЦРУР3ёц·е,ЖдЗҝ¶ИұИОӘ3ЎГ2ЎГ1Ј¬ФтёГ»ҜәПОпөДҪб№№јтКҪҝЙДЬОӘ_______ЈЁРҙіцТ»ЦЦјҙҝЙЈ©ЎЈ
ЈЁ5Ј©ИрПгЛШКЗТ»ЦЦҫЯУРҝ№ҫъЎўҝ№СЧЎўҝ№ДэСӘөИЙъОп»оРФөДП㶹ЛШ»ҜәПОпЈ¬Жд·ЦЧУҪб№№ИзНјЛщКҫЎЈ»ШҙрПВБРОКМвЎЈ
![]()
ўЩИрПгЛШөД»ҜС§КҪОӘ____Ј¬ә¬Сх№ЩДЬНЕГыіЖ____Ј»
ўЪ1molҙЛ»ҜәПОпҝЙУл______molBr2·ҙУҰЈ¬Чо¶аҝЙТФУл____molNaOH·ҙУҰЎЈ
ЈЁ6Ј©јЧИ©әНРВЦЖЗвСх»ҜНӯөД·ҙУҰПФКҫБЛјЧИ©өД»№ФӯРФЈ¬·ўЙъ·ҙУҰөД»ҜС§·ҪіМКҪНЁіЈұнКҫОӘHCHO+2Cu(OH)2+NaOH![]() HCOONa+Cu2OЎэ+3H2OЎЈИфПтЧгБҝРВЦЖЗвСх»ҜНӯЦРјУИл4.00mLјЧИ©Л®ИЬТәЈ¬ід·Ц·ҙУҰЎЈЗлЙијЖТ»ёцјтөҘКөСйСйЦӨјЧИ©өДСх»ҜІъОпІ»КЗјЧЛбСОЎЈ____ЎЈЈЁҝЙ№©СЎУГөДКФјБЈәБтЛбНӯИЬТәЎўјЧИ©ЎўјЧЛбЎўЗвСх»ҜДЖИЬТәЎЈЈ©
HCOONa+Cu2OЎэ+3H2OЎЈИфПтЧгБҝРВЦЖЗвСх»ҜНӯЦРјУИл4.00mLјЧИ©Л®ИЬТәЈ¬ід·Ц·ҙУҰЎЈЗлЙијЖТ»ёцјтөҘКөСйСйЦӨјЧИ©өДСх»ҜІъОпІ»КЗјЧЛбСОЎЈ____ЎЈЈЁҝЙ№©СЎУГөДКФјБЈәБтЛбНӯИЬТәЎўјЧИ©ЎўјЧЛбЎўЗвСх»ҜДЖИЬТәЎЈЈ©
Ійҝҙҙр°ёәНҪвОц>>
ҝЖДҝЈәёЯЦР»ҜС§ АҙФҙЈә МвРНЈә
ЎҫМвДҝЎҝТСЦӘAЎўBЎўCҫщОӘә¬Мъ»ҜәПОпЈ¬ЗлёщҫЭТФПВЛДЦЦОпЦКөДЧӘ»Ҝ№эіМ»ШҙрПа№ШОКМвЈә
Fe![]() A
A![]() B
B![]() C
C
ЈЁ1Ј©·ҙУҰўЩЎўўЫЦРКфУЪСх»Ҝ»№Фӯ·ҙУҰөДКЗ________________ЈЁМоРтәЕЈ©ЎЈ
ЈЁ2Ј©ПтBөДИЬТәЦРөОИлјёөОKSCNИЬТәәуЈ¬ҝЙ№ЫІмөҪөДПЦПуКЗ__________ЎЈ
ЈЁ3Ј©·ҙУҰўЪөДАлЧУ·ҪіМКҪОӘ _____________ ЎЈ
Ійҝҙҙр°ёәНҪвОц>>
°Щ¶ИЦВРЕ - Б·П°ІбБРұн - КФМвБРұн
әюұұКЎ»ҘБӘНшОҘ·ЁәНІ»БјРЕПўҫЩұЁЖҪМЁ | НшЙПУРәҰРЕПўҫЩұЁЧЁЗш | өзРЕХ©ЖӯҫЩұЁЧЁЗш | ЙжАъК·РйОЮЦчТеУРәҰРЕПўҫЩұЁЧЁЗш | ЙжЖуЗЦИЁҫЩұЁЧЁЗш
ОҘ·ЁәНІ»БјРЕПўҫЩұЁөз»°Јә027-86699610 ҫЩұЁУКПдЈә58377363@163.com