
下列离子方程式书写正确的是
A.向NH4HCO3溶液中加过量Ca(OH)2溶液: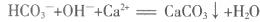
B.用惰性电极MgCl2电解水溶液: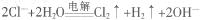
C.向偏铝酸钠溶液中加入少量硫酸氢钠溶液:
D.浓盐酸跟二氧化锰混合共热: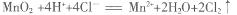
科目:高中化学 来源: 题型:
500 mL KNO3和Cu(N03)2的混合溶液中c(NO3-)=6.0 mol·L-1,用石墨作电极电解此溶液,当通电一段时间后,两极均收集到22.4 L气体(标准状况),假定电解后溶液体积仍为500 mL,下列说法正确的是( )
A.原混合溶液中c(K+)为1 mol·L-1
B.上述电解过程中共转移4 mol电子
C.电解得到的Cu的物质的量为0.5 mol
D.电解后溶液中c(H+)为2 mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
在恒温恒容容器中进行反应 ,若A的浓度由0.1 mol.L
,若A的浓度由0.1 mol.L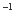 降到0.06 mol.L
降到0.06 mol.L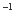 需20 s,那么由0.06 mol.L
需20 s,那么由0.06 mol.L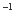 降到0.024 mol.L
降到0.024 mol.L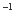 需要的时间
需要的时间
A.等于18s B,等于12s C,小于18s D.大于18s
查看答案和解析>>
科目:高中化学 来源: 题型:
一定温度下,在容积为VL的密闭容器中进行反应:
的物质的量随时间的变化曲线如图所示:(1)此反应的化学方程式中 =________。
=________。
(2)t1到t2时刻,以M的浓度变化表示的平均反应速率为_________。
 (3)下列叙述中能说明上述反应达到平衡状态的是________。
(3)下列叙述中能说明上述反应达到平衡状态的是________。
A.反应中M与N的物质的量之比为1:1
B.混合气体的总质量不随时间的变化而变化
C.混合气体的总物质的量不随时间的变化而变化
D.单位时间内每消耗a mol N,同时生成b mol M
E.混合气体的压强不随时间的变化而变化
F.N的质量分数在混合气体中保持不变
查看答案和解析>>
科目:高中化学 来源: 题型:
化学与生活密切相关,下列有关说法正确的是 ( )
A.维生素C具有还原性,在人体内起抗氧化作用
B.糖类、蛋白质、油脂属于天然高分子化合物
C.煤经气化和液化两个物理变化过程,可变为清洁能源
D.制作航天服的聚酯纤维和用于光缆通信的光导纤维都是新型无机非金属材料
查看答案和解析>>
科目:高中化学 来源: 题型:
实验室制取少量溴乙烷的装置如图所示。根据题意完成下列填空:

(1) 圆底烧瓶中加入的反应物是溴化钠、__________和1∶1的硫酸。配制体积比1∶1的硫酸所用的定量仪器为_________(选填编号)。
a.天平 b.量筒 c.容量瓶 d.滴定管
(2) 写出加热时烧瓶中发生的主要反应的化学方程式:
__________________________________________________________
___________________________________________________________
(3) 将生成物导入盛有冰水混合物的试管A中,冰水混合物的作用是_____________。
试管A中的物质分为三层(如图所示),产物在第____________________________层。
(4) 试管A中除了产物和水之外,还可能存在__________、___________(写出化学式)。
(5) 用浓的硫酸进行实验,若试管A中获得的有机物呈棕黄色,除去其中杂质的正确方法是___________(选填编号)。
a.蒸馏 b.用氢氧化钠溶液洗涤
c.用四氯化碳萃取 d.用亚硫酸钠溶液洗涤
若试管B中的酸性高锰酸钾溶液褪色,使之褪色的物质的名称是________。
(6)实验员老师建议把上述装置中的仪器连接部分都改成标准玻璃接口,其原因是__________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
以炼锌烟尘(主要成份为ZnO,含少量CuO和FeO)为原料,可以制取氯化锌和金属锌。
Ⅰ、制取氯化锌主要工艺如下:
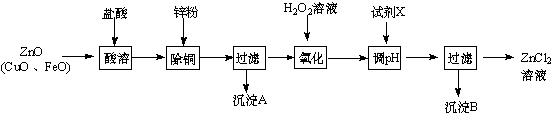
下表列出了相关金属离子生成氢氧化物沉淀的pH(开始沉淀的pH按金属离子浓度为
1.0 mol·L-1计算)。
金属离子 | 开始沉淀的pH | 沉淀完全的pH |
Fe3+ | 1. 1 | 3. 2 |
Zn2+ | 5. 2 | 6. 4 |
Fe2+ | 5. 8 | 8. 8 |
(1)加入H2O2溶液发生反应的离子方程式为 ▲ 。
(2)流程图中,为了降低溶液的酸度,试剂X可以是 ▲ (选填序号:a.ZnO;b.Zn(OH)2 ; c.Zn2(OH)2CO3 ;d.ZnSO4);pH应调整到 ▲ 。
(3)氯化锌能催化乳酸(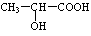 )生成丙交酯(C6H8O4)和聚乳酸,丙交酯的结构简式为 ▲ ,聚乳酸的结构简式为 ▲ 。
)生成丙交酯(C6H8O4)和聚乳酸,丙交酯的结构简式为 ▲ ,聚乳酸的结构简式为 ▲ 。
Ⅱ、制取金属锌采用碱溶解{ZnO(s)+2NaOH(aq)+H2O(l)=Na2[Zn(OH)4](aq)},然后电解浸取液。
(4)以石墨作电极电解时,阳极产生的气体为 ▲ ;阴极的电极反应为 ▲ 。
(5)炼锌烟尘采用碱溶,而不采用酸溶后电解,主要原因是 ▲ 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com