
����Ŀ���о����֣�һ�ڵ�����ڵ���ܹ�ʹһƽ��������ʧȥ���ü�ֵ���Ͼɵ�ص�Σ����Ҫ���������������������ؽ����ϡ����Ͼ�п�̵�ػ��մ��������ܼ������Ի�������Ⱦ������ʵ�ַϵ�ص���Դ�����á�
��1�����������еĶ������̺��Ȼ�李���֪���Ͼɸɵ�����ϵ���Ҫ�ɷ�Ϊ�������̡�̿�ۡ��Ȼ�狀��Ȼ�п�ȣ������Ȼ�李��Ȼ�п������ˮ���������ʵ�������ͼ��ʾ��
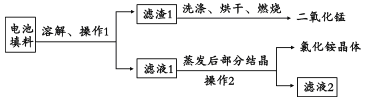
�� �������Ƚ�������������Ŀ���ǣ�________________��
�� ����l�Ͳ���2�����ƶ���___________���ò����в�������������___________��
�� ��������l��Ŀ����______________________��
��2�����ն��Ȼ��̣����Ͼ�п�̵�ش������õ����̻�����û�������Ũ���Ტ���ȡ�
��д��MnOOH��Ũ���ᷴӦ�Ļ�ѧ����ʽ��________________��
�� �̻����·�������Ͼ�п�̵���ڵĻ����[��Ҫ�ɷ�MnOOH��Zn(OH)2]�м���һ������ϡ�����ϡ���ᣨH2C2O4���������Ͻ�������CO2����Ϊֹ��д��MnOOH���뷴Ӧ�Ļ�ѧ����ʽ______________����ʹ��Ũ�����������ȣ��·������ŵ���___________����l�㼴�ɣ���
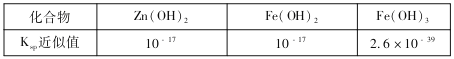
��3���÷ϵ�ص�пƤ�����ڻ�������ZnSO4��7H2O�������У����ȥпƤ�е��������������䷽���ǣ������£�����ϡH2SO4��H2O2�����ܽ��ΪFe3+���Ӽ����pHΪ4��ʹ��Һ�е�Fe3+ת��ΪFe(OH)3��������ʱ��Һ��c(Fe3+)=_________�������Ӽ����pHΪ____ʱ��п��ʼ�������ٶ�Zn2+Ũ��Ϊ0.1mol/L�����������ܵĵ�����ܶȻ�������Ksp�����±���
���𰸡� ����Ӵ�������ӿ췴Ӧ���� ���� ���� ��ȥ̿�� 2MnOOH+6HCl=2MnCl2+Cl2��+4H2O ��2MnOOH+H2C2O4+2H2SO4=2MnSO4+2CO2��+4H2O �����̼�����CO2��H2O��Ӱ��MnSO4���ȣ���Ӧ�������ж��к��������ɣ�����ɶ�����Ⱦ��������Դ���ȣ���1�㼴�ɣ� 2.6��10-9 6
����������������������ԷϾɵ�ص�������Ϊ���忼�黯ѧʵ�������������ѧ����ʽ����д�ͳ����ܽ�ƽ����ؼ��㡣��Ŀ�Ѷ��еȡ������Ҫע����ϵ��ѧʵ��������������ϼ���������ƽ�ͳ����ܽ�ƽ�����֪ʶ��������
�����1�����������еĶ������̺��Ȼ�李��Ͼɸɵ�����ϵ���Ҫ�ɷ�Ϊ�������̡�̿�ۡ��Ȼ�狀��Ȼ�п�ȣ������Ȼ�李��Ȼ�п������ˮ��̿�ۺͶ������̲�����ˮ������������ܽ⡢���ˣ�����1Ϊ̿�ۺͶ������̵Ļ�����ϴ�ӡ���ɡ�ȼ�գ�̿����������Ӧ���ɶ�����̼��ʣ��Ĺ���Ϊ�������̣���Һ1Ϊ�Ȼ�狀��Ȼ�п�Ļ��Һ�������ᾧ�����˵��Ȼ�茶��塣
�� �������Ƚ�������������Ŀ��������Ӵ�������ӿ췴Ӧ���ʡ�
�� ����l�Ͳ���2Ϊ��������Һ������IJ����������ǹ��ˣ���������������������
�� ��������l��Ŀ���dz�ȥ̿�ۡ�
��2����MnOOH��Ũ���ᷴӦ���ɶ��Ȼ��̡�������ˮ�����û��ϼ���������ƽ���÷�Ӧ����ѧ����ʽΪ2MnOOH+6HCl=2MnCl2+Cl2��+4H2O��
��MnOOH��ϡ�����ϡ���ᣨH2C2O4����Ӧ���������̡�������̼��ˮ�����û��ϼ���������ƽ���÷�Ӧ�Ļ�ѧ����ʽΪ2MnOOH+H2C2O4+2H2SO4=2MnSO4+2CO2��+4H2O ����ʹ��Ũ�����������ȣ��·������ŵ����������̼�����CO2��H2O��Ӱ��MnSO4���ȣ���Ӧ�������ж��к��������ɣ�����ɶ�����Ⱦ��������Դ���ȡ�
��3����Һ��pHΪ4��c(OH-)=1��10-10mol/L����Ksp[Fe(OH)3]=c(Fe3+)c3(OH-)=2.6��10-39����ʱ��Һ��c(Fe3+)= 2.6��10-9mol/L��Ksp[Zn(OH)2]=c(Zn2+)c2(OH-)=10-17����Zn2+Ũ��Ϊ0.1mol/L����c(OH-)=10-8mol/L��c(H+)=10-6mol/L��pH=6��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������£��ֱ�ȡ��������Ӧ�������������������������Һ���ã����˺��ʣ����Һ���������м���ָ�����ʣ���Ӧ�����Һ����Ҫ���ڵ�һ�����ӣ��л�����⣩��ȷ����
A. ͨ�������NH3(g)�� Ag+��NH4+��NO3-��OH-
B. ������� HNO3(aq)�� NH4+��Ag+��H+��NO3-��
C. ͨ����� HCl(g)�� [Ag(NH3)2]+��NH4+��H+��Cl-��NO3-��
D. �������NaOH(aq)�� [Ag(NH3)2]+��NH4+��Na+��NO3-��OH-
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������������Դ��Ҳ����Ҫ�Ļ���ԭ�ϣ����������������ⷽ��������������⣺

��1������һ��H2S�ȷֽⷨ����ӦʽΪ��H2S (g) ![]() H2 (g)+S(g) ��H���ں����ܱ������У��ⶨH2S�ֽ��ת����(H2S����ʼŨ�Ⱦ�Ϊc mol/L)���ⶨ�����ͼ1����������a��ʾH2S��ƽ��ת�������¶ȹ�ϵ������b��ʾ��ͬ�¶��·�Ӧ������ͬʱ��δ�ﵽ��ѧƽ��ʱH2S��ת���ʡ�
H2 (g)+S(g) ��H���ں����ܱ������У��ⶨH2S�ֽ��ת����(H2S����ʼŨ�Ⱦ�Ϊc mol/L)���ⶨ�����ͼ1����������a��ʾH2S��ƽ��ת�������¶ȹ�ϵ������b��ʾ��ͬ�¶��·�Ӧ������ͬʱ��δ�ﵽ��ѧƽ��ʱH2S��ת���ʡ�
�١�H___________0���>����<����=������
����985��ʱ����Ӧ��t min�ﵽƽ�⣬��ʱH2S��ת����Ϊ40%����tmin�ڷ�Ӧ����v(H2)=______���ú�c��t�Ĵ���ʽ��ʾ����
����˵�����¶ȵ����ߣ�����b������a�ӽ���ԭ��_________________��
��2������������CaOΪ�����壬��������ʣ���C�ƣ���ˮ������Ӧ��ȡH2�������Ҫ��Ӧ���£�
I��C(s) + H2O (g) = CO (g) + H2(g) ��H = + 131.6 kJ/mol
II��CO (g) + H2O (g) = CO2 (g) + H2 (g) ��H = -43 kJ/mol
III��CaO(s) + CO2(g) = CaCO3(s) ��H = -178.3 kJ/mol
�ټ��㷴ӦC (s) +2H2O(g) +CaO(s) ==CaCO3 (s)+2H2 (g)�ġ�H=_____��������С�������1λ������K1��K2��K3�ֱ�Ϊ��ӦI��II��III��ƽ�ⳣ�����÷�Ӧ��ƽ�ⳣ��k=______����K1��K2��K3��ʾ����
�ڶ��ڿ��淴ӦC (s) +2H2O(g) +CaO(s) ![]() CaCO3 (s)+2H2 (g)����ȡ���´�ʩ�������H2���ʵ���___�� ������ĸ��ţ�
CaCO3 (s)+2H2 (g)����ȡ���´�ʩ�������H2���ʵ���___�� ������ĸ��ţ�
A���ʵ��Ľ�����ϵ���¶� B��ʹ���������Ũ�Ⱦ��ӱ�
C������������������� D������CaO����
��ͼ2Ϊ��ӦI��һ���¶��£�ƽ��ʱ����������ٷֺ�����ѹǿ�仯�Ĺ�ϵͼ������Ӧ��ijһƽ��״̬ʱ�����c( H2O)=2c(H2)= 2c(CO)=2 mol��L���Ը���H2O������ٷֺ����仯���ߣ���������CO�ı仯����ʾ��ͼ��___________________
(3)��N2��H2Ϊ�缫��Ӧ���HCl-NH4C1Ϊ�������Һ��������ȼ�ϵ�أ��ŵ�����У���Һ��NH4+Ũ��������д���õ�ص�������Ӧʽ��___________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ij��ӦX+3Y=2E+2F�ڼס��ҡ����������ֲ�ͬ�����¡��ֱ��÷�Ӧ����Ϊ�ף�Vx=0.3mol��L-1��min-1���ң�VY=1.2mol��L-1��min-1������VE=0.8mol��L-1��min-1������VF=0.9mol��L-1��min-1����Ӧ������ ( )
A���� B���� C���� D����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��2016�������ҹ�����������������Ⱦ�������ء��п�Ժ���������������������Ŀ��Ա���ǿ�����̽��з�����ǿ��������,�����˴����ж��к��ĺ����л������ȼú�ͻ�����β���ǵ����������Ҫ��Դ�����ڶ����е�һЩ���������һ�����о���
��1����CH4����ԭ��������������������������Ⱦ��
��֪��
��CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g)��H=-574kJ��mol-1
��OCH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g)��H=-1160kJ��mol-1
��H2O(g)=H2O(1)��H=-44.0kJ��mol-1
д��CH4(g)��NO2(g)��Ӧ����N2(g)��CO2(g)��H2O(l)���Ȼ�ѧ����ʽ_________________________��
��2��Ϊ�˼��������Ⱦ���������������β�������ܿڲ��ô�����NO��COת��������Ⱦ����������ѭ����T��ʱ,�������ʵ�����NO��CO�����ݻ�Ϊ2L���ܱ�������,�����¶Ⱥ��������,��Ӧ������NO�����ʵ�����ʱ��仯����ͼ��ʾ��

��д���÷�Ӧ�Ļ�ѧ����ʽ��________________________________��
��10min�ڸ÷�Ӧ������v(N2)=___________;�÷�Ӧ��ƽ��ʱCO��ת����Ϊ___________;T��ʱ�û�ѧ��Ӧ��ƽ�ⳣ��K=___________��
�����÷�Ӧ��H<0,�ں��ݵ��ܱ�������,��Ӧ��ƽ��ı�ijһ����������ʾ��ͼ��ȷ����________��

��һ���¶���,�ں����ܱ������г���һ����NO��CO���и÷�Ӧ,���жϷ�Ӧ�Ѵﵽ��ѧƽ��״̬����____________��
a��������ѹǿ���ٱ仯 b��CO2��Ũ�Ȳ��ٸı�
c��2v��(NO)=v��(N2) d��������ܶȱ��ֲ���
��3����ȼ�ϵ��Ϊ����������Դ���ƹ���ʹ���ܴ����Ⱦ����ŷš���ͼ��һ�ּ���ȼ�ϵ�ؽṹ����д���õ�ظ����ĵ缫��Ӧʽ��________________________________________��

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������ӷ���ʽ��ȷ���ǣ� ��
A������������Һ�еμ�������ˮ��Ag++2NH3�T[Ag��NH3��2]+
B���Ჴ���ᣨ![]() ����̼��������Һ��Ӧ��
����̼��������Һ��Ӧ��
![]()
C����ȩ��������Ӧ��CH3CHO+2[Ag��NH3��2]++2OH��![]() CH3COO��+NH4++2Ag��+3NH3+H2O
CH3COO��+NH4++2Ag��+3NH3+H2O
D����������Һ��ͨ��CO2��2C6H5O��+CO2+H2O��2C6H5OH+CO32��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������ӷ���ʽ����д��ȷ����
A������ʯ��ˮ��ϡ���ᷴӦ: Ca(OH)2+2H+=Ca2++2H2O
B��ϡ�������ͭƬ�ϣ�Cu+2H+=Cu2++H2��
C����������Һ�м���ͭ����2Ag++Cu=Cu2++2Ag��
D��������������þ��Ӧ��H++OH-=H2O
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����2017���㽭ʡ���߲��������¸߿��о����˸����Ͽ��ԡ���֪��H2O![]() OH��+ H������25 ����100 ��ʱˮ��Kw�ֱ�Ϊ1.0��10-14��2.5��10-13������˵������ȷ����
OH��+ H������25 ����100 ��ʱˮ��Kw�ֱ�Ϊ1.0��10-14��2.5��10-13������˵������ȷ����
A��25 ��ʱ����ˮ��pH = 7������
B��100 ��ʱ����ˮ��pH �� 7������
C����ˮ��c(H��)100 ������25 ��
D��100 ���Ĵ�ˮ��c(H��)= c(OH��)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����1�������ӷ���ʽ���ͣ�ʢ������Һ���Լ�ƿ�в�������ʱ����˲��״�_____________��
��2��ijͬѧ���AlCl3(aq)��Na2S(aq)�����ȡA12S3,�����õ�һ�ְ�ɫ��״���������һ��Һ���г�������ζ������ų����Խ�����ɴ˽����ԭ��д����Ӧ�����ӷ���ʽ___________________��
��3��ͬ�¶��£�������ͬ NH4+Ũ�ȵ� NH3 ��H2O, NH4CI��CH3COONH4, NH4Fe(SO4)2 �У�����Ũ���ɴ�С��˳��Ϊ_____________��
��4�������£���A��B��C��D������ɫ��Һ�����Ƿֱ���CH3COONa��Һ��NH4C1��Һ�������NaNO3��Һ�е�һ�֡���֪A��B��ˮ��Һ��ˮ�ĵ���̶���ͬ��A��C��Һ��pH��ͬ����B�� ��Һ��C��_____________��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com