
【题目】某化学小组通过查阅资料,设计了如下图所示的方法以含镍废催化剂为原料来制备NiSO47H2O.已知某化工厂的含镍废催化剂主要含有Ni,还含有Al(31%)、Fe(1.3%)的单质及氧化物,其他不溶杂质(3.3%). 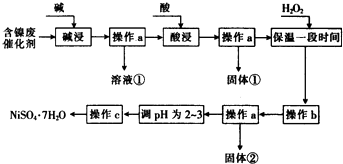
部分阳离子以氢氧化物形式沉淀时的pH如下:
沉淀物 | 开始沉淀时的pH | 完全沉淀时的pH |
Al(OH)3 | 3.8 | 5.2 |
Fe(OH)3 | 2.7 | 3.2 |
Fe(OH)2 | 7.6 | 9.7 |
Ni(OH)2 | 7.1 | 9.2 |
(1)“碱浸”过程中发生反应的离子方程式是
(2)“酸浸”时所加入的酸是(填化学式).
(3)加入H2O2时发生反应的离子方程式为
(4)操作b为调节溶液的pH,你认为pH的调控范围是
(5)产品晶体中有时会混有少量绿矾(FeSO47H2O),其原因可能是(写出一点即可).
(6)NiS047H2O可用于制备镍氢电池(NiMH),镍氢电池目前已经成为混合动力汽车的一种主要电池类型.NiMH中的M表示储氢金属或合金.该电池在充电过程中总反应的化学方程式是Ni(OH)2+M=NiOOH+MH,则NiMH电池放电过程中,正极的电极反应式为 .
【答案】
(1)2Al+2OH﹣+2H2O═2AlO ![]() +3H2↑、Al2O3+2OH﹣═2AlO
+3H2↑、Al2O3+2OH﹣═2AlO ![]() +H2O
+H2O
(2)H2SO4
(3)H2O2+2Fe2++2H+=2Fe3++2H2O
(4)3.2﹣7.1
(5)H2O2的用量不足(或H2O2失效)、保温时间不足导致Fe2+未被完全氧化造成的
(6)NiOOH+H2O+e﹣=Ni(OH)2+OH﹣
【解析】解:由流程可知,某化工厂的含镍催化剂主要含有Ni,还含有Al(31%)、Fe(1.3%)的单质及氧化物,其他不溶杂质(3.3%).碱浸过滤得到固体加入酸浸过滤加入过氧化氢氧化亚铁离子为铁离子,调节溶液PH使铁离子和铝离子全部沉淀,镍离子不沉淀,过滤后调节溶液PH2﹣3防止镍离子水解,通过蒸发浓缩,冷却结晶,过滤洗涤得到NiSO47H2O晶体;(1)“碱浸”过程中是为了除去铝及其氧化物,铝是两性元素和强碱反应,氧化铝是两性氧化物和强碱反应,镍单质和铁及其氧化物不和碱反应达到除去铝元素的目的;反应的两种方程式为:2Al+2OH﹣+2H2O═2AlO ![]() +3H2↑、Al2O3+2OH﹣═2AlO
+3H2↑、Al2O3+2OH﹣═2AlO ![]() +3H2O, 所以答案是:2Al+2OH﹣+2H2O═2AlO
+3H2O, 所以答案是:2Al+2OH﹣+2H2O═2AlO ![]() +3H2↑、Al2O3+2OH﹣═2AlO
+3H2↑、Al2O3+2OH﹣═2AlO ![]() +H2O;(2)“酸浸”时主要是溶解镍金属和铁单质及其氧化物,依据制备目的是得到NiSO47H2O,加入的酸不能引入新的杂质,所以需要加入硫酸进行酸浸;
+H2O;(2)“酸浸”时主要是溶解镍金属和铁单质及其氧化物,依据制备目的是得到NiSO47H2O,加入的酸不能引入新的杂质,所以需要加入硫酸进行酸浸;
所以答案是:H2SO4;(3)铁离子易转化为沉淀除去,加入过氧化氢氧化亚铁离子为铁离子,其反应的离子方程式为:H2O2+2Fe2++2H+=2Fe3++2H2O;所以答案是:H2O2+2Fe2++2H+=2Fe3++2H2O;(4)依据图表中沉淀需要的溶液pH,加入过氧化氢氧化亚铁离子为铁离子后,调节溶液pH使铁离子全部沉淀,镍离子不沉淀得到较纯净的硫酸镍溶液,pH应在3.2﹣7.1间,所以答案是:3.2﹣7.1;(5)产品晶体中有时会混有少量绿矾(FeSO47H2O),说明在加入过氧化氢氧化剂氧化亚铁离子时未把亚铁离子全部氧化,氢氧化亚铁沉淀的pH大于镍离子沉淀的pH,保温目的是把亚铁离子完全氧化,所以答案是:H2O2的用量不足(或H2O2失效)、保温时间不足导致Fe2+未被完全氧化造成的;(6)NiMH电池放电过程中,正极上NiOOH得电子生成Ni(OH)2 , 则正极的电极方程式为:NiOOH+H2O+e﹣=Ni(OH)2+OH﹣ , 所以答案是:NiOOH+H2O+e﹣=Ni(OH)2+OH﹣ .


科目:高中化学 来源: 题型:
【题目】丹参酮ⅡA是一种治疗心血管疾病的药物,其中的一种合成路线如下:
(1)丹参酮ⅡA中含氧官能团为和(写名称).
(2)试剂X的分子式为C5H11N,则X的结构简式为 .
(3)C→D的反应类型为 .
(4)写出同时满足下列条件的E的一种同分异构体的结构简式: .
(5)写出以CH3CH=CHCH3和CH2=CHCHO为原料制备 ![]() 的合成路线流程图(无机试剂可任选).合成路线流程图示例如下:CH3CHO
的合成路线流程图(无机试剂可任选).合成路线流程图示例如下:CH3CHO ![]() CH3COOH
CH3COOH ![]() CH3COOCH2CH3 .
CH3COOCH2CH3 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学是一门以实验为基础的科学,正确的实验操作是完成实验任务的保证。下列做法中,不合理的是( )
A. 在实验室里制取气体时,先检查装置的气密性
B. 做铁丝在氧气中燃烧实验时,预先在集气瓶中加少量水
C. 稀释浓硫酸时,将浓硫酸注入盛水的量筒中
D. 做氢气燃烧实验时,先检查氢气的纯度
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按要求填空
(1)化学反应可视为旧键断裂和新键形成的过程.化学键的键能是形成(或拆开)1mol化学键时释放(或吸收)的能量.已知:N≡N键的键能是948.9kJmol﹣1 , H﹣H键的键能是436.0kJmol﹣1;由N2和H2合成1mol NH3时可放出46.2kJ的热量.N﹣H键的键能是
(2)由氢气和氧气反应生成1mol水蒸气,放热241.8KJ.写出该反应的热化学方程式:① .
已知常温下NO与O2反应生成1molNO2的焓变为﹣57.07KJ,1molNO2与H2O反应生成HNO3溶液和NO的焓变为﹣46KJ,写出NO与O2及水生成HNO3溶液的热化学方程式② .
(3)某温度下纯水中的c(H+)=2×10﹣7mol/L,则此时c(OH﹣)=mol/L,该纯水的pH(填“>7”、“<7”、“=7”).若温度不变,滴入稀硫酸使c(H+)=5×10﹣6mol/L,则c(OH﹣)=mol/.
(4)纳米MgO可用于尿素与氯化镁合成.某小组研究该反应在温度为378~398K时的反应时间、反应物配比等因素对其产率的影响.请完成以下实验设计表:
编号 | 温度/K | 反应时间/h | 反应物物质的量配比 | 实验目的 |
① | 378 | 3 | 3:1 | 实验②和④探究 |
② | 378 | 4 | 4:1 | |
③ | 378 | 3 | ||
④ | 398 | 4 | 4:1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为除去括号内的少量杂质,所选用的试剂或方法不正确的是( )
A.Na2CO3溶液(NaHCO3),加入适量的NaOH溶液
B.NaHCO3溶液(Na2CO3),通入过量的CO2气体
C.Na2O2粉末(Na2O),将混合物在空气中加热
D.Na2CO3溶液(Na2SO4),加入适量的Ba(OH)2溶液,过滤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向某Na2CO3溶液中逐滴滴加1 mol·L-1的盐酸,测得溶液中Cl-、HCO的物质的量随加入盐酸体积的关系如图所示,其中n2:n1=3:2,则下列说法中正确的是( )

A.Oa段反应的离子方程式与ab段反应的离子方程式相同
B.该Na2CO3溶液中含有1 mol Na2CO3
C.b点的数值为0.6
D.b点时生成CO2的物质的量为0.3 mol
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com