
 氮及其化合物在工农业生产中具有重要作用.
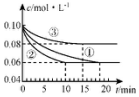
氮及其化合物在工农业生产中具有重要作用.分析 (1)根据v=$\frac{△c}{△t}$计算反应速率,根据图象可知②到达平衡的时间比①短,到达平衡时N2的浓度与①相同,化学平衡不移动,故②与①相比加了催化剂,①和③比较可知,③的速率比①小,平衡时氮气的浓度高,即平衡逆向移动,故③减小了压强;
(2)提高废气中氮氧化物的转化率,应改变条件使平衡向正反应移动,结合平衡移动原理分析.
解答 解:(1)根据像可知,②在10min时达到平衡,此时氮气的浓度变化为0.04mol/L,根据方程式或知,氨气的浓度变化了0.08mol/L,根据v=$\frac{△c}{△t}$可知v(NH3)=$\frac{0.08mol/L}{10min}$=0.008mol•L-1•min-1,则v(H2)=0.012mol•L-1•min-1,根据图象可知②到达平衡的时间比①短,到达平衡时N2的浓度与①相同,化学平衡不移动,故②与①相比加了催化剂,故选e,
故答案为:0.012mol•L-1•min-1;e;
(2)提高废气中氮氧化物的转化率,应改变条件使平衡向正反应移动,
a.该反应正反应是放热反应,升高温度,平衡向逆反应移动,氮氧化物的转化率降低,故a错误;
b.该反应正反应是体积增大的反应,增大压强,平衡向逆反应移动,氮氧化物的转化率降低,故b错误;
c.增大NH3的浓度,平衡向正反应移动,氮氧化物的转化率增大,故c正确;
故答案为:c.
点评 本题主要考查了物质的量或浓度随时间的变化曲线、化学平衡常数的含义、化学平衡的影响因素、化学反应速率的影响因素及有关平衡常数的判断,中等难度,侧重考查学生的综合能力.


 名校联盟冲刺卷系列答案
名校联盟冲刺卷系列答案 名校提分一卷通系列答案
名校提分一卷通系列答案 课程达标测试卷闯关100分系列答案
课程达标测试卷闯关100分系列答案 新卷王期末冲刺100分系列答案
新卷王期末冲刺100分系列答案科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 镁着火不能用CO2灭火 | |
| B. | 钠只有在加热条件下才能与氯气反应 | |
| C. | 浓硫酸有氧化性,稀硫酸没有氧化性 | |
| D. | SO2能使酸性高锰酸钾溶液褪色,说明SO2具有漂白性 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
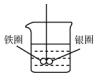 如图所示的装置,在盛有水的烧杯中,铁圈和银圈的连接处吊着一根绝缘的细丝,使之平痕.小心地从烧杯中央滴入CuSO4溶液.
如图所示的装置,在盛有水的烧杯中,铁圈和银圈的连接处吊着一根绝缘的细丝,使之平痕.小心地从烧杯中央滴入CuSO4溶液.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 溶液pH先变大后变小 | B. | 溶液导电能力逐渐增强 | ||
| C. | 氢硫酸完全反应生成1.6g硫 | D. | 这个反应可以证明还原性Cl->S2- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 实验事实 | 结论 | |
| A | 常温下白磷可自燃,而氮气要在放电条件下才与氧气反应 | 氮气的化学性质比磷稳定 |
| B | CO2的水溶液可导电 | CO2是电解质 |
| C | SO2通入到氯化钡溶液中出现白色沉淀 | 沉淀为亚硫酸钡 |
| D | 向某无色溶液中滴入少量NaOH溶液,用湿润的红色石蕊试纸放在试管口检验,试纸不变蓝色 | 无色溶液中不含NH4+ |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 2 mol•L-1NaCl溶液中含有Na+个数为2NA | |
| B. | 标准态况下,22.4 LH2O含有水分子数为NA | |
| C. | 71g氯气与足量铁粉充分反应,转移的电子数为3NA | |
| D. | 标准状况下,16gO2和O3的混合气体中原子的物质的量为1mol |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com