
| A. | 正向移动 | B. | 逆向移动 | ||
| C. | 不移动 | D. | 无法确定移动方向 |
分析 平衡时容器体积为1L,该温度下平衡常数K=$\frac{{c}^{2}(N{H}_{3})}{c({N}_{2})×{c}^{3}({H}_{2})}$=$\frac{{2}^{2}}{1×{3}^{3}}$=$\frac{4}{27}$,再向容器中再充入54mol N2,利用体积之比等于气体物质的量之比计算容器体积,再计算此时浓度商Qc,若Qc=K,处于平衡状态,若Qc<K,反应向正反应进行,若Qc>K,反应向逆反应进行.
解答 解:平衡时容器体积为1L,该温度下平衡常数K=$\frac{{c}^{2}(N{H}_{3})}{c({N}_{2})×{c}^{3}({H}_{2})}$=$\frac{{2}^{2}}{1×{3}^{3}}$=$\frac{4}{27}$=0.15,
再向容器中再充入54mol N2,恒温恒压下体积之比等于气体物质的量之比,则容器体积=1L×$\frac{60mol}{6mol}$=10L,
浓度商Qc=$\frac{(\frac{2}{10})^{2}}{\frac{55}{10}×(\frac{3}{10})^{3}}$=0.27>K=0.15,反应向逆反应进行,
故选:B.
点评 本题考查化学平衡计算与应用,关键是计算通入氮气后容器的体积,注意掌握化学平衡常数的用途:1、判断反应进行的程度,2、判断反应的热效应,3、判断反应进行的方向,4、计算转化率等.


 轻巧夺冠周测月考直通中考系列答案
轻巧夺冠周测月考直通中考系列答案科目:高中化学 来源: 题型:解答题
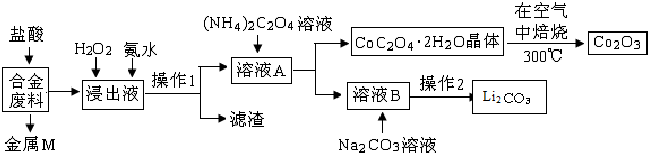
| 温度/℃ | 10 | 30 | 60 | 90 |
| 浓度/mol?L-1 | 0.21 | 0.17 | 0.14 | 0.10 |
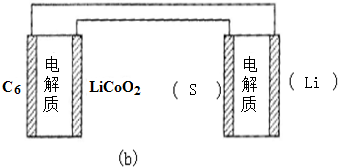 中填写“Li”或“S”,以达到给锂硫电池充电的目的.
中填写“Li”或“S”,以达到给锂硫电池充电的目的.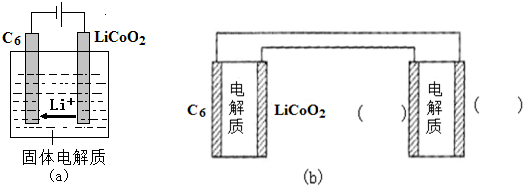
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用试管取出试剂瓶中的Na2CO3溶液,发现取量过多,为了不浪费,又把过量的试剂倒入试剂瓶中 | |
| B. | 开始蒸馏时,应该先通冷凝水,再加热;蒸馏完毕,应该先撤酒精灯再停通冷凝水 | |
| C. | 使用托盘天平称量物质时,先取小砝码,再依次取较大的砝码 | |
| D. | Ba(NO3)2溶于水,可将含有Ba(NO3)2的废液倒入水槽中,再用水冲入下水道 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 二氧化硫溶于水能导电,故二氧化硫属于电解质 | |
| B. | 硫酸钡难溶于水,故硫酸钡属于弱电解质 | |
| C. | 硫酸是强电解质,故纯硫酸能导电 | |
| D. | 氢氧根离子浓度相同的氢氧化钠溶液和氨水导电能力相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
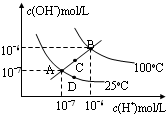
| A. | 图中四点Kw间的关系:A=D<C<B | |
| B. | 若从A点到D点,可采用:温度不变在水中加少量酸 | |
| C. | 若从A点到C点,可采用:温度不变在水中加少量NaAc固体 | |
| D. | 若从A点到D,可采用:温度不变在水中加少量NaAc固体 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 下列生活用品主要由有机合成材料制成:羊毛衫、腈纶运动衣、涤纶连衣裙、纯棉T恤 | |
| B. | 不锈钢制作就是在普通钢中添加铬、镍等元素改变了钢铁内部结构,所以不锈钢是化合物 | |
| C. | 黄河入海口沙洲的形成与用卤水点豆腐,都体现了胶体聚沉的性质 | |
| D. | 建筑业使用大量的沙,常使用内陆河的河沙及海洋的海沙 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常温常压下,22.4L氮气所含原子数目大于2NA | |
| B. | 1 mol Na2O2跟H2O反应转移的电子数目为2NA | |
| C. | 标准状态下,22.4L三氧化硫所含分子数目大于NA | |
| D. | 1 mol甲烷的质量与0.5 mol O2的质量不相等 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com