
| A. | 46 g 14CO2含氧原子数为2 NA | |
| B. | 1 mol Fe与足量的浓盐酸完全反应时转移电子数为3 NA | |
| C. | 标准状况下,22.4 L CCl4含有的分子数目为NA | |
| D. | 1 mol•L-1 CuCl2溶液中含Cl-数目为2 NA |
分析 A.物质的量n=$\frac{m}{M}$计算,1个14CO2分子中含氧原子2个;
B.1 mol Fe与足量的浓盐酸反应生成氯化亚铁和氢气;
C.标准状况下四氯化碳不是气体;
D.溶液体积不知不能计算微粒数.
解答 解:A.46 g 14CO2含物质的量n=$\frac{46g}{46g/mol}$=1mol,含氧原子数为2 NA,故A正确;
B.1 mol Fe与足量的浓盐酸完全反应时生成氯化亚铁,转移电子数为2NA,故B错误;
C.标准状况下四氯化碳不是气体,22.4 L CCl4含物质的量不是1mol,故C错误;
D.1 mol•L-1 CuCl2 溶液体积不知,不能计算微粒数,故D错误.
故选A.
点评 本题考查了阿伏伽德罗常数的有关计算,注意铁和盐酸反应生成氯化亚铁和氢气,熟练掌握公式的使用和物质的结构是解题关键,题目难度不大.


 小学同步三练核心密卷系列答案
小学同步三练核心密卷系列答案科目:高中化学 来源: 题型:选择题
| A. | 加强对煤、石油、天然气等综合利用的研究,提高燃料的利用率 | |
| B. | 大力研发新型有机溶剂替代水作为萃取剂 | |
| C. | 利用CO2合成聚碳酸酯类可降解塑料,实现“碳”的循环利用 | |
| D. | 使用甲醇、乙醇混合型汽油可以减少对大气的污染 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 标准状况下,5.6 LCCl4含有的分子数为0.25NA | |
| B. | 常温常压下,8g CH4含有的分子数为0.5NA | |
| C. | 7.8g Na2O2与足量水反应,转移电子数为0.2NA | |
| D. | 常温下,0.1mol Fe与酸完全反应时,失去的电子数一定为0.3NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 海带中的碘可以直接用四氯化碳萃取 | |
| B. | 在蒸发皿中灼烧海带使之变为海带灰 | |
| C. | 将海带灰溶于水中,滴加淀粉溶液,溶液变蓝 | |
| D. | 为了将I-氧化,加入的氧化剂最好选择H2O2溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
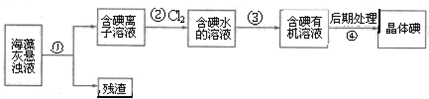
| A. | 步骤①、③的操作分别是过滤、萃取分液 | |
| B. | 可用淀粉溶液检验步骤②的反应是否进行完全 | |
| C. | 步骤③中加入的有机溶剂是乙醇 | |
| D. | 步骤④的操作是蒸馏 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.3 mol/L•min | B. | 0.6 mol/(L•min) | C. | 0.9 mol/(L•min) | D. | 1.2 mol/L•min |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 构成电池的两极必须是活泼性不同的金属 | |
| B. | 锌锰干电池工作时,锌作负极 | |
| C. | 在电池中,电子流出的一极是负极,发生还原反应 | |
| D. | 银锌纽扣电池工作时,电子由锌极流出经过溶液后流向银极 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com