
 )的一条路线如图:
)的一条路线如图: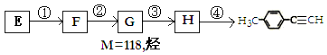
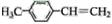 .
. 、
、 .
.分析 由E转化为对甲基苯乙炔(
 ,以此解答该题.
,以此解答该题.
解答 解:(1)①反应中所加试剂是:氢气和催化剂; ③的反应类型是:加成反应,
故答案为:氢气和催化剂;加成反应;
(2)由以上分析可知G的结构简式为: ,故答案为:
,故答案为: ;
;
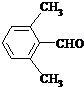
(3)E的同分异构体符合条件:①属于芳香醛;②苯环上有两种不同环境的氢原子,符合条件的同分异构体的结构简式为 ,
, ,
,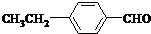 ,
,
故答案为: 、
、 、
、 (任意2种).
(任意2种).
点评 本题考查有机推断,为高考和高频考点,侧重考查学生的分析能力,需要学生熟练掌握官能团的性质与转化,难度中等.


 习题精选系列答案
习题精选系列答案科目:高中化学 来源: 题型:解答题
 在含有弱电解质的溶液中,往往有多个化学平衡共存.
在含有弱电解质的溶液中,往往有多个化学平衡共存.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
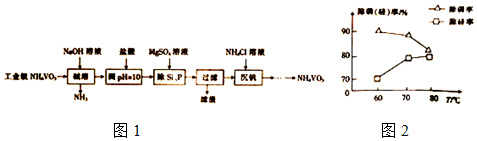
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 硫化钠溶液加入稀硝酸:S2-+2H+═H2 S↑ | |
| B. | 用惰性电极电解饱和硫酸铜溶液:2Cu2++2H2O$\frac{\underline{\;电解\;}}{\;}$2Cu+O2↑+4H+ | |
| C. | NaHSO4溶液与Ba(OH)2溶液混合:HSO4-+Ba2++OH-═BaSO4↓+H2O | |
| D. | 在强碱溶液中次氯酸钠与Fe(OH)3反应生成Na2FeO4的离子方程式:3ClO-+2Fe(OH)3═2FeO42-+3Cl-+H2O+4H+ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
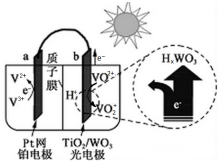
| A. | 光照时,太阳能主要转化为电能 | |
| B. | 光照时,b极的电极反应式为VO2+-e-+H2O═VO2++2H+ | |
| C. | 光照时,每转移5 mol电子,有5mol H+由b极区向a极区迁移 | |
| D. | 夜间,a极的电极反应式为V3++e-═V2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
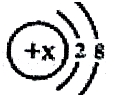 当x=8时,该粒子符号为O2-;当x=11时,该粒子符号为Na+;当x=13时,写出该粒子的硝酸盐的化学式为Al(NO3)3.
当x=8时,该粒子符号为O2-;当x=11时,该粒子符号为Na+;当x=13时,写出该粒子的硝酸盐的化学式为Al(NO3)3.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com