
 开心快乐假期作业暑假作业西安出版社系列答案
开心快乐假期作业暑假作业西安出版社系列答案 名题训练系列答案
名题训练系列答案科目:高中化学 来源: 题型:解答题
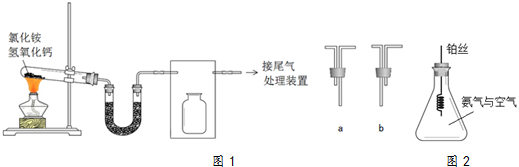
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 电解法精炼铜时,以粗铜作阴极,纯铜作阳极 | |
| B. | 铅蓄电池中Pb作负极,PbO2作正极 | |
| C. | 在物质的量浓度相等的NaCl和KBr的混合溶液中滴加AgNO3溶液,先产生淡黄色沉淀 | |
| D. | 常温下,pH=3的盐酸、醋酸分别用水稀释m倍、n倍后pH相同,则m<n |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
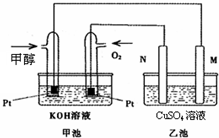 科学家利用太阳能分解水生成的氢气在催化剂作用下与二氧化碳反应生成甲醇和水,并开发出以甲醇为燃料的燃料电池.已知图甲池为甲醇燃
科学家利用太阳能分解水生成的氢气在催化剂作用下与二氧化碳反应生成甲醇和水,并开发出以甲醇为燃料的燃料电池.已知图甲池为甲醇燃查看答案和解析>>
科目:高中化学 来源: 题型:多选题
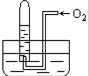 如图所示,试管中盛装的是红棕色气体(可能是混合物),当倒扣在盛有水的水槽中,与水充分作用后,试管内水面上升,但不能充满试管,当向试管内鼓如氧气后,可以观察到试管中水柱继续上升,经过多次重复后,试管内完全被水充满,原来试管中盛装的气体可能是( )
如图所示,试管中盛装的是红棕色气体(可能是混合物),当倒扣在盛有水的水槽中,与水充分作用后,试管内水面上升,但不能充满试管,当向试管内鼓如氧气后,可以观察到试管中水柱继续上升,经过多次重复后,试管内完全被水充满,原来试管中盛装的气体可能是( )| A. | N2与NO2的混和气体 | B. | NO2与O2按4:1体积比混合的气体 | ||
| C. | NO与NO2的混和气体 | D. | NO与O2按4:3体积比混合的气体 |
查看答案和解析>>
科目:高中化学 来源:2016-2017学年山东省高一上10月月考化学试卷(解析版) 题型:选择题
将质量分数为a%,物质的量浓度为c1mol/L的稀H2SO4蒸发掉一定量的水,使之质量分数为2a%,此时物质的量浓度为c2 mol/L,则c1和c2的数值关系是
A.c2 =c1 B.c2<2 c1 C.c2>2c1 D.c2=2c1
查看答案和解析>>
科目:高中化学 来源:2016-2017学年山东省高一上10月月考化学试卷(解析版) 题型:选择题
若NA表示阿伏伽德罗常数,下列说法正确的是
A.16g氧气和臭氧的混合物中含有的氧原子数为NA
B.标准状况下,22.4 L水中含有的原子数为NA
C.0.5mol/L的H2SO4溶液中含有硫酸分子数目为0.5NA
D.0.1mol氦气所含有的原子数为0.2NA
查看答案和解析>>
科目:高中化学 来源:2016-2017学年江西省高二上第一次月考化学卷(解析版) 题型:选择题
常温时,将CH3COOH溶液和NaOH溶液等体积混合后,溶液呈中性。则下列各项正确的是
A.混合前:pH(CH3COOH)+pH(NaOH)=14
B.混合后:c(Na+)=c(CH3COO-)+c(OH-)
C.混合前:c(CH3COOH)>c(NaOH)
D.混合后:c(Na+)>c(CH3COO-)>c(OH-)>c(H+)
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
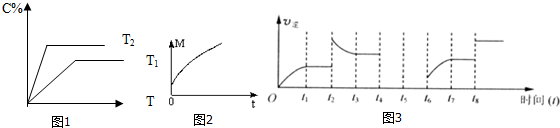
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com