
 ��̿��CO��H2������Ҫ����Դ��Ҳ����Ҫ�Ļ���ԭ�ϣ�
��̿��CO��H2������Ҫ����Դ��Ҳ����Ҫ�Ļ���ԭ�ϣ����� ��1������C��H2��CO��ȼ���ȣ���H���ֱ�Ϊ-393.5kJ•mol-1��-285.8kJ•mol-1��-283kJ•mol-1���Լ�ˮ��������Ϊ+44kJ/mol���ɵâ�C��s��+O2��g���TCO2��g������H=-393.5 kJ/mol����H2��g��+$\frac{1}{2}$O2��g���TH2O��l������H=-285.8kJ/mol����CO��g��+$\frac{1}{2}$O2��g��=CO2��g������H=-283.0kJ•mol-1����H2O��g��=H2O��l������H=-44kJ/mol�����ݸ�˹���ɣ�����+��-��-�ۿɵ�̼��ˮ������Ӧ���Ȼ�ѧ����ʽ��
�ڸ����Ȼ�ѧ����ʽ�Լ���Ӧ�зų�����������μӷ�Ӧ��ˮ�������ٸ���ת����=$\frac{��ת�������ʵ���}{��ʼ�����ʵ���}$��100%���㣻
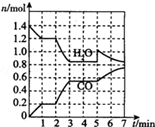
��2���ٸ���ͼ���֪���ڵ�һ��ƽ��ʱ�ε�CO�����ʵ���Ϊ0.2mol�����ʱ���ɵ�H2Ҳ��0.2mol����Ӧ��ϵ��ˮ�����ʵ���Ϊ1.2mol���ɵ�֪���ʵ�ƽ��Ũ�ȣ��ٸ���K=$\frac{c��CO��•c��{H}_{2}��}{c��{H}_{2}O��}$���㣬��Ӧ������2minʱ������ͼ��֪����ͬʱ���ڣ�ˮ��һ����̼�����ʵ����仯������0-1min�ڣ�˵����Ӧ�����������¶ȶԷ�Ӧ���ʡ���ѧƽ����ƶ���Ӱ�������
�ڷ�Ӧ����5minʱ��CO�����ʵ������䣬ˮ�����ʵ�������˵���ı������ˮ�����ʵ�����
��3���������ݻ�ѹ����1L��ѹǿ����Ӧ���ʱ����ƽ�������ƶ���H2O�����ʵ�����ԭ���Ļ����ϻ�����CO���ʵ�����ԭ���Ļ����ϻ��С��
��4����ȼ�ϵ���У�ͨ��CO�ĵ缫Ϊ������������COʧ���Ӻ�̼������ӷ�Ӧ���ɶ�����̼��ˮ��ͨ��O2�ĵ缫Ϊ�����������������õ��ӺͶ�����̼��Ӧ����̼������ӣ����ݵ��ӵ�ʧ�غ������ʳ��ˮ�в��������������ӵ����ʵ���������ȷ��pHֵ���ݴ˴��⣮
��� �⣺��1������C��H2��CO��ȼ���ȣ���H���ֱ�Ϊ-393.5kJ•mol-1��-285.8kJ•mol-1��-283kJ•mol-1���Լ�ˮ��������Ϊ+44kJ/mol���ɵâ�C��s��+O2��g���TCO2��g����H=-393.5 kJ/mol����H2��g��+$\frac{1}{2}$O2��g���TH2O��l����H=-285.8kJ/mol����CO��g��+$\frac{1}{2}$O2��g��=CO2��g����H=-283.0kJ•mol-1����H2O��g��=H2O��l����H=-44kJ/mol�����ݸ�˹���ɣ�����+��-��-�ۿɵ�C��s��+H2O��g��=CO��g��+H2��g����H=+131.3kJ/mol��
�ʴ�Ϊ��C��s��+H2O��g��=CO��g��+H2��g����H=+131.3kJ/mol��
�ڸ����Ȼ�ѧ����ʽC��s��+H2O��g��=CO��g��+H2��g������H=+131.3kJ/mol������������Ϊ191.7kJʱ���μӷ�Ӧ��ˮ���������ʵ���Ϊ$\frac{191.7kJ}{131.3kJ/mol}$=1.46mol������ˮ��ת����=$\frac{1.46}{2}$��100%=73%��
�ʴ�Ϊ��73%��
��2���ٸ���ͼ���֪���ڵ�һ��ƽ��ʱ�ε�CO�����ʵ���Ϊ0.2mol�����ʱ���ɵ�H2Ҳ��0.2mol����Ӧ��ϵ��ˮ�����ʵ���Ϊ1.2mol���ݻ�Ϊ2L�����Դ�ʱCO��ƽ��Ũ��Ϊ0.1mol/L��H2��ƽ��Ũ��Ϊ0.1mol/L��H2O��ƽ��Ũ��Ϊ0.6mol/L����K=$\frac{c��CO��•c��{H}_{2}��}{c��{H}_{2}O��}$=$\frac{0.1��0.1}{0.6}$=0.017��
Ӧ������2minʱ������ͼ��֪����ͬʱ���ڣ�ˮ��һ����̼�����ʵ����仯������0-1min�ڣ�˵����Ӧ��������ˮ���������ʵ������٣�һ����̼�����ʵ������ӣ�˵��ƽ��������Ӧ�����ƶ������÷�ӦΪ���ȷ�Ӧ����øı������ֻ���������¶ȣ�
�ʴ�Ϊ��0.017�����£�
�ڷ�Ӧ����5minʱ��CO�����ʵ������䣬ˮ�����ʵ�������˵���ı����������ˮ�����ʵ������淴Ӧ����ˮ������С��һ����̼����ƽ��������У�
a��������C�ǹ��壬��Ӱ�컯ѧƽ�⣬��a����
b��������ˮ������5minʱ��CO�����ʵ������䣬ˮ�����ʵ�������b��ȷ��
c����Ӧ�����ȷ�Ӧ���������¶�ƽ��������У�ͼ���ϣ���c����
d��������ѹǿ��ƽ��������У�������ͼ��仯����d����
�ʴ�Ϊ��b��
��3���������ݻ�ѹ����1L��ѹǿ����Ӧ���ʱ����ƽ�������ƶ���H2O�����ʵ�����ԭ���Ļ����ϻ�����CO���ʵ�����ԭ���Ļ����ϻ��С������H2O��CO���ʵ����仯���Ƶ�ͼ��Ϊ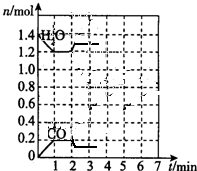 ���ʴ�Ϊ��
���ʴ�Ϊ�� ��
��
��4����ȼ�ϵ���У�ͨ��CO�ĵ缫Ϊ������������COʧ���Ӻ�̼������ӷ�Ӧ���ɶ�����̼��ˮ��������ӦʽΪCO+CO32--2e-=2CO2������5.6g����0.2mol��CO������ʱ����·�������ĵ��ӵ����ʵ���Ϊ0.4mol�����ݵ�ⷽ��ʽ2NaCl+2H2O$\frac{\underline{\;ͨ��\;}}{\;}$2NaOH+H2��+Cl2����2e-��֪�������в������������Ƶ����ʵ���Ϊ0.4mol�������������Ƶ�Ũ��Ϊ$\frac{0.4}{0.4}$mol/L=1mol/L��������Һ��pH=14��
�ʴ�Ϊ��CO+CO32--2e-=2CO2��14��
���� ���⿼�����Ȼ�ѧ����ʽ��Ӱ�컯ѧ��Ӧ���ʺͻ�ѧƽ���ƶ������ء��缫��Ӧʽ����д�����صļ����֪ʶ�㣬��ȷ��˹���ɺͻ�ѧƽ���ƶ�ԭ�������ӵ�ʧ�غ��ǽ���Ŀ�Ĺؼ�����Ŀ�Ѷ��еȣ�


 ��ʱѵ���������������ϵ�д�
��ʱѵ���������������ϵ�д� �ƸԾ���Ȥζ����ϵ�д�
�ƸԾ���Ȥζ����ϵ�д� ����С����ҵ��ϵ�д�
����С����ҵ��ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ������λ��Ԫȡ����ֻ��һ�� | B�� | ���ļ�λ��Ԫȡ����ֻ��һ�� | ||
| C�� | ���Ķ�λ��Ԫȡ����ֻ��һ�� | D�� | ������λ��Ԫȡ�����ж��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| ʱ��t��s�� | 0 | 1 | 2 | 3 | 4 | 5 |
| n��NO����mol�� | 0.020 | 0.010 | 0.008 | 0.007 | 0.007 | 0.007 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ��һ�������£���������������������·�Ӧ��2SO2��g��+O2��g��?2SO3��g������H��0��
��һ�������£���������������������·�Ӧ��2SO2��g��+O2��g��?2SO3��g������H��0���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
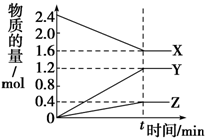 ��2L��������3�����ʽ��з�Ӧ��X��Y��Z�����ʵ�����ʱ��ı仯������ͼ��ʾ����Ӧ��tʱ�̴ﵽƽ�⣮
��2L��������3�����ʽ��з�Ӧ��X��Y��Z�����ʵ�����ʱ��ı仯������ͼ��ʾ����Ӧ��tʱ�̴ﵽƽ�⣮| A | B | C | |
| ��Ӧ��ʼʱŨ�ȣ�mol/L�� | 4.8 | 0 | |
| 2min���Ũ�ȣ�mol/L�� | 1.2 | 0.8 | |
| 2min�ڵ�Ũ�ȵı仯��mol/L�� | 0.4 | ||
| ��ѧѧ��Ӧ����[mol/��L•min��] | 0.5 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
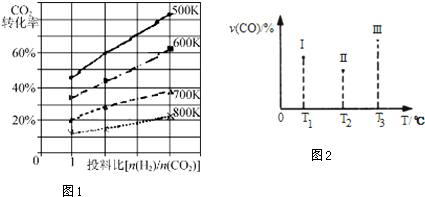
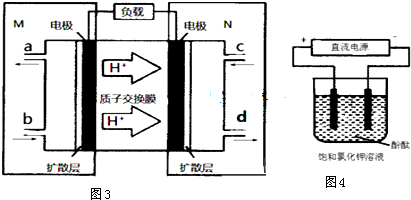
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
| ����̿/mol | NO/mol | A/mol | B/mol | ��/Mpa | |
| 200�� | 2.000 | 0.0400 | 0.0300 | 0.0300 | 3.93 |
| 335�� | 2.005 | 0.0500 | 0.0250 | 0.0250 | �� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
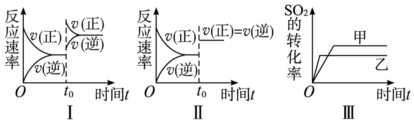
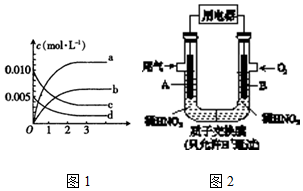
| A�� | ͼ���о�����t0ʱ������O2��Ũ�ȶԷ�Ӧ���ʵ�Ӱ�� | |
| B�� | ͼ���о������¶ȶԻ�ѧƽ���Ӱ�죬���ҵ��¶Ƚϵ� | |
| C�� | ͼ���о����Ǵ�����ƽ���Ӱ�죬�ҼĴ�Ч�ʱ��Ҹ� | |
| D�� | ͼ���о�����t0ʱ�̼��������Է�Ӧ���ʵ�Ӱ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | $\frac{1}{44}$ mol-1 | B�� | $\frac{x}{22}$ mol-1 | C�� | $\frac{3x}{44}$ mol-1 | D�� | $\frac{44x}{3}$ mol-1 |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com