
香料Ⅴ的制备方法如下:
(1)化合物I的分子式为 ,Ⅳ中含氧官能团的名称是 。
(2)化合物I可由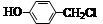 经两步反应制得,写出第一步反应的化学方程式 。
经两步反应制得,写出第一步反应的化学方程式 。
(3)1mol的化合物II和Ⅲ分别与H2反应,最多消耗H2的物质的量之比为 。
(4)该工艺中第①步的目的是 。为检验①中CH3I的碘原子,实验室的操作是:取少量CH3I于试管中,加入足量的NaOH水溶液,加热充分反应,冷却后加入 ,再加入少量硝酸银溶液。
(5)芳香化合物Ⅵ是Ⅲ的一种无甲基同分异构体,能发生水解反应和银镜反应,Ⅵ的结构简式为 。
(6)一定条件下,化合物Ⅳ与乙二醇发生类似反应④的反应,该有机产物的结构简式为 。
(1)C7H8O2(2分),羟基和醛基(2分)
(2)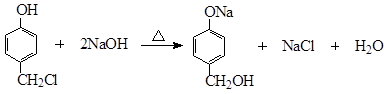 (2分)
(2分)
(3)3:4(2分)
(4)保护酚羟基,防止化合物Ⅰ氧化制醛时氧化酚羟基(2分)。加入稀硝酸(1分)至酸性(1分)。或加入足(过)量(1分)稀硝酸(1分)。
(5)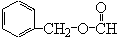 (2分)
(2分)
(6)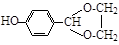 或者
或者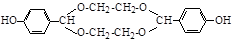 (2分)
(2分)
解析试题分析: (1)根据I的结构简式很容易得出其分子式为C7H8O2 ;IV中的含氧官能团是醛基和酚羟基。
(2)化合物I由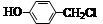 制备,主要是Cl原子在碱性水溶液中被OH取代,形成醇羟基,因为酚羟基有弱酸性,所以在碱性条件下要反应生成酚纳盐,所以要得到I,还需酸化。因此制备总共经过两步反应,那么第一步的反应的化学方程式就是:
制备,主要是Cl原子在碱性水溶液中被OH取代,形成醇羟基,因为酚羟基有弱酸性,所以在碱性条件下要反应生成酚纳盐,所以要得到I,还需酸化。因此制备总共经过两步反应,那么第一步的反应的化学方程式就是: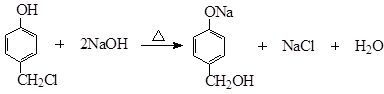
(3)化合物III比化合物II侧链多了一个-CHO,因此能多消耗H21mol,所以消耗H2的物质的量之比为3:4。
(4)工艺中反应②是氧化反应,因此第一步的目的是保护酚羟基,防止其被氧化;CH3I的I原子与C原子以共价键的形式连接,因此要检验I原子,要让CH3I在碱性条件下水解,再用硝酸酸化,后加硝酸银溶液,若出现黄色沉淀,证明含有I原子。
(5)III的同分异构体VI不含有-CH3,而能够发声水解,说明含有酯基,且能发生银镜反应,则构成的是甲酸某酯的结构(-O-CHO),因此满足条件的VI的结构简式为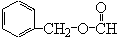 。
。
(6)从反应④的产物来看,化合物IV中的醛基和2分子的乙醇分子发生反应,形成两个C-O单键,因此若把2分子的乙醇换成乙二醇,则反应会按1:1或2:2进行,乙二醇中的2个羟基均反应,所以该有机物的结构简式为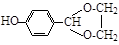 或
或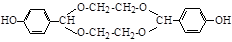 。
。
考点:本题考查的有机化合物的推断。


科目:高中化学 来源: 题型:单选题
下列有关物质的性质与应用不相对应的是
| A.CaH2能与水反应生成H2,可用作野外制氢气 |
| B.NH3具有还原性,可与灼热的CuO反应制备少量氮气 |
| C.SO2具有还原性,可使酸性高锰酸钾溶液褪色 |
| D.Si能导电,可用于制作光导纤维 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列有关物质的性质或用途的说法中正确的是
①Cl2具有漂白性,可以直接使有色布条褪色;②SO2具有较强的还原性,不能用浓硫酸干燥;③SiO2是酸性氧化物,能与氢氟酸反应;④Al(OH)3是两性氢氧化物,能溶于强酸或强碱。
| A.①②③ | B.②③④ | C.③④ | D.①②④ |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列反应,其产物的颜色按红色、红褐色、淡黄色、蓝色顺序排列的是( )
①金属钠在纯氧中燃烧 ②FeSO4溶液中滴入NaOH溶液,并在空气中放置一段时间 ③FeCl3溶液中滴入KSCN溶液 ④无水硫酸铜放入医用酒精中
| A.②③①④ | B.③②①④ |
| C.③①②④ | D.①②③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
(1)写出下列反应的化学方程式:
①铝热反应(铝粉与四氧化三铁): ;
②铜片与过量的浓硫酸共热: ;
(2)写出下列反应的离子方程式:
③铵盐溶液与烧碱溶液共热: ;
④铜片与浓硝酸反应: 。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
某化合物M(式量为80)俗称黑肥宝,它由原子序数不大于20的X、Y、Z三种元素组成,X、Y、Z的原子序数依次增大,其关系为Z=X+2Y。X、Y是同周期相邻的两种元素。M微溶于水,在常温下与水作用发生缓慢水解,最终产物为一种白色沉淀A与气体B,该气体能使湿润的红色石蕊试纸变蓝,A在高温条件下可分解产生一种有温室效应的气体。(注:以下回答若涉及到具体物质均用相应的化学式或元素符号表示)
(1)化合物M的化学式为 ;Z的原子结构示意图为 。
(2)写出下列反应的化学方程式。A在高温下分解: ; M与水反应生成A和B: 。
(3)Z的氢化物可作为一种储氢材料,写出其与水反应的化学方程式 。
(4)储氢材料的研究很广泛。下列物质中,可作为储氢材料的是 。(填编号)
| A.Ca(OH)2 | B.MgH2 | C.O2 | D.LaNi5 |
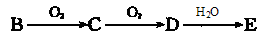 (强酸),将C和D的混气体通入NaOH溶液中恰好完全反应得到一种盐,请设计一个实验方案检验其中的阴离子 。
(强酸),将C和D的混气体通入NaOH溶液中恰好完全反应得到一种盐,请设计一个实验方案检验其中的阴离子 。查看答案和解析>>
科目:高中化学 来源: 题型:填空题
A、B、C、D均为中学化学中常见的单质或化合物,它们之间的关系如图所示(部分产物已略去)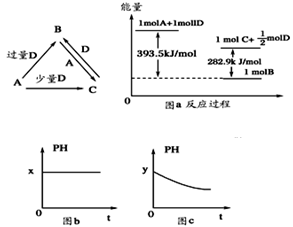
(1)若A为金属单质,D是某强酸的稀溶液,则反应C+D→B的离子方程式为_________
(2)若A、B为盐,D为强碱,A的水溶液显酸性,则 ①C的化学式为___________
②反应B+A→C的离子方程式为____________。
(3)若A为强碱,D为气态氧化物。常温时,将B的水溶液露置于空气中,其pH随时间t变化可能如上图的图b或图c所示(不考虑D的溶解和水的挥发)
①若图b符合事实,则D为________(填化学式),此时图b中x________7(填“﹥”“﹤”“=”)。②若图c符合事实,则其pH变化的原因是_______(用离子方程式表示)
(4)若A为非金属单质,D是空气的主要成分之一。它们之间转化时能量变化如上图a,请写出1molA和D反应生成C的反应热为ΔH=________________
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
已知A、B、C、D、E五种主族元素分属三个短周期,且原子序数依次增大。A、C同主族,可形成离子化合物CA;B、D同主族,可形成DB2、DB3两种分子。请回答下列问题:
(1)元素E在元素周期表中的位置是
(2)A、B两种元素能形成两种常温下呈液态的化合物M、N,具有强氧化性的化合物M的电子式可表示为 ;化合物N在同主族元素形成有具有相同结构的物质中,具有较高的沸点,其原因是 。
(3)A、B、C、D中的三种或四种元素能形成多种离子化合物,其水溶液呈碱性的有 (写出所有化合物,用化学式表示,下同),呈酸性的有 (写出所有化合物)。
(4)元素B、E的单质或两元素之间形成的化合物可作水消毒剂的有 (写出其中两种物质的化学式)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com