
【题目】“2015·8·12”天津港爆炸中有一定量的氰化物泄露。氰化物多数易溶于水,有剧毒,易造成水污染。已知部分弱酸的电离平衡常数如下表:
弱酸 | HCOOH | HCN | H2CO3 |
电离平衡常数(25℃) | Ki=1.77×10-4 | Ki=5.0×10-10 | Ki1=4.3×10-7 Ki2=5.6×10-11 |
(1)根据价键规则,写出H2CO3的结构式__________。
(2)下列能用于判断氮、碳两种元素非金属性强弱的是_________(填序号)
a. 气态氢化物的稳定性强弱 b. 最高价氧化物对应水化物酸性强弱
c. Al2O3+N2+3C=2AlN+3CO d. 比较在周期表中的位置
(3)0.01mol/L的NaCN溶液pH=9,用离子方程式表示呈碱性的原因_______。 请判断该溶液中:c(CN-)__c(OH-)(填“>”、“<”或“=”)
(4)含CN-的污水危害很大,处理该污水时,可在催化剂TiO2作用下用NaClO将CN-氧化成CNO-。CNO-在酸性条件下继续被NaClO氧化生成N2与CO2。某环保部门用下图装置进行实验,以证明该处理方法的有效性并测定CN-被处理的百分率。

将浓缩后含CN-的废水与过量NaClO溶液的混合液(其中CN-浓度为0.05mol/L)200mL倒入甲中,塞上橡皮塞,一段时间后,打开活塞,使溶液全部放入乙中,关闭活塞。
①甲中反应的离子方程式为___________,乙中反应的离子方程式为________。
②上述实验是通过测定CO2的量来确定CN-的处理效果。若丙中的试剂是饱和食盐水,且丙、丁都是除杂装置,则乙中产生的气体除CO2、N2外,还可能含有的杂质气体是__________,戊中盛有足量的石灰水,若实验后戊中生成0.9g沉淀,则CN-被处理的百分率为_________。
(5)装置中碱石灰的作用是__________。
【答案】 ![]() abcd CN-+H2O
abcd CN-+H2O![]() HCN+OH- > CN-+ClO-=CNO-+Cl- 2CNO-+3ClO-+2H+=N2↑+2CO2↑+H2O+3Cl- HCl、Cl2 90% 防止空气中的CO2进入戊,影响对产物的测定
HCN+OH- > CN-+ClO-=CNO-+Cl- 2CNO-+3ClO-+2H+=N2↑+2CO2↑+H2O+3Cl- HCl、Cl2 90% 防止空气中的CO2进入戊,影响对产物的测定
【解析】(1) H2CO3中C能形成四对共价键,O能形成两对共价键,H只能形成一对共价键,故结构式为:![]() ,故答案为:
,故答案为:![]() ;
;
(2)a.非金属性的强弱与气态氢化物稳定性相关,非金属性越强,气态氢化物越稳定,故a正确;b.最高价氧化物对应水化物酸性强弱,越强非金属性越强;故b正确;c.Al2O3+N2+3C═2AlN+3CO,反应中C为还原剂,N2为氧化剂,说明氮气氧化性大于碳单质,能说明非金属性强弱,故c正确;d.非金属性强弱与元素在周期表中的位置有关,同一周期从左到右非金属性逐渐增强,同一主族,从上到下非金属性逐渐减弱,故d正确;故选abcd;
(3)0.01mol/L的NaCN溶液pH=9,NaCN为强碱弱酸盐,水解呈碱性,CN-+H2O![]() HCN+OH-,pH=9,则c(OH-)=10-5mol/L,根据电荷守恒,c(CN-)+ c(OH-)= c(Na+)+ c(H+)=0.01+10-9,因此c(CN-)=0.01+10-9-10-5≈0.01 mol/L,因此c(CN-)>c(OH-),故答案为:CN-+H2O
HCN+OH-,pH=9,则c(OH-)=10-5mol/L,根据电荷守恒,c(CN-)+ c(OH-)= c(Na+)+ c(H+)=0.01+10-9,因此c(CN-)=0.01+10-9-10-5≈0.01 mol/L,因此c(CN-)>c(OH-),故答案为:CN-+H2O![]() HCN+OH-;>;
HCN+OH-;>;
(4)①CN-的废水在催化剂TiO2作用下用NaClO氧化,使CN-转化成CNO-,还生成氯离子,离子反应为CN-+ClO-═CNO-+Cl-,CNO-在酸性条件下继续被NaClO氧化成N2与CO2,还生成氯离子、水,离子反应为2CNO-+3ClO-+2H+═N2+2CO2+3Cl-+H2O,故答案为;CN-+ClO-=CNO-+Cl-,2CNO-+3ClO-+2H+═N2+2CO2+3Cl-+H2O;
②乙中生成的气体除N2和CO2外,还有HCl及副产物Cl2等;200mL(其中CN-的浓度0.05mol/L)混合液中含有的CN-的物质的量是:0.2L×0.05mol/L=0.01mol,根据碳原子守恒,增多生成0.01mol二氧化碳,所以石灰水过量,生成的碳酸钙的物质的量是: ![]() =0.009mol,反应的CN-的物质的量是0.009mol,CN-被处理的百分率是:
=0.009mol,反应的CN-的物质的量是0.009mol,CN-被处理的百分率是: ![]() ×100%=90%,故答案为:HCl、Cl2;90%;
×100%=90%,故答案为:HCl、Cl2;90%;
(5)装置中碱石灰可以防止空气中的CO2进入戊,影响对产物的测定,故答案为:防止空气中的CO2进入戊,影响对产物的测定。


科目:高中化学 来源: 题型:
【题目】工业以软锰矿(主要成分是MnO2,含有SiO2、Fe2O3等少量杂质)为主要原料制备高性能的磁性材料碳酸锰(MnCO3)。其工业流程如下:

(1)浸锰过程中Fe2O3与SO2反应的化学方程式为Fe2O3+ SO2+2H+=2Fe2++ SO42-+ H2O,该反应是经历以下两步反应实现的。写出ⅱ的离子方程式:_____________。
ⅰ:Fe2O3 + 6H+ = 2Fe3++3H2O
ⅱ:……
(2)过滤Ⅰ所得滤液中主要存在的两种金属阳离子为_____________(填离子符号)。
(3)写出氧化过程中MnO2与SO2反应的化学方程式:_________________。
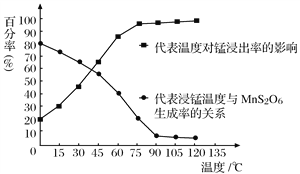
(4)“浸锰”反应中往往有副产物MnS2O6生成,温度对“浸锰”反应的影响如图所示,为减少MnS2O6的生成,“浸锰”的适宜温度是_________;向过滤Ⅱ所得的滤液中加入NH4HCO3溶液时温度不宜太高的原因是___________________。
(5)加入NH4HCO3溶液后,生成MnCO3沉淀,同时还有气体生成,写出反应的离子方程式:___________________。
(6)生成的MnCO3沉淀需经充分洗涤,检验洗涤是否完全的方法是____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关非金属及其化合物的说法正确的是( )
A.硅酸可使紫色石蕊试液变红色
B.二氧化硫通入紫色石蕊试液中.试液先变红后褪色
C.可用锌粒与稀硝酸反应制备氢气
D.液溴易挥发,所以存放液溴的试剂瓶中应加水封保存
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列解释事实的方程式不正确的是
A. 硫酸型酸雨的形成涉及反应:2H2SO3+O2![]() 2H2SO4
2H2SO4
B. SO2的水溶液显酸性:SO2+H2O ![]() H2SO3
H2SO3![]() 2H++ SO32-
2H++ SO32-
C. 常温下,0.1mol/L醋酸溶液pH≈3:CH3COOH![]() CH3COO-+ H+
CH3COO-+ H+
D. Mg(OH)2固体在溶液中存在平衡:Mg(OH)2(s)Mg2+(aq)+2OH-(aq),该固体可溶于NH4Cl溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在80℃时,将0.4mol的四氧化二氮气体充入2L已抽空的固定容积的密闭容器中,隔一段时间对该容器内的物质进行分析,得到如下数据:
时间(s) C(mol/L) | 0 | 20 | 40 | 60 | 80 | 100 |
C(N2O4) | 0. 20 | a | 0.10 | c | d | e |
C(NO2) | 0.00 | 0.12 | b | 0.22 | 0.22 | 0.22 |
反应进行至100s后将反应混合物的温度降低,发现气体的颜色变浅。
(1)该反应的化学方程式为__________________________,表中b_________c(填“<”、“=”、“>”)。
(2)20s时,N2O4的的浓度为__________________mol·L-1,0~20s内N2O4的平均反应速率为________________;
(3)该反应的平衡常数表达式K=___________________
在80℃时该反应的平衡常数K值为:______________(保留到小数点后2位)。
(4)在其他条件相同时,该反应的K值越大,表明建立平衡时____________。
A.N2O4的转化率越高 B.NO2的产量越大
C.N2O4与NO2的浓度之比越大 D.正反应进行的程度越大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】15 g A物质和10.5 g B物质完全反应,生成7.2 g C物质、1.8 g D物质和0.3 mol E物质,则E的摩尔质量为( )
A.16.5 g·mol-1 B.85 g·mol-1 C.55 D.55 g·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】过滤后的食盐水仍含有可溶性的CaCl2、MgCl2、Na2SO4 等杂质,通过如下几个实验步骤,可制得纯净的食盐水:① 加入稍过量的Na2CO3溶液;② 加入稍过量的NaOH溶液;③ 加入稍过量的BaCl2 溶液;④滴入稀盐酸至无气泡产生;⑤ 过滤。正确的操作顺序是 ( )
A.③②①⑤④ B.①②③⑤④ C.②③①④⑤ D.③⑤②①④
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com