
| A. | Na2CO3溶液 | B. | 水 | C. | CuSO4(aq) | D. | NaHSO4(s) |
分析 反应的实质为Zn+2H+═Zn2++H2↑,为了减缓反应速率,但又不影响生成氢气的总量,则减小氢离子的浓度但不能改变氢离子的物质的量即可,以此来解答.
解答 解:A.加入碳酸钠,与硫酸反应生成二氧化碳,减缓反应速率,硫酸不足,且影响生成氢气的总量,故A不选;
B.加水,氢离子的浓度减小,减缓反应速率,但又不影响生成氢气的总量,故B选;
C.加入硫酸铜,锌置换出铜,形成原电池反应,加快反应速率,故C不选;
D.加入硫酸氢钠,在溶液中电离出氢离子,氢离子浓度增大,则反应速率增大,生成氢气的总量增大,故D不选.
故选B.
点评 本题考查影响化学反应速率的因素,为高频考点,侧重于基本概念的综合理解和运用的考查,明确温度、浓度、接触面积对反应速率的影响即可解答,选项D为学生解答中的难点,题目难度不大.


科目:高中化学 来源: 题型:解答题
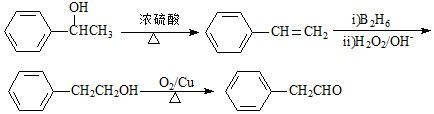
 . G的一种合成路线如下:
. G的一种合成路线如下:


 ;X生成Y的反应类型是消去反应.
;X生成Y的反应类型是消去反应.
 .
. .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 25℃时,向0.10mol•L-1 H2Y溶液中逐渐加入NaOH固体(忽略加入时引起的溶液体积变化),所得溶液中含Y元素的三种微粒的分布系数(浓度分数)δ随溶液pH变化的关系如图”所示,下列说法正确的是( )
25℃时,向0.10mol•L-1 H2Y溶液中逐渐加入NaOH固体(忽略加入时引起的溶液体积变化),所得溶液中含Y元素的三种微粒的分布系数(浓度分数)δ随溶液pH变化的关系如图”所示,下列说法正确的是( )| A. | 曲线上任意一点均存在:c(H+)+c(Na+)═c(OH-)+c(Y2-)+c(HY-) | |
| B. | c(Na+)=0.10 mol•L-1时,溶液中的c(H+)+c(H2Y)═c(OH-)+c(Y2-) | |
| C. | 由图可知,H2Y为二元弱酸,如果将物质的量浓度均为0.20mol•L-1的NaHY和Na2Y溶液等体积混合,所得溶液的pH=4.2 | |
| D. | 已知25℃时,HCOOH的Ka=1×10-4.若把少量H2Y加入到HCOONa溶液中,发生的离子反应可表示为:H2Y+2HCOO-═2HCOOH+Y2- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | H2SO4与Ba(OH)2溶液反应:Ba2++SO42-→BaSO4↓ | |
| B. | 碳酸钙溶于稀硝酸:CO32-+2H+→CO2↑+H2O | |
| C. | 氨水与稀硫酸反应:NH3•H2O+H+→NH4++H2O | |
| D. | CH3COOH溶液与NaOH溶液反应:H++OH-→H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 单质硅是良好的半导体材料 | B. | 光导纤维的主要成分是硅酸盐 | ||
| C. | 硅是构成矿物与岩石的主要元素 | D. | 玻璃、水泥、陶瓷都属于硅酸盐产品 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 最近世界各国都在研究“1C化学”、“2C化学”,它们是以1个或2个碳原子
最近世界各国都在研究“1C化学”、“2C化学”,它们是以1个或2个碳原子| 时间 (s) | 0 | 1 | 2 | 3 | 4 | 5 |
| c(NO)/10-3mol•L-1 | 10.0 | 4.50 | 2.50 | 1.50 | 1.00 | 1.00 |
| c(CO)/10-3mol•L-1 | 3.60 | 3.05 | 2.85 | 2.75 | 2.70 | 2.70 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com