
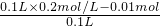 =0.1mol/L,故答案为:0.64;0.1.
=0.1mol/L,故答案为:0.64;0.1.

 中考解读考点精练系列答案
中考解读考点精练系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源:2011-2012学年福建省厦门市翔安一中高一上学期期中考试化学试卷 题型:填空题
某100mL的CuCl2溶液中,已知溶液中的Cl-的浓度为0.2 mol·L-1。现将一定量的铁粉投入到该溶液中,回答下列问题:
(1)原溶液中Cu2+的浓度为 ;
(2)反应后测得Cl-的浓度为 mol·L-1;
(3)若反应后测得Fe2+的溶液为0.05 mol·L-1,则反应生成铜单质的质量为 g;
(4)剩余的Cu2+的浓度为 。
查看答案和解析>>
科目:高中化学 来源:2012-2013学年福建省四地六校高一第三次月考化学试卷(带解析) 题型:填空题
(11分)
Ⅰ、质量相等的O3和O2中,分子个数之比为___________,原子个数之比为____________;
如果是在相同温度和相同压强条件下(O3为气体)O3与O2的体积比为___ ________。
Ⅱ、某100mL的CuCl2溶液中,已知溶液中的Cl-的浓度为0.2mol/L。现将一定量的铁粉投入到该溶液中(不考虑溶液的体积变化),回答下列问题:
(1)原溶液中Cu2+的物质的量浓度为 ;
(2)反应后测得Cl-的物质的量浓度为 ;
(3)若反应后测得Fe2+的溶液为0.05mol/L,则反应生成铜单质的质量为 ;
(4)剩余的Cu2+的物质的量浓度为 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com