
 ��������ЧӦ����Դ��ȱ�����⣬��ν��ʹ����е�CO2���������Կ������ã������˸������ձ����ӣ�Ŀǰ��ҵ����һ�ַ�������CO2����ȼ�ϼ״���һ�������·������·�Ӧ��CO2��g��+3H2��g��?CH3OH��g��+H2O��g��
��������ЧӦ����Դ��ȱ�����⣬��ν��ʹ����е�CO2���������Կ������ã������˸������ձ����ӣ�Ŀǰ��ҵ����һ�ַ�������CO2����ȼ�ϼ״���һ�������·������·�Ӧ��CO2��g��+3H2��g��?CH3OH��g��+H2O��g��| n(CH3OH) |
| n(CO2) |
| ��c |
| ��t |
| c(CH3OH)?c(H2O) |
| c(CO2)?c3(H2) |
| c(CH3OH)?c(H2O) |
| c(CO2)?c3(H2) |
| 2.25mol/L |
| 10min |



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A����ѧȼ�Ϻ�ֲ��ȼ��ȼ��ʱ�ų�����������Դ��̫���� |
| B���������������DZ�������CO2������ת��ɻ�ѧ�ܵĹ��� |
| C��һ����ѧ��Ӧ�У����������������С�ڷ�Ӧ���������ʱ����Ӧ���ȣ���HΪ��+�� |
| D��ͬ��ͬѹ�£�H2��g��+Cl2��g���T2HCl��g���ڹ��պ͵�ȼ�����µġ�H��ͬ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
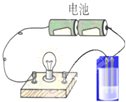 ����ͼ��ʾ��װ�÷ֱ��������ʵ�飬�����ӷ���ʽ��ȷ���������ʷ�Ӧ����Һ�ĵ����Աȷ�Ӧǰ������ǿ���ǣ�������
����ͼ��ʾ��װ�÷ֱ��������ʵ�飬�����ӷ���ʽ��ȷ���������ʷ�Ӧ����Һ�ĵ����Աȷ�Ӧǰ������ǿ���ǣ�������| A������������Һ��ͨ�������Ȼ��⣺Ag++Cl-�TAgCl�� |
| B������������Һ��ͨ��������H2SO3+Cl2+H2O�TSO42-+4H++2Cl- |
| C����FeI2��Һ��ͨ������������2Fe2++Cl2�T2Fe3++2Cl- |
| D����NaOH��Һ��ͨ������������2OH?+Cl2�TCl-+ClO-+H20 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��25�棬1mL H2O������OH-��Ϊ10-10NA |
| B����״���£�0.1mol Cl2����ˮ��ת�Ƶĵ�����ĿΪ0.1NA |
| C����״���£�11.2L CH3CH2OH�к��еķ�����ĿΪ0.5NA |
| D����״���£�33.6L�������к��з�ԭ�ӵ���ĿΪ1.5NA |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com