
 图是学校实验室从化学试剂商店买回的硫酸试剂标签上的部分内容,据此,回答问题:
图是学校实验室从化学试剂商店买回的硫酸试剂标签上的部分内容,据此,回答问题:分析 (1)纯净物只含一种物质,依据药品标签解答;
(2)依据C=$\frac{1000ρω}{M}$计算浓硫酸的物质的量浓度;
(3)依据溶液稀释过程中所含溶质的物质的量不变计算需要浓硫酸的体积;
(4)依据配制一定物质的量浓度溶液的一般步骤选择用到的仪器;
(5)分析操作对溶质的物质的量和溶液体积的影响,依据C=$\frac{n}{V}$进行误差分析.
解答 解:(1)通过标签可知该物质含有硫酸98%,水2%,属于混合物;
故答案为:混合物;
(2)浓硫酸的物质的量浓度C=$\frac{1000×1.84×98%}{98}$=18.4mol/L;
故答案为:18.4;
(3)配制500mL、0.2mol•L-1的稀H2SO4设需要浓硫酸体积为V,则依据溶液稀释过程中所含溶质的物质的量不变得V×18.4mol/L=0.2mol/L×500mL,解得V=5.4mL;
故答案为:5.4;
(4)配制一定物质的量浓度溶液的一般步骤:计算、量取、稀释、冷却、移液、洗涤、定容、摇匀、装瓶,依次用到的仪器:量筒、烧杯、玻璃棒、容量瓶、胶头滴管;
故选:D;
(5)①洗涤量取浓H2SO4后的量筒,并将洗涤液转移到容量瓶中,导致量取的浓硫酸体积偏大,溶质的物质的量偏大,溶液浓度偏高,故选;
②转移前,容量瓶中含有少量蒸馏水,对溶质的物质的量和溶液体积都不会产生影响,溶液浓度不变,故不选;
③定容时,加蒸馏水超过标线,又用胶头滴管吸出,导致部分溶质损失,溶质的物质的量偏小,溶液浓度偏低,故不选;
④定容时,俯视标线,导致溶液体积偏小,溶液浓度偏高,故选;
⑤定容摇匀后,发现液面低于标线,又用胶头滴管加蒸馏水至标线,导致溶液体积偏大,溶液浓度偏低,故不选;
故选:①④.
点评 本题考查了一定物质的量浓度溶液的配制及误差分析,明确配制原理及操作步骤是解题关键,注意依据C=$\frac{n}{V}$进行误差分析的方法.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
| 温度/℃ | 25 | t1 | t2 |
| 水的离子积 | 1×10-14 | a | 1×10-12 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
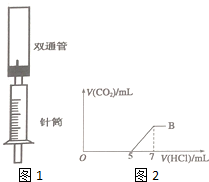 为探究Na2CO3与盐酸的反应原理,设计了如图1实验装置.
为探究Na2CO3与盐酸的反应原理,设计了如图1实验装置.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
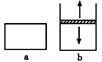
| A. | x的值为2 | |
| B. | B物质可为固体或液体 | |
| C. | 平衡时,a容器的体积小于V L | |
| D. | a、b容器中从起始到平衡所需时间相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

 .C-D的反应类型为还原反应.
.C-D的反应类型为还原反应.
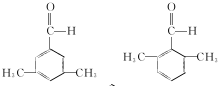 (写结构简式).
(写结构简式). 参照上述合成路线,设计一条由苯和乙酸为起始原料制备
参照上述合成路线,设计一条由苯和乙酸为起始原料制备 的合成路线:
的合成路线: .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①② | B. | ②③ | C. | ①③ | D. | ①②③ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com