
分析 根据蒸发前后溶质的质量不变,计算出原溶液的质量,根据m(溶质)=m(溶液)•ω计算溶质质量,根据n=$\frac{m}{M}$计算溶质KOH的物质的量,进而根据c=$\frac{n}{V}$计算溶液的物质的量浓度.
解答 解:蒸发掉63g水后质量分数恰好增大一倍,蒸发水后溶质质量分数为28%,
设14%氢氧化钾溶液的质量为m,蒸发前后溶质的质量不变,则:m×14%=(m-63g)×28%,解得:m=126g,
则28%的氢氧化钾溶液中含有氢氧化钾的物质的量为:$\frac{(126-63)g×28%}{56g/mol}$=0.315mol,
所得溶液的物质的量浓度为:c(KOH)=$\frac{0.315mol}{0.5L}$=0.63mol/L,
故答案为:0.63mol/L.
点评 本题考查了物质的量浓度的计算,题目难度不大,明确溶质质量分数的概念及表达式为解答关键,注意掌握物质的量浓度的计算方法,试题培养了学生的化学计算能力.


科目:高中化学 来源: 题型:选择题
| A. | Fe2+ | B. | Fe3+ | C. | Al3+ | D. | NH4+ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
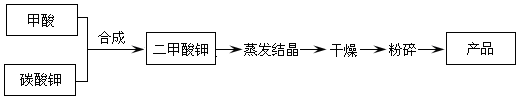
| 反应温度(℃) | 20 | 30 | 40 | 50 | 60 | 70 | 80 |
| 产品回收率(%) | 75.6 | 78.4 | 80.6 | 82.6 | 83.1 | 82.1 | 73.7 |
| 反应物料比 | 2:1 | 3:1 | 4:1 | 5:1 | 6:1 | 7:1 |
| 产品回收率(%) | 0 | 38.4 | 82. 6 | 83.6 | 84.5 | 84.8 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
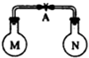 室温时,两个容积相同的烧瓶中分别盛有M和N 两种气体(同温同压),取下弹簧夹A,使两烧瓶内的气体充分混合后,容器内的压强由大到小的顺序是( )
室温时,两个容积相同的烧瓶中分别盛有M和N 两种气体(同温同压),取下弹簧夹A,使两烧瓶内的气体充分混合后,容器内的压强由大到小的顺序是( )| 编号 | ① | ② | ③ | ④ |
| 气体M | H2S | H2 | NH3 | NO |
| 气体N | SO2 | Cl2 | HCl | O2 |
| A. | ②④①③ | B. | ①②③④ | C. | ④①②③ | D. | ①④③② |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 少量SO2气体通入NaClO溶液中:SO2+H2O+2ClO-=2HClO+SO32- | |
| B. | 碳酸钙中滴入醋酸溶液:CaCO3+2CH3COOH=Ca2++2CH3COO-+H2O+CO2↑ | |
| C. | 碳酸氢镁溶液中加入过量的澄清石灰水:Mg2++2HCO3-+Ca2++2OH-=CaCO3↓+MgCO3↓+2H2O | |
| D. | 硫酸亚铁溶液中加过氧化氢溶液:2Fe2++2H++H2O2=2Fe3++2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
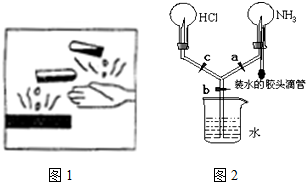
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
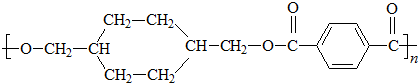
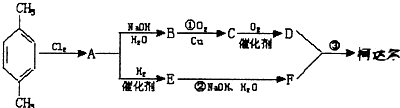
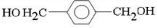 、D
、D 、E
、E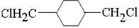 ;
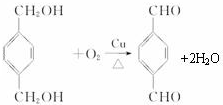
;
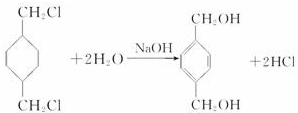 ;
; +
+ $\stackrel{一定条件}{→}$
$\stackrel{一定条件}{→}$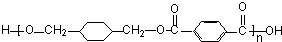 +(2n-1)H2O.
+(2n-1)H2O.查看答案和解析>>
科目:高中化学 来源: 题型:实验题
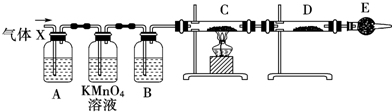
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 明矾净水与液氯净水的原理相同 | |
| B. | 将草木灰和硫铵混合施用,肥效更高 | |
| C. | 冬季形成的大雾属于气溶胶 | |
| D. | 电解精炼铜时,同一时间内阴极溶解铜的质量比阳极析出铜的质量小 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com