
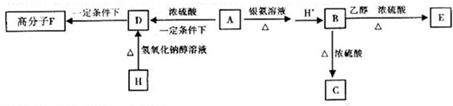
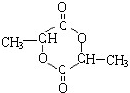
 ,A在浓硫酸作用下发生消去反应生成D为CH2=CHCHO,E发生加聚反应生成F为
,A在浓硫酸作用下发生消去反应生成D为CH2=CHCHO,E发生加聚反应生成F为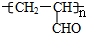 .H为含氯有机化合物,发生消去反应生成E,则G为
.H为含氯有机化合物,发生消去反应生成E,则G为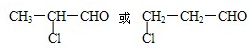 ,据此解答.
,据此解答. ,A在浓硫酸作用下发生消去反应生成D为CH2=CHCHO,E发生加聚反应生成F为
,A在浓硫酸作用下发生消去反应生成D为CH2=CHCHO,E发生加聚反应生成F为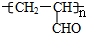 .H为含氯有机化合物,发生消去反应生成E,则G为
.H为含氯有机化合物,发生消去反应生成E,则G为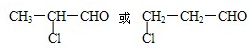 ,
, ,F的结构简式为
,F的结构简式为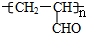 ,故答案为:
,故答案为: ;
;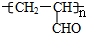 ;
;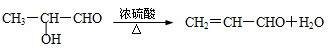 ,反应类型为:消去反应,
,反应类型为:消去反应, ;消去反应;
;消去反应;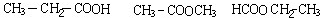 ,
,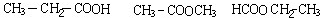 ;
;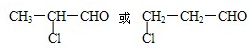 ,故答案为:
,故答案为: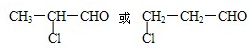 .
.


 小学期末标准试卷系列答案
小学期末标准试卷系列答案科目:高中化学 来源: 题型:
| A、一定不含Fe3+和Fe2+ |
| B、溶液可能含有AlO2- |
| C、溶液可能含有NO3- |
| D、可能含有Fe3+但一定不含Fe2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:
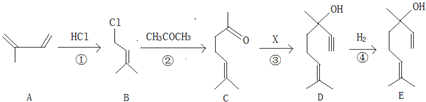
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、0.1mol的白磷(P4)或四氯化碳(CCl4)中所含的共价键数均为0.4NA |
| B、1L amol/L的氯化铁溶液中,若Fe3+的数目为NA,则Cl-的数目为3NA |
| C、0.1 molN2和0.3molH2在一定条件下充分反应,转移电子数目为0.6NA |
| D、常温常压下,65gZn与足量浓 H2SO4充分反应,转移电子数一定为2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
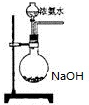 氨在国民经济中占有重要地位.
氨在国民经济中占有重要地位.查看答案和解析>>
科目:高中化学 来源: 题型:
| A、升温增压 | B、降温减压 |
| C、升温减压 | D、降温增压 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 物质 | CH3OH | CH3OCH3 | H2O |
| 浓度/(mol?L-1) | 0.64 | 0.50 | 0.50 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、阿司匹林具有解热镇痛作用 |
| B、可以用Si3N4、Al2O3制作高温结构陶瓷制品 |
| C、禁止使用四乙基铅作汽油抗爆震剂,可减少汽车尾气污染 |
| D、在入海口的钢铁闸门上装一定数量的铜块可防止闸门被腐蚀 |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、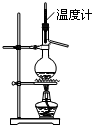 实验室用图所示装置制取乙烯 |
| B、由水电离出的c(H+)=10-13mol?L-1的溶液中,Na+、ClO-、K+、I-一定能大量共存 |
| C、肥皂的主要成分是高级脂肪酸盐 |
| D、某温度下Fe(OH)3的KSP=4×10-38,则该温度下,饱和溶液的c(OH-)=2×10-19 mol?L-1 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com