


科目:高中化学 来源: 题型:阅读理解
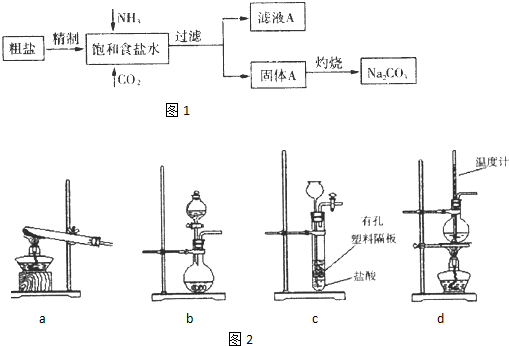
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)将K+、Na+、Mg2+大致分离,并把Cl-、Br-也大致分离开来,有以下的方法和步骤可供选择(有些可以重复使用):①溶于水配成稀溶液;②溶于水配成饱和溶液;③通入足量的CO2;④通入足量的氯水;⑤加入足量浓氨水;⑥过滤;⑦用CCl4萃取。最合理的方法和步骤的顺序依次是(用编号)___________________。
(2)分离后剩余的水溶液中所含的主要物质是______________________。
(3)如果上述分离过程中分离出的一种物质是小苏打,要得到干燥的小苏打应采取的最简单的措施是什么?
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com