
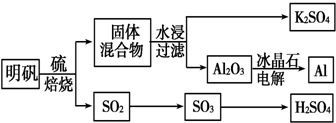
���� ���������շ���4KAl��SO4��2•12H2O+3S=2K2SO4+2Al2O3+9SO2��+48H2O�������������������������������������������������������������������98.3%��Ũ�������գ�SO3+H2O=H2SO4���Ƶ�����������ù��������ˮ����Ϊ��߽����ʣ��ɲ�ȡ�������������Ͻ��裬��ˮ�������Һ�������ᾧ�õ�K2SO4���壬����۵��Al2O3���Ƶ�Al���Դ˽����⣮
��� �⣺���������շ���4KAl��SO4��2•12H2O+3S=2K2SO4+2Al2O3+9SO2��+48H2O�������������������������������������������������������������������98.3%��Ũ�������գ�SO3+H2O=H2SO4���Ƶ�����������ù��������ˮ����Ϊ��߽����ʣ��ɲ�ȡ�������������Ͻ��裬��ˮ�������Һ�������ᾧ�õ�K2SO4���壬����۵��Al2O3���Ƶ�Al��
��1�����������շ���4KAl��SO4��2•12H2O+3S=2K2SO4+2Al2O3+9SO2��+48H2O����Ӧ��SS���������ɶ������ʻ�ԭ��ΪS���ʴ�Ϊ��S����
��2������Һ�л�þ��壬��Ҫ��������Ũ������ȴ�ᾧ�����˵Ȳ������ʴ�Ϊ�������ᾧ��
��3���ŵ�ʱNiO��OH��ת��ΪNi��OH��2��ͬʱ��������������Һ�ʼ��ԣ�������ƫ�����ƣ���Ӧ���ܷ���ʽΪAl+3NiO��OH��+NaOH+H2O�TNaAlO2+3Ni��OH��2��
�ʴ�Ϊ��Al+3NiO��OH��+NaOH+H2O�TNaAlO2+3Ni��OH��2��
���� ���⿼�����ʵ��Ʊ���Ϊ�߿��������ͣ���Ŀ�Ѷ��еȣ���������������ѧ�������������������ѧ��������û���֪ʶ���ʵ�������������ʵ��������


 ӥ�ɽ̸��νӽ̲ĺӱ�����������ϵ�д�
ӥ�ɽ̸��νӽ̲ĺӱ�����������ϵ�д� ���������ν�ϵ�д�
���������ν�ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��3��Ԫ��������� | |
| B�� | ÿһ�ж��зǽ���Ԫ�� | |
| C�� | ���ϵ��µ�1��Ԫ�صĵ����۵������ߣ�����17��Ԫ�صĵ����۵����� | |
| D�� | ֻ�е�2��Ԫ�ص�ԭ���������2������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
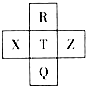 Ԫ��R��X��T��Z��Q��Ԫ�����ڱ��е����λ�����±���ʾ������R�����ڰ�����H2���һ��ϲ�������ը���������ж���ȷ���ǣ�������
Ԫ��R��X��T��Z��Q��Ԫ�����ڱ��е����λ�����±���ʾ������R�����ڰ�����H2���һ��ϲ�������ը���������ж���ȷ���ǣ�������| A�� | �ǽ����ԣ�Z��T��X | B�� | R��Q�ĵ��������26 | ||
| C�� | ��̬�⻯���ȶ��ԣ�R��T��Q | D�� | ����������ˮ��������ԣ�R��Q |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ��=4����
��=4����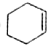 ��=2����
��=2���� ��=4��
��=4��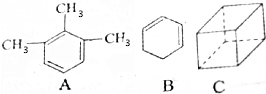
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
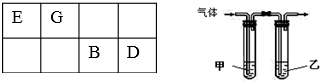
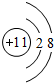 ��
��| ʵ���� | X���ʵ���Ũ�ȣ�mol•L-1�� | Y���ʵ���Ũ�ȣ�mol•L-1�� | �����Һ��pH |
| �� | 0.1 | 0.1 | pH=5 |
| �� | 0.2 | 0.1 | pH��7 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | X��������Y������ | |
| B�� | ����һ��ʱ���KOH�����ʵ������� | |
| C�� | ��ع���ʱ����һ��������Һ��pH��С | |
| D�� | ���ڱ�״����ͨ��5.6 L O2��ȫ��Ӧ������1.0mol���ӷ���ת�� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com