
【题目】若某原电池的离子方程式是Zn+Cu2+=Zn2++Cu,则该原电池的构成是( )
正极 | 负极 | 电解质溶液 | |
A | Cu | Zn | HCl |
B | Zn | Cu | CuSO4 |
C | Cu | Zn | CuSO4 |
D | Cu | Zn | ZnCl2 |
A. A B. B C. C D. D
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】能正确表示下列反应的离子反应方程式为( )
A.NH4HCO3溶液与过量的KOH溶液反应:NH4++HCO ![]() +2OH﹣=CO
+2OH﹣=CO ![]() +NH3↑+2H2O
+NH3↑+2H2O
B.向明矾溶液中滴加Ba(OH)2溶液,恰好使SO42﹣沉淀完全:2Al3++3SO ![]() +3Ba2++6OH﹣=2Al(OH)3↓+3BaSO4↓
+3Ba2++6OH﹣=2Al(OH)3↓+3BaSO4↓
C.向FeBr2溶液中通入足量氯气:2Fe2++4Br﹣+3Cl2=2Fe3++2Br2+6Cl﹣
D.醋酸除去水垢:2H++CaCO3=Ca2++CO2↑+H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】能正确表示下列反应的离子方程式的是( )
A.Cl2通入NaOH溶液:Cl2+OH﹣═Cl﹣+ClO﹣+H2O
B.NaHCO3溶液中加入稀HCl:CO ![]() +2H+═CO2↑+H2O
+2H+═CO2↑+H2O
C.AlCl3溶液中加入过量稀氨水:Al3++4NH3?H2O═AlO2﹣+4NH4++2H2O
D.Cu溶于稀HNO3:3Cu+8H++2NO3﹣═3Cu2++2NO↑+4H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知下列热化学方程式:Zn(s)+![]() O2(g)=ZnO(s) △H1=–351.1 kJ/mol
O2(g)=ZnO(s) △H1=–351.1 kJ/mol
Hg(l)+![]() O2(g)=HgO(s) △H2=–90.7 kJ/mol
O2(g)=HgO(s) △H2=–90.7 kJ/mol
由此可知反应Zn(s) + HgO(s) = ZnO(s) + Hg(l) △H3 ;其中△H3的值为 ( )
A. –441.8 kJ/mol B. –254.6 kJ/mol
C. –438.9 kJ/mol D. –260.4 kJ/mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】H2O2是一种绿色氧化还原试剂,在化学研究中应用广泛.
(1)某小组拟在同浓度Fe3+的催化下,探究H2O2浓度对H2O2分解反应速率的影响.限选试剂与仪器:30% H2O2、0.1molL﹣1 Fe2(SO4)3、蒸馏水、锥形瓶、双孔塞、水槽、胶管、玻璃导管、量筒、秒表、恒温水浴槽、注射器①写出本实验H2O2分解反应方程式并标明电子转移的方向和数目:
②设计实验方案:在不同H2O2浓度下,测定(要求所测得的数据能直接体现反应速率大小).
③设计实验装置,完成如1图所示的装置示意图.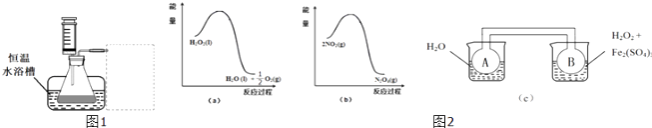
④参照下表格式,拟定实验表格,完整体现实验方案(列出所选试剂体积、需记录的待测物理量和所拟定的数据;数据用字母表示).
实验序号 | V[0.1molL﹣1 Fe2(SO4)3]/mL | ||||
1 | a | ||||
2 | a |
(2)利用图2(a)和2(b)中的信息,按图2(c)装置(连能的A、B瓶中已充有NO2气体)进行实验.可观察到B瓶中气体颜色比A瓶中的(填“深”或“浅”),其原因是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学与生活密切联系,下列与盐类水解无关的是( )
A. 用NaHCO3粉末作灭火剂
B. 实验室盛放Na2SiO3溶液的试剂瓶应用橡皮塞,而不能用玻璃塞
C. 实验室配制FeCl3溶液时,应先将其溶解在盐酸中,而后加水稀释
D. 加热蒸干A1C13溶液得到A1(OH)3固体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铁、钴(Co)、镍(Ni)是同族元素,它们的化合物在工业上有重要的应用。
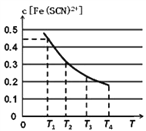
(1)现将含0.5mol FeCl3的溶液和含0.5mol KSCN的溶液混合,混合后溶液体积为1L,已知溶液存在平衡:Fe3+(aq)+SCN-(aq) ![]() Fe(SCN)2+(aq)(忽略其它过程)。平衡浓度c[Fe(SCN)2+]与温度T的关系如图所示:温度为T1时,反应在5秒钟时达到平衡,平衡时c[Fe(SCN)2+]=0.45 mol·L-1,求达到平衡时的平均反应速率v(SCN-)=____________,该温度下的Fe3+的平衡转化率为_____________,该温度下反应的平衡常数为__________。
Fe(SCN)2+(aq)(忽略其它过程)。平衡浓度c[Fe(SCN)2+]与温度T的关系如图所示:温度为T1时,反应在5秒钟时达到平衡,平衡时c[Fe(SCN)2+]=0.45 mol·L-1,求达到平衡时的平均反应速率v(SCN-)=____________,该温度下的Fe3+的平衡转化率为_____________,该温度下反应的平衡常数为__________。
(2)羰基法提纯镍涉及的一个反应为:Ni(s)+4CO(g)![]() Ni(CO)4(g)
Ni(CO)4(g)
①当温度升高时,![]() 减小,则该反应的⊿H_____0(填“>”或“<”)。
减小,则该反应的⊿H_____0(填“>”或“<”)。
②一定温度下,将一定量的粗镍和CO加入一恒压密闭容器中,下列示意图正确且能说明反应达到平衡状态的是________(填代号)。
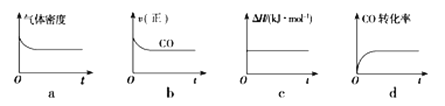
(3)CoxNi(1-x)Fe2O4 (其中Co、Ni均为+2价)可用作H2O2分解的催化剂,具有较高的活性。两种不同方法制得的催化剂在10℃时催化、分解6%的H2O2溶液的相对初始速率随x变化的曲线如右图所示。
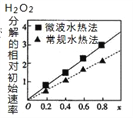
由图中信息可知__________法制取得到的催化剂活性更高;Co2+、Ni2+ 两种离子中催化效果较好的是_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在1L容器中充入0.5mol N2和1.5mol H2发生反应:N2(g)+3H2(g)![]() 2NH3(g)ΔH ="-92.4" kJmol-1,下列关于该反应的说法正确的是
2NH3(g)ΔH ="-92.4" kJmol-1,下列关于该反应的说法正确的是
A. 反应达到平衡时共放出46.2 kJ的热量
B. 若将容器体积压缩至0.5L,可提高单位体积内活化分子百分数,从而加快正反应速率,降低逆反应速率
C. 任何时刻均有:υ(N2)=3υ(H2)=2υ(NH3)
D. 若保持容器体积不变,继续通入0.5mol N2和1.5mol H2,则N2的转化率变大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列排列顺序不正确的是( )
A. 热稳定性:H2O>NH3>PH3
B. 原子半径:Si>Na>O
C. 碱性: CsOH>KOH>NaOH
D. 失电子能力:K>Na>Mg
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com