��úΪԭ�ϣ�����ѧ�ӹ�ʹúת��Ϊ���塢Һ�塢����ȼ���Լ����ֻ�����Ʒ�Ĺ�ҵ��ú������
��1����ˮ����ͨ�����ȵ�̼���ɲ���ˮú������ӦΪ��C��s��+H
2O��g��?CO��g��+H
2��g����H=+131.3kJ?mol
-1�ٸ÷�Ӧ�ڸ�����
��
��
�Է����У���ܡ����ܡ���
�ں����£����ݻ�������ܱ������У��������Ͽ��淴Ӧ��һ��ʱ��������������������仯ʱ���ܱ����÷�Ӧ�Ѵﵽƽ��״̬���ǣ�
D
D
��
����������ܶȣ��������������ѹǿ����������������ʵ�������CO���ʵ���Ũ��
A��ֻ�Т���
Bֻ�Т�͢�
C��ֻ�Т�͢�
D��ֻ�Т�͢�
��2��ˮú���ٽ�һ����Ӧ����ȡ��������ӦΪH
2O��g��+CO��g��?H
2��g��+CO
2��g����ij�¶��¸÷�Ӧ��ƽ�ⳣ��K=4/9�����¶����ڼס��ҡ������������ܱ������У�ֻͶ��H
2��g����CO
2��g��������ʼŨ���±���ʾ�������жϲ���ȷ����
C
C
| ��ʼŨ�� |
�� |
�� |
�� |
| c��H2��/mol/L |
0.010 |
0.020 |
0.020 |
| c��CO2��/mol/L |
0.010 |
0.010 |
0.020 |
A����Ӧ��ʼʱ�����еķ�Ӧ������죬���еķ�Ӧ����
B��ƽ��ʱ���кͱ��е�H
2��ת���ʾ���60%
C��ƽ��ʱ�����е�c��CO
2���Ǽ��е�2������0.102mol/L
D��ƽ��ʱ�����е�CO
2��ת���ʴ���60%
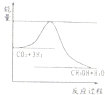
��3��Ŀǰ��ҵ����һ�ַ�������CO
2����ȡ�״���һ�������·�����Ӧ��CO
2��g��+3H
2��g��?CH
3OH��g��+H
2O��g������ͼ��ʾ�÷�Ӧ���й�������������λΪkJ?mol
-1���ı仯�������Ϊ1L�ĺ����ܱ������У�����1molCO
2��3molH
2��
�����д�ʩ����ʹƽ��������c��CH
3OH�����������
CD
CD
A�������¶�
B������He��g��ʹ��ϵѹǿ����
C����H
2O��g������ϵ�з������
D���ٳ���1molCO
2��3molH
2�����¶�T
1ʱ������Ӧ�ﵽƽ��ʱ�����n��H
2��=2.4mol�������������䣬���¶�T
2ʱ������Ӧ�ﵽƽ��ʱ�����n��CO
2��=0.82mol�����T
1��
��
T
2�����������������=����
��4����һ�������¿�ѧ�Ҵ��̵����з����CO
2��̫���ܵ�ص��ˮ������H
2�ϳɼ״���������ΪҺ�壩��CH
3OH��H
2��ȼ���ȷֱ�Ϊ����H=-725.5kJ/mol����H=-285.5kJ/mol
��д����ҵ����CO
2��H
2�ϳ�CH
3OH��Һ̬ˮ���Ȼ�ѧ����ʽ��
CO2��g��+3H2��g��=CH3OH��l��+H2O��l����H=-131.9kJ/mol
CO2��g��+3H2��g��=CH3OH��l��+H2O��l����H=-131.9kJ/mol
�ڸ�ת���Ļ���������
�ɽ�������ЧӦ���ֲ���Դ��ȱ
�ɽ�������ЧӦ���ֲ���Դ��ȱ
���������������Ʒ�ӦCO
2=C+O
2����H��0����S��0��������CO
2�Ի�����Ӱ�죮�����ж��Ƿ���в�˵�����ɣ�
�����У��÷�Ӧ��һ���������ؼ��ķ�Ӧ�����Բ����Է�����
�����У��÷�Ӧ��һ���������ؼ��ķ�Ӧ�����Բ����Է�����
��

 ��1����ˮ����ͨ�����ȵĽ�̿���ɲ���ˮú������ӦΪ��C��s��+H2O��g��?CO��g��+H2��g��һ���¶��£���һ���ݻ��ɱ���ܱ������У�����������Ӧ�����в����жϸ÷�Ӧ�ﵽ��ѧƽ��״̬����
��1����ˮ����ͨ�����ȵĽ�̿���ɲ���ˮú������ӦΪ��C��s��+H2O��g��?CO��g��+H2��g��һ���¶��£���һ���ݻ��ɱ���ܱ������У�����������Ӧ�����в����жϸ÷�Ӧ�ﵽ��ѧƽ��״̬����

 �����������Ů��ͯ������ϵ�д�
�����������Ů��ͯ������ϵ�д�

