
反应A(g)+B(s)===C(g) ΔH<0,在其他条件不变时,改变其中一个条件,则生成C的速率(填“加快”、“减慢”或“不变”):
(1)升温_____________________________________________________________;
(2)增大压强____________________________________________________________;
(3)增大容器容积_________________________________________________________;
(4)加入A______________________________________________________________;
(5)加入B______________________________________________________________;
(6)加正催化剂___________________________________________________________。
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
已知NaHSO3溶液显酸性,溶液中存在以下平衡:
HSO3―+ H2OH2SO3 + OH― ① HSO3―
H+ + SO32― ②
向0.1 mol · L -1的NaHSO3溶液中分别加入以下物质,下列有关说法正确的是
A.加入少量金属Na,平衡①左移,平衡②右移,溶液中c(HSO3―)增大
B.加入少量Na2SO3固体,则c(H+) + c(Na+) = c(HSO3―) + c(OH―) +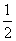 c(SO32―)
c(SO32―)
C.加入少量NaOH溶液,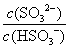 、
、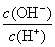 的值均增大
的值均增大
D.加入氨水至中性,则2c(Na+) = c(SO32―)>c(H+) = c(OH―)
查看答案和解析>>
科目:高中化学 来源: 题型:
已知A、B、C、D四种短周期元素,它们的核电荷数依次增大。A与C原子的基态电子排布中L能层都有两个未成对电子,C、D同主族。 E、F都是第四周期元素,E原子的基态电子排布中有4个未成对电子,F原子除最外能层只有1个电子外,其余各能层均为全充满。根据以上信息填空:
(1)基态D原子中,电子占据的最高能层符号 ,该能层具有的原子轨道数为 。
(2)E2+离子的价层电子排布图是 ,F原子的电子排布式是 。
(3)A元素的最高价氧化物对应的水化物中心原子采取的轨道杂化方式为 ,B元素的气态氢化物的VSEPR模型为 。
(4)化合物AC2、B2C和阴离子DAB-互为等电子体,它们结构相似,DAB-的电子式为 。
(5)配合物甲的焰色反应呈紫色,其内界由中心离子E3+与配位体AB-构成,配位数为6,甲的水溶液可以用于实验室中E2+离子的定性检验,检验E2+离子的离子方程为 。
(6)某种化合物由D,E,F三种元素组成,其晶胞如图所示,则其化学式为 ,该晶胞上下底面为正方形,侧面与底面垂直,根据图中所示的数据列式计算该晶体的密度d= g/cm3。(保留两位小数)
查看答案和解析>>
科目:高中化学 来源: 题型:
今有一种固体化合物X,X本身不导电,但熔融状态或溶于水时能够电离,下列关于该化合物X的说法中,正确的是( )
A.X一定为电解质 B.X可能为非电解质
C.X只能是盐类 D.X可以是任何化合物
查看答案和解析>>
科目:高中化学 来源: 题型:
反应A(g)+3B(g)===2C(g)+2D(g),在不同情况下测得的反应速率如下,其中反应速率最大的是( )
A.v(D)=0.4 mol·L-1·s-1
B.v(C)=0.5 mol·L-1·s-1
C.v(B)=0.6 mol·L-1·s-1
D.v(A)=0.15 mol·L-1·s-1
查看答案和解析>>
科目:高中化学 来源: 题型:
下列离子方程式改写为化学方程式,正确的是( )
A.Ag++Cl-===AgCl↓
AgNO3+NaCl===AgCl↓+NaNO3
B.Cu+2Ag+===Cu2++2Ag
Cu+2AgCl===CuCl2+2Ag
C.Ba2++SO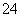 ===BaSO4↓
===BaSO4↓
Ba(OH)2+H2SO4===BaSO4↓+2H2O
D.CO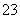 +2H+===CO2↑+H2O
+2H+===CO2↑+H2O
NaHCO3+HCl===NaCl+CO2↑+H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
A、B、C、D四种可溶性盐,它们的阳离子分别是Ba2+、Ag+、Na+、Cu2+,阴离子分别是NO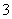 、SO
、SO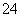 、Cl-、CO
、Cl-、CO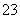 (离子不能重复出现),进行如下实验:
(离子不能重复出现),进行如下实验:
(1)分别溶于水,只有C溶液呈蓝色。
(2)若向溶于水的四种溶液中分别加入盐酸,B溶液中出现沉淀,D溶液中有气体逸出。
试确定四种物质的化学式:
A________,B________,C________,D________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于N2性质的叙述,错误的是( )
A.任何物质在N2中都不能燃烧
B.氮气既具有氧化性,又具有还原性
C.将空气中的N2转变成含氮化合物属于氮的固定
D.N2的化学性质很不活泼的原因是两个氮原子之间共用三对电子,使每个原子都达到稳定结构
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com