
| A. | 该反应在T1、T3温度时达到过化学平衡 | |
| B. | 该反应的正反应是吸热反应 | |
| C. | 该反应在T2温度时达到过化学平衡 | |
| D. | 升高温度,平衡会向正反应方向移动 |
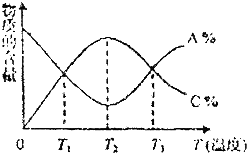
分析 T2℃之前A%变小,C%从0渐增大,而T2℃之后A%渐大,C%渐小,说明T2℃之前是反应没有达到平衡状态,而T2℃时恰好平衡,T2℃之后是温度升高使平衡向左移动,所以逆反应是吸热反应,正反应为放热反应,据此分析.
解答 解:T2℃之前A%变小,C%从0渐增大,而T2℃之后A%渐大,C%渐小,说明T2℃之前是反应没有达到平衡状态,而T2℃时恰好平衡,T2℃之后是温度升高使平衡向左移动,所以逆反应是吸热反应,正反应为放热反应.
A、T1温度之后A%继续变小,C%继续增大,T3温度之后A%继续增大,C%继续减小,故T1、T3温度时未达到化学平衡,故A错误;
B、T2℃时恰好平衡,T2℃之后A%渐大,C%渐小,说明T2℃之后是温度升高使平衡向左移动,所以逆反应是吸热反应,正反应为放热反应,故B错误;
C、T2℃之前A%变小,C%从0渐增大,而T2℃之后A%渐大,C%渐小,而T2℃时恰好平衡,故C正确;
D、T2℃时恰好平衡,T2℃之后A%渐大,C%渐小,说明T2℃之后是温度升高使平衡向左移动,所以逆反应是吸热反应,温度升高使平衡向逆反应移动,故D错误.
故选:C.
点评 本题考查化学平衡图象、温度对化学平衡的影响,难度中等,明确图象中含量随温度的平衡关系判断T2℃时恰好平衡是解题关键.


科目:高中化学 来源: 题型:选择题
| 温度 | Na2S2O3溶液的体积和浓度 | H2SO4溶液的体积和浓度 | |
| A | 50℃ | 5mL 0.5mol•L-1 | 5mL 0.5mol•L-1 |
| B | 50℃ | 50mL 0.1mol•L-1 | 50mL 0.1mol•L-1 |
| C | 50℃ | 10mL 0.2mol•L-1 | 10mL 0.2mol•L-1 |
| D | 50℃ | 15mL 0.1mol•L-1 | 15mL 0.1mol•L-1 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 物质的质量之比为9:1 | B. | 原子数之比为1:1 | ||
| C. | 分子数之比为1:1 | D. | 电子数之比为5:1 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 氯化铁溶液中通入硫化氢气体:2Fe3++S2-═2Fe2++S↓ | |
| B. | 碳酸钡中加入稀硫酸BaCO3+2H+═Ba2++CO2↑+H2O | |
| C. | 碳酸钙跟醋酸反应:CaCO3+2CH3COOH═Ca2++2CH3COO-+H2O+CO2↑ | |
| D. | 碳酸氢钠溶液中加入过量氢氧化钠溶液:HCO3-+OH-═CO32-+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | v(Fe)=0.5mol•(L•min)-1 | B. | v(H2SO4)=1mol•(L•min)-1 | ||
| C. | v(H2)=0.5mol•(L•min)-1 | D. | v=(FeSO4)=0.5mol•(L•min)-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常温常压下,48gO3含有的氧分子数为3NA | |
| B. | 标准状况下,1.8g的水中含有的氧原子数为0.1NA | |
| C. | 22.4 L O2中含有的氧气分子数约为6.02×1023 | |
| D. | 1mol O2氧气分子所占的体积数约为22.4 L |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 酸式滴定管滴至终点对,俯视读数 | |
| B. | 锥形瓶用蒸馏水洗后,未干燥 | |
| C. | 酸式滴定管用蒸馏水洗后,未用标准液润洗 | |
| D. | 酸式滴定管滴定至终点后,发现尖嘴处有气泡(原来无气泡) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙烯能发生加成反应 | |
| B. | 乙烯易溶于水,也易溶于有机溶剂 | |
| C. | 可用酸性高锰酸钾溶液鉴别乙烯与甲烷 | |
| D. | 乙烯的产量是衡量一个国家石油化工发展水平的标志 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com