
【题目】苯和溴取代反应的实验装置如图所示,其中A为由具支试管改制成的反应容器,在其下端开了一小孔,塞好石棉绒,再加入少量铁屑粉。填写下列空白:

(1)向反应容器A中逐滴加入溴和苯的混合液,几秒内就发生反应。写出A中所发生反应的化学方程式(有机物写结构简式):____________________________。
(2)B中NaOH溶液的作用是____________________。
(3)试管C中苯的作用是_______________________。
反应开始后,观察D和E两试管,看到的现象为____________________________,此现象可以验证苯和液溴的反应为____________(填反应类型)。
科目:高中化学 来源: 题型:
【题目】(1)研究物质时会涉及物质的组成、分类、性质和用途等方面。
①Na2O2属于____________(填物质的类别),检验其组成中所含阳离子的方法是_____________。
②将包有少量____色Na2O2固体的棉花放在石棉网上,用滴管向棉花上滴几滴水,观察到的现象是__________________,由此得出的结论是_________________________________。
③在潜水艇和消防员的呼吸面具中,Na2O2所发生反应的化学方程式为_________________________,从氧化剂和还原剂的角度分析,在该反应中Na2O2的作用是___________________。某潜水艇上有25人,如果每人每分钟消耗的O2在标准状况下体积为0.80L(标准状况下O2的密度为1.429g/L),假设所需要的O2全部由Na2O2来提供,则该潜水艇一天所需要的Na2O2的物质的量是_____________。
(2)写出下列反应的离子方程式:
①NaHCO3溶于醋酸:__________________________________________________。
②过量CO2与NaOH溶液:_____________________________________________。
③工业制漂白液:______________________________________________________。
④生活中漂白粉的漂白原理:____________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向10mL0.1mol·L-1 NH4Al(SO4)2溶液中,滴加等浓度Ba(OH)2溶液xmL。下列叙述正确的是( )
A. x=10时,溶液中有NH4+、Al3+、SO42-,且c(NH4+)>c(SO42-)
B. x=10时,溶液中有NH4+、AlO2-、SO42-,且c(NH4+)<c(Al3+)
C. x=30时,溶液中有Ba2+、AlO2-、OH-,且c(OH-)>c(Ba2+)
D. x=30时,溶液中有Ba2+、AlO2-、OH-,且c(OH-)<c(AlO2-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是制备和研究乙炔性质的实验装置图,有关说法正确的是( )
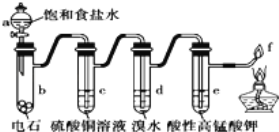
A. 用蒸馏水替代a中饱和食盐水产生的乙炔更为纯净
B. c(过量)的作用是除去影响后续实验的杂质
C. d、e褪色原理相同
D. f处产生明亮的蓝色火焰
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA表示阿伏加德罗常数的值,下列叙述正确的是
A. 1mol钠与氧气反应生成Na2O或Na2O2时,失电子数目均为NA
B. 7.8 g Na2O2中含有的阴离子数目为0.2NA
C. 将标准状况下11.2L的Cl2通入足量水中发生反应,转移的电子总数为0.5NA
D. 23 g Na 与足量H2O反应完全后可生成NA个H2分子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将一定质量的Mg和Al的混合物投入500 mL稀硫酸中,固体全部溶解并产生气体。待反应完全后,向所得溶液中加入NaOH溶液,生成沉淀的物质的量与加入NaOH溶液的体积关系如下图所示。则下列说法正确的是( )

A.Mg和Al的总质量为8 g
B.原稀硫酸溶液的物质的量浓度为5 mol·L-1
C.生成的H2在标准状况下的体积为11.2 L
D.NaOH溶液的物质的量浓度为5 mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在标准状况下,有物质①44.8LH2,②24gCH4,③1molH2O,④3.01×1023个O2,含分子数最多的是______(填序号,下同),含电子数最多的是______,质量最大的是______,体积最小的是______;密度由小到大的顺序为______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铬合金具有高硬度、耐腐蚀特性,广泛应用于精密仪器制造。由高碳铬铁合金废料粉末制取铬的简单流程如下:
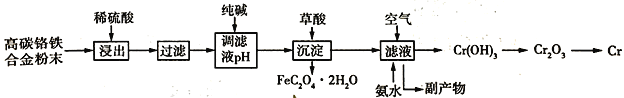
已知:Cr + H2SO4 = CrSO4 + H2↑
请回答下列问题:
(1)稀硫酸酸浸过程中,提高“浸出率”的措施有______________(合理、一条即可)
(2)用纯碱调节溶液酸度,若纯碱过量,则可能导致的后果是_________________,副产物直接排放环境不仅浪费,还污染水质。请你写出副产物的一个用途______________(合理给分)。
(3)加入草酸(H2C2O4)发生的离子方程式为__________________,铬属于难熔金属,写出工业中冶炼铬的化学方程式_________________。
(4)向滤液中通入空气,加入氨水后发生反应的化学方程式为_________________。
(5)已知高碳铬铁废料中铁铬元素质量之比为14:13。上述流程中铁元素转化为草酸亚铁的利用率为80%。废料中提取金属铬的总转化率为95%,如果得到草酸亚铁晶体(FeC2O42H2O)的质量为18.00 t ,则可以冶炼铬的质量为________t(结果保留1位小数)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某一反应体系中有反应物和生成物共五种物质:O2、H2CrO4、Cr (OH)3、H2O、H2O2。 已知该反应中H2O2只发生如下过程:H2O2→O2
(1)该反应中的还原剂是______________。
(2)该反应中,发生还原反应的过程是________→________。
(3)写出该反应的化学方程式,并用单线桥标出电子转移的方向和数目:__________。
(4)如反应转移了0.3 mol电子,则产生的气体在标准状况下体积为__________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com