
°Њћвƒњ°њ‘ƒґЅѕ¬Ѕ–”–єЎƒ№‘іµƒ≤ƒЅѕ£ђїЎір”–єЎќ ћв£Ї
£®1£©‘Џ≥£ќ¬£ђ1.01°Ѕ105Pa ±£ђ48g Љ„іЉ‘Џ„гЅњµƒ—х∆ш÷–≥дЈ÷»Љ…’…ъ≥…ґю—хїѓћЉЇЌ“ЇћђЋЃ£ђЈ≈≥ц1089kJµƒ»»Ѕњ£ђ‘т±н ЊЉ„іЉ»Љ…’»»µƒ»»їѓ—ІЈљ≥ћ љќ™____________________________°£
£®2£©‘Џ…ъ≤ъЇЌ…ъїо÷–Њ≠≥£”цµљїѓ—Іƒ№”лµзƒ№µƒѕаї•„™їѓ°£‘Џ»зЌЉЉ„°Ґ““Ѕљ„∞÷√÷–£ђЉ„÷–ЄЇЉЂµзЉЂЈі”¶ љќ™____________________________£ђЉ„÷–µƒ—фјл„”ѕт _______ ЉЂ“∆ґѓ£®ћо°∞’э°±їт°∞ЄЇ°±£©£ї““÷–¬ЅµзЉЂ„ч____ЉЂ£ђ““÷–’эЉЂµзЉЂЈі”¶ љќ™____________________________
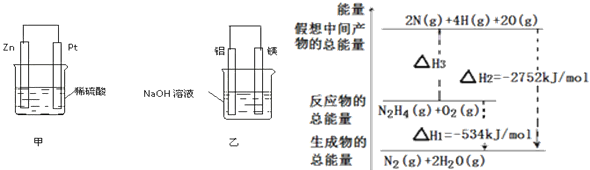
£®3£©л¬(N2H4)њ…„чќ™їрЉэЈҐґѓїъµƒ»ЉЅѕ£ђ”–єЎл¬їѓ—ІЈі”¶µƒƒ№Ѕњ±дїѓ»зЌЉЋщ Њ£ђ“—÷™ґѕЅ—1molїѓ—ІЉьЋщ–иµƒƒ№Ѕњ(kJ)£ЇN°‘Nќ™944°ҐO=Oќ™500°ҐN-Nќ™154£ђ‘тЈі”¶ќп„™їѓќ™÷–Љд≤ъќпµƒ¶§H3=_________£ђґѕЅ—1 mol N°™HЉьЋщ–иµƒƒ№Ѕњ «__________ kJ°£
£®4£©є§“µ÷∆«в∆шµƒ“їЄц÷Ў“™Јі”¶ «£ЇCO(g)+ H2O(g) =CO2(g) + H2(g),
“—÷™25°ж ±£Ї C( ѓƒЂ)+O2(g) = CO2(g) £ї °чH1 = -394 kJmol-1
C( ѓƒЂ)+![]() O2(g) = CO(g)£ї °чH2 = -111 kJmol-1
O2(g) = CO(g)£ї °чH2 = -111 kJmol-1
H2(g)+ ![]() O2 (g)=H2O(g)£ї °чH3= -242kJmol£≠1
O2 (g)=H2O(g)£ї °чH3= -242kJmol£≠1
‘Љ∆Ћг25°ж ±CO(g)+H2O(g)=CO2(g)+H2(g)µƒЈі”¶»»°чH£љ____________kJmol-1°£
°Њір∞Є°њCH3OH£®l£©+![]() O2(g)=CO2(g)+2H2O(l) °чH=-726kJ/moL Zn-2e-=Zn2+ ’э ЄЇ 2H2O+2e-=H2°ь+2OH- +2218kJ/moL 391 -39kJ/moL
O2(g)=CO2(g)+2H2O(l) °чH=-726kJ/moL Zn-2e-=Zn2+ ’э ЄЇ 2H2O+2e-=H2°ь+2OH- +2218kJ/moL 391 -39kJ/moL
°Њљвќц°њ
ЄщЊЁЄ«Ћєґ®¬…£ђ”…“—÷™»»їѓ—ІЈљ≥Ћ“‘ µ±µƒѕµ эљш––Љ”Љхєє‘мƒњ±к»»їѓ—ІЈљ≥ћ љ£ђЈі”¶»»“≤≥Ћ“‘ѕа”¶µƒѕµ э≤Ґљш––ѕа”¶µƒЉ”Љх£ђЊЁіЋЉ∆Ћг°£
£®1£©48g CH3OH‘Џ—х∆ш÷–»Љ…’…ъ≥…CO2ЇЌ“ЇћђЋЃ£ђЈ≈≥ц1089kJ»»Ѕњ£ђ32gЉі1mol CH3OH‘Џ—х∆ш÷–»Љ…’…ъ≥…CO2ЇЌ“ЇћђЋЃ£ђЈ≈≥ц726kJ»»Ѕњ£ђ‘т±н ЊЉ„іЉ»Љ…’»»µƒ»»їѓ—ІЈљ≥ћ љќ™£ЇCH3OH(g)+![]() O2(g)®TCO2(g)+2H2O(l) °чH= -726kJ/mol£ї
O2(g)®TCO2(g)+2H2O(l) °чH= -726kJ/mol£ї
£®2£©‘≠µз≥Ў÷–љѕїо∆√µƒљр ф «ЄЇЉЂ£ђ І»•µз„”£ђЈҐ…ъ—хїѓЈі”¶£ђЉ„÷–ЄЇЉЂµзЉЂЈі”¶ љќ™£ЇZn-2e-=Zn2+£ї‘≠µз≥Ў÷–—фјл„”ѕт’эЉЂ“∆ґѓ£ђЉіѕтPtµзЉЂ“∆ґѓ£ї
““÷–√Њµƒљр ф–‘«њ”Џ¬Ѕµƒ£ђµЂ√Њ≤ї”л«в—хїѓƒ∆»№“ЇЈі”¶£ђ¬Ѕ”л«в—хїѓƒ∆»№“ЇЈі”¶£ђ¬Ѕ Іµз„”„чќ™ЄЇЉЂ£ђ““÷–’эЉЂ…ѕЋЃµзјл≤ъ…ъµƒ«вјл„”µ√µз„”≤ъ…ъ«в∆ш£ђµзЉЂЈі”¶ љќ™2H2O+2e-=H2°ь+2OH-£ї
£®3£©ЄщЊЁЌЉѕсњ…÷™£ЇN2H4(g)+O2(g)=2N(g)+4H(g)+2O(g)
°чH3=2752kJ/mol-534kJ/mol=+2218kJ/mol£ї
їѓ—ІЈі”¶÷–£ђЊ…ЉьґѕЅ—ќь ’ƒ№Ѕњ£ђ…иґѕЅ—1molN-HЉьЋщ–иµƒƒ№Ѕњќ™x£ђ‘тЊ…ЉьґѕЅ—ќь ’µƒƒ№Ѕњ=154+4x+500=2218£ђљвµ√£Їx=391£ї
£®4£©“—÷™‘Џ25°ж ±£Ї
ҐўC( ѓƒЂ)+O2(g)®TCO2(g) °чH1= -394kJ/mol
ҐЏC( ѓƒЂ)+![]() O2(g)®TCO(g) °чH2= -111kJ/mol
O2(g)®TCO(g) °чH2= -111kJ/mol
ҐџH2(g)+![]() O2(g)®TH2O(g) °чH3= -242kJ/mol
O2(g)®TH2O(g) °чH3= -242kJ/mol
”…Є«Ћєґ®¬…£ђҐў-Ґџ-ҐЏµ√£ЇCO(g)+H2O(g)®TCO2(g)+H2(g)£ђє °чH=°чH1-°чH3-°чH2= -111kJ/mol -(-394kJ/mol)-(-242kJ/mol)= -39kJ/mol°£



| ƒкЉґ | Єя÷–њќ≥ћ | ƒкЉґ | ≥х÷–њќ≥ћ |
| Єя“ї | Єя“ї√вЈ—њќ≥ћЌ∆Љц£° | ≥х“ї | ≥х“ї√вЈ—њќ≥ћЌ∆Љц£° |
| Єяґю | Єяґю√вЈ—њќ≥ћЌ∆Љц£° | ≥хґю | ≥хґю√вЈ—њќ≥ћЌ∆Љц£° |
| Єя»э | Єя»э√вЈ—њќ≥ћЌ∆Љц£° | ≥х»э | ≥х»э√вЈ—њќ≥ћЌ∆Љц£° |
њ∆ƒњ£ЇЄя÷–їѓ—І јі‘і£Ї ћв–Ќ£Ї
°Њћвƒњ°њ“їґ®ќ¬ґ»ѕ¬,‘Џ2 Lµƒ√№±’»Ё∆ч÷–,X°ҐY°ҐZ»э÷÷∆шћеµƒЅњЋж ±Љд±дїѓµƒ«ъѕя»зЌЉЋщ Њ:

(1)і”Јі”¶њ™ Љµљ10 s ±,”√Z±н ЊµƒЈі”¶Ћў¬ ќ™°°°°°°°°°°°°°°°°,Xµƒќп÷ µƒЅњ≈®ґ»Љх…ўЅЋ°°°°°°°°,Yµƒ„™їѓ¬ ќ™°°°°°£
(2)Є√Јі”¶µƒїѓ—ІЈљ≥ћ љќ™°°
(3)10 sЇуµƒƒ≥“ї ±њћ(t1)Єƒ±дЅЋЌвљзћхЉю,∆дЋў¬ Ћж ±Љдµƒ±дїѓЌЉѕс»зЌЉЋщ Њ:

‘тѕ¬Ѕ–ЋµЈ®ЈыЇѕЄ√ЌЉѕсµƒ «°°°°°°°°°£
A.t1 ±њћ,‘ціуЅЋXµƒ≈®ґ» B.t1 ±њћ,…эЄяЅЋћеѕµќ¬ґ»
C.t1 ±њћ,Ћх–°ЅЋ»Ё∆чћеїэ D.t1 ±њћ, є”√ЅЋіяїѓЉЅ
≤йњіір∞ЄЇЌљвќц>>
њ∆ƒњ£ЇЄя÷–їѓ—І јі‘і£Ї ћв–Ќ£Ї
°Њћвƒњ°њ‘Ћ”√їѓ—ІЈі”¶‘≠јн—–ЊњЇѕ≥…∞±Јі”¶”–÷Ў“™“в“е£ђ«лЌк≥…ѕ¬Ѕ–ћљЊњ°£
£®1£©…ъ≤ъ«в∆ш£ЇљЂЋЃ’ф∆шЌ®єэЇм»»µƒћњЉі≤ъ…ъЋЃ√Ї∆ш°£C(s)£ЂH2O(g)![]() H2(g)£ЂCO(g) ¶§H£љ£Ђ131.3kJ°§mol£≠1£ђ¶§S£љ£Ђ133.7J°§mol£≠1°§K£≠1£ђ
H2(g)£ЂCO(g) ¶§H£љ£Ђ131.3kJ°§mol£≠1£ђ¶§S£љ£Ђ133.7J°§mol£≠1°§K£≠1£ђ
ҐўЄ√Јі”¶‘ЏµЌќ¬ѕ¬___________(ћо°∞ƒ№°±їт°∞≤їƒ№°±)„‘ЈҐљш––°£
ҐЏ–і≥цЄ√Јі”¶µƒ∆љЇв≥£ э±ніп љ_________________°£
£®2£©“—÷™‘Џ400°ж ±£ђN2(g)£Ђ3H2(g)![]() 2NH3(g)µƒK£љ0.5°£
2NH3(g)µƒK£љ0.5°£
Ґў‘Џ400°ж ±£ђ2NH3(g)![]() N2(g)£Ђ3H2(g)µƒK°д£љ________(ћо э÷µ)°£
N2(g)£Ђ3H2(g)µƒK°д£љ________(ћо э÷µ)°£
ҐЏ400°ж ±£ђ‘Џ0.5LµƒЈі”¶»Ё∆ч÷–љш––Їѕ≥…∞±Јі”¶£ђ“їґќ ±ЉдЇу£ђ≤вµ√N2°ҐH2°ҐNH3µƒќп÷ µƒЅњЈ÷±рќ™2mol°Ґ1mol°Ґ2mol£ђ‘тіЋ ±Јі”¶v(N2)’э________v(N2)ƒж(ћо°∞£Њ°±°Ґ°∞£Љ°±°Ґ°∞£љ°±їт°∞≤їƒ№»Јґ®°±)°£
Ґџ»ф‘ЏЇгќ¬°ҐЇг—єћхЉюѕ¬ѕт∆љЇвћеѕµ÷–Ќ®»лл≤∆ш£ђ‘тЇѕ≥…∞±Јі”¶µƒ∆љЇв________“∆ґѓ(ћо°∞ѕт„у°±°Ґ°∞ѕт„у°±їт°∞≤ї°±)£їЈі”¶µƒ¶§H__________(ћо°∞‘ціу°±°Ґ°∞Љх–°°±їт°∞≤їЄƒ±д°±)°£
£®3£©ЋЃ√Ї∆ш„™їѓЈі”¶CO(g)+H2O(g) ![]() CO2(g)+H2(g)‘Џ“їґ®ќ¬ґ»ѕ¬іпµљїѓ—І∆љЇв°£ѕ÷љЂ≤їЌђЅњµƒCO(g)ЇЌH2O(g)Ј÷±рЌ®»лµљћеїэќ™2LµƒЇг»Ё√№±’»Ё∆ч÷–љш––Јі”¶£ђµ√µљ»зѕ¬Ѕљ„йљћЊЁ£Ї
CO2(g)+H2(g)‘Џ“їґ®ќ¬ґ»ѕ¬іпµљїѓ—І∆љЇв°£ѕ÷љЂ≤їЌђЅњµƒCO(g)ЇЌH2O(g)Ј÷±рЌ®»лµљћеїэќ™2LµƒЇг»Ё√№±’»Ё∆ч÷–љш––Јі”¶£ђµ√µљ»зѕ¬Ѕљ„йљћЊЁ£Ї
µ—й±аЇ≈ | ќ¬ґ»/°ж | ∆р ЉЅњ/mol | ∆љЇвЅњ/mol | іпµљ∆љЇвЋщ–и ±Љд/min | ||
CO | H2O | H2 | CO | |||
1 | 650 | 4 | 2 | 1.6 | 2.4 | 5 |
2 | 900 | 2 | 1 | 0.4 | 1.6 | 3 |
Ґў µ—йl÷–“‘CO2±н ЊµƒЈі”¶Ћў¬ ќ™v(CO2)=____________£ї
ҐЏ µ—й1µƒ∆љЇв≥£ эK1_________£я µ—й2µƒ∆љЇв≥£ эK2(ћо°∞іу”Џ°±°±–°”Џ£ђ°∞µ»”Џ°±°∞≤їƒ№»Јґ®°±)°£
Ґџ Є√Јі”¶’эЈљѕтќ™_____________(ћо°∞ќь°±їт°ЃЈ≈°±)»»Јі”¶£ї
≤йњіір∞ЄЇЌљвќц>>
њ∆ƒњ£ЇЄя÷–їѓ—І јі‘і£Ї ћв–Ќ£Ї
°Њћвƒњ°њѕ¬√ж «ґ°іЉµƒЅљ÷÷ЌђЈ÷“мєєће£ђ∆дљбєєЉт љ°ҐЈ–µгЉ∞»џµг»зѕ¬±нЋщ Њ£Ї
“мґ°іЉ | еґ°іЉ | |
љбєєЉт љ |
|
|
Ј–µг/°ж | 108 | 82.3 |
»џµг/°ж | -108 | 25.5 |
ѕ¬Ѕ–ЋµЈ®≤ї’э»Јµƒ «
A. ”√ѕµЌ≥√ь√ыЈ®Єш“мґ°іЉ√ь√ыќ™£Ї2-Љ„їщ-1-±ыіЉ
B. “мґ°іЉµƒЇЋі≈є≤’с«в∆„”–»э„йЈе£ђ«“√жїэ÷Ѓ±» «1°√2°√6
C. ”√’фЅуµƒЈљЈ®њ…љЂ еґ°іЉі”ґю’яµƒїмЇѕќп÷–Ј÷јл≥цјі
D. Ѕљ÷÷іЉЈҐ…ъѕы»•Јі”¶Їуµ√µљЌђ“ї÷÷ѕ©ћю
≤йњіір∞ЄЇЌљвќц>>
њ∆ƒњ£ЇЄя÷–їѓ—І јі‘і£Ї ћв–Ќ£Ї
°Њћвƒњ°њ‘Џћеїэќ™1Lµƒ√№±’»Ё∆ч÷–![]() ћеїэ≤ї±д
ћеїэ≤ї±д![]() ≥д»л
≥д»л![]() ЇЌ
ЇЌ![]() £ђ“їґ®ћхЉюѕ¬ЈҐ…ъЈі”¶£Ї
£ђ“їґ®ћхЉюѕ¬ЈҐ…ъЈі”¶£Ї![]() £ђ≤вµ√
£ђ≤вµ√![]() ЇЌ
ЇЌ![]() µƒ≈®ґ»Ћж ±Љд±дїѓ»зЌЉЋщ Њ°£ѕ¬Ѕ–ЋµЈ®’э»Јµƒ «
µƒ≈®ґ»Ћж ±Љд±дїѓ»зЌЉЋщ Њ°£ѕ¬Ѕ–ЋµЈ®’э»Јµƒ «
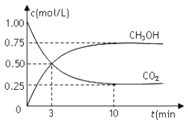
A.і”Јі”¶њ™ Љµљ∆љЇв£ђ«в∆шµƒ∆љЊщЈі”¶Ћў¬ ќ™![]()
B.љш––µљ3min ±£ђ’эЈі”¶Ћў¬ ЇЌƒжЈі”¶Ћў¬ ѕаµ»
C.10minЇу»Ё∆ч÷–Єчќп÷ µƒЅњ≈®ґ»≤ї‘ўЄƒ±д
D.µљіп∆љЇв„іћђ ±£ђЈі”¶Ј≈≥ц![]() µƒƒ№Ѕњ
µƒƒ№Ѕњ
≤йњіір∞ЄЇЌљвќц>>
њ∆ƒњ£ЇЄя÷–їѓ—І јі‘і£Ї ћв–Ќ£Ї
°Њћвƒњ°њ‘Џ“їґ®ћхЉюѕ¬їѓ—ІЈі”¶£Ї![]() ѕ÷”–»ЁїэѕаЌђ«“єћґ®≤ї±дµƒЉ„°Ґ““°Ґ±ы»эЄц»Ё∆ч£ђ‘Џ…ѕ цћхЉюѕ¬Ј÷±р≥д»лµƒ∆шћеЇЌЈі”¶Ј≈≥цµƒ»»Ѕњ
ѕ÷”–»ЁїэѕаЌђ«“єћґ®≤ї±дµƒЉ„°Ґ““°Ґ±ы»эЄц»Ё∆ч£ђ‘Џ…ѕ цћхЉюѕ¬Ј÷±р≥д»лµƒ∆шћеЇЌЈі”¶Ј≈≥цµƒ»»Ѕњ![]() »з±нЋщЅ–£Ї
»з±нЋщЅ–£Ї
»Ё∆ч |
|
| N2(mol) |
|
Љ„ | 2 | 1 | 0 |
|
““ | 1 |
| 0 |
|
±ы | 1 |
| 1 |
|
ЄщЊЁ“‘…ѕ эЊЁ£ђѕ¬Ѕ––р ц≤ї’э»Јµƒ «
A.![]()
B.![]()
C.![]()
D.‘Џ…ѕ цћхЉюѕ¬Јі”¶…ъ≥…![]() ∆шћеЈ≈»»
∆шћеЈ≈»»![]()
≤йњіір∞ЄЇЌљвќц>>
њ∆ƒњ£ЇЄя÷–їѓ—І јі‘і£Ї ћв–Ќ£Ї
°Њћвƒњ°њ“‘Mg∆ђЇЌAl∆ђќ™µзЉЂ£ђ≤Ґ”√µЉѕяЅђљ”£ђЌђ ±≤е»лNaOH»№“Ї÷–£ђѕ¬Ѕ–ЋµЈ®’э»Јµƒ «
A.Mg∆ђ„чЄЇЉЂ£ђµзЉЂЈі”¶£ЇMg£≠2e- ![]() Mg2+
Mg2+
B.Al∆ђ„чЄЇЉЂ£ђµзЉЂЈі”¶£ЇAl+4OH- £≠3e- ![]() AlO2- +2H2 O
AlO2- +2H2 O
C.µз„”і”MgµзЉЂ—ЎµЉѕяЅчѕтAlµзЉЂ
D.Al∆ђ…ѕ”–∆ш≈Ё≤ъ…ъ
≤йњіір∞ЄЇЌљвќц>>
њ∆ƒњ£ЇЄя÷–їѓ—І јі‘і£Ї ћв–Ќ£Ї
°Њћвƒњ°њ‘Џ√№±’»Ё∆ч÷–Ќ®»лA°ҐBЅљ÷÷∆шће£ђ‘Џ“їґ®ћхЉюѕ¬ є÷ЃЈҐ…ъ»зѕ¬Јі”¶£Ї2A(g)£ЂB(g)![]() 2C(g)(’эЈі”¶ќ™Ј≈»»Јі”¶)£ђіпµљ∆љЇвЇу£ђЄƒ±д“їЄцћхЉю(x)(Їб„ш±к)£ђѕ¬Ѕ–(y)(„Ё„ш±к)“їґ®ЈыЇѕЌЉ÷–Ћщ Њ±дїѓєЎѕµµƒ «( )
2C(g)(’эЈі”¶ќ™Ј≈»»Јі”¶)£ђіпµљ∆љЇвЇу£ђЄƒ±д“їЄцћхЉю(x)(Їб„ш±к)£ђѕ¬Ѕ–(y)(„Ё„ш±к)“їґ®ЈыЇѕЌЉ÷–Ћщ Њ±дїѓєЎѕµµƒ «( )

Ґўx±н Њќ¬ґ»£ђy±н ЊCµƒ÷ Ѕњ
ҐЏx±н Њ—є«њ£ђy±н ЊїмЇѕ∆шћеµƒ∆љЊщѕаґ‘Ј÷„”÷ Ѕњ
Ґџx±н Њ‘ўЉ”»лAµƒ÷ Ѕњ£ђy±н ЊAµƒ∞ўЈ÷ЇђЅњ
Ґ№x±н Њ‘ўЉ”»лAµƒ÷ Ѕњ£ђy±н ЊAµƒ„™їѓ¬
ҐЁx±н Њ‘ўЉ”»лAµƒ÷ Ѕњ£ђy±н ЊBµƒ„™їѓ¬
Ґёx±н Њќ¬ґ»£ђy±н ЊBµƒ„™їѓ¬
A.ҐўҐџҐЁB.ҐЏҐџҐЁC.ҐџҐ№ҐЁD.Ґ№ҐЁҐё
≤йњіір∞ЄЇЌљвќц>>
њ∆ƒњ£ЇЄя÷–їѓ—І јі‘і£Ї ћв–Ќ£Ї
°Њћвƒњ°њЄщЊЁѕ¬ ц„™їѓєЎѕµ£ђїЎірќ ћв£Ї

“—÷™£ЇҐў£ЂCH3Br![]() CH3£ЂHBr£ї
CH3£ЂHBr£ї
ҐЏCќп÷ ±љїЈ…ѕ“ї¬±іъќп÷ї”–Ѕљ÷÷°£
(1)–і≥цBќп÷ µƒ√ы≥∆__________£їDќп÷ µƒљбєєЉт љ________°£
(2)–і≥цЈі”¶ҐЏµƒја–Ќ________£їЈі”¶ҐЁµƒћхЉю________°£
(3)–і≥цЈі”¶Ґёµƒїѓ—ІЈљ≥ћ љ£Ї________________________________°£
(4)–і≥цD£ЂEЈі”¶µƒїѓ—ІЈљ≥ћ љ£Ї_______________°£
(5)Јі”¶ҐЏїє”–њ…ƒ№…ъ≥…“ї÷÷C16H18µƒ”–їъќп£ђ∆д±љїЈ…ѕ“ї¬±іъќп“≤÷ї”–Ѕљ÷÷£ђ–і≥цЋьµƒљбєєЉт љ£Ї_______________________________°£
≤йњіір∞ЄЇЌљвќц>>
∞ўґ»÷¬–≈ - ЅЈѕ∞≤бЅ–±н - ‘ћвЅ–±н
Їю±± °ї•Ѕ™Ќшќ•Ј®ЇЌ≤їЅЉ–≈ѕҐЊў±®∆љћ® | Ќш…ѕ”–Ї¶–≈ѕҐЊў±®„®«ш | µз–≈’©∆≠Њў±®„®«ш | …жјъ Ј–йќё÷ч“е”–Ї¶–≈ѕҐЊў±®„®«ш | …ж∆у«÷»®Њў±®„®«ш
ќ•Ј®ЇЌ≤їЅЉ–≈ѕҐЊў±®µзї∞£Ї027-86699610 Њў±®” ѕд£Ї58377363@163.com