
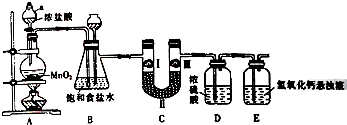
 氯气在工农业生产在应用非常广泛.如图是实验室制备氯气并进行一系列相关实验的装置.
氯气在工农业生产在应用非常广泛.如图是实验室制备氯气并进行一系列相关实验的装置.| 选项 | a | b | c |
| Ⅰ | 湿润的有色布条 | 湿润的有色布条 | 湿润的有色布条 |
| Ⅱ | 碱石灰 | 浓硫酸 | 无水氯化钙 |
| Ⅲ | 湿润的有色布条 | 干燥的有色布条 | 干燥的有色布条 |
分析 (1)由仪器a的结构可知,a为分液漏斗;
(2)制备的氯气中含有HCl,饱和食盐水吸收HCl;C中堵塞时,A、B装置内压强增大,B中饱和食盐水会被压入长颈漏斗中;
(3)通过Ⅰ、Ⅲ的有色布条对比验证,Ⅱ处为干燥剂,只能为固体干燥剂且不能与氯气反应,D中浓硫酸防止E中水蒸气进入C中;
(4)氯气有毒,氢氧化钙溶液吸收氯气,防止污染环境.
解答 解:(1)由仪器a的结构可知,a为分液漏斗,
故答案为:分液漏斗;
(2)盐酸易挥发,制备的氯气中含有HCl,饱和食盐水除去Cl2中的HCl气体;C中堵塞时,A、B装置内压强增大,饱和食盐水会被压入长颈漏斗中,B的现象为:锥形瓶中液面下降,长颈漏斗中液面上升,
故答案为:除去Cl2中的HCl气体;锥形瓶中液面下降,长颈漏斗中液面上升;
(3)通过Ⅰ、Ⅲ的有色布条对比验证,Ⅱ处为干燥剂,只能为固体干燥剂且不能与氯气反应,D中浓硫酸防止E中水蒸气进入C中,装置C中Ⅰ、Ⅱ、Ⅲ处依次放入湿润的有色布条、氯化钙、干燥的有色布条,
故选:c;
(4)氯气有毒,装置E中氢氧化钙悬浊液的作用是:吸收多余的Cl2,防止污染空气,反应离子方程式为:Ca(OH)2+Cl2=Ca2++Cl-+ClO-+H2O,
故答案为:吸收多余的Cl2,防止污染空气;Ca(OH)2+Cl2=Ca2++Cl-+ClO-+H2O.
点评 本题考查氯气的实验室制备与性质实验,涉及化学仪器、对装置的分析与评价等,关键是明确实验原理,难度不大.


科目:高中化学 来源: 题型:选择题
| A. | X中一定不存在FeO | |
| B. | Y中一定含有MnO2,Fe2O3 | |
| C. | Z溶液中一定含有Na2SO4,不能确定是否含有AlCl3 | |
| D. | 不溶物Y中一定含有Fe和CuO |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 实验操作 | 实验现象 | 解释或结论 |
| A | 向盛有某溶液的试管中滴加NaOH溶液,将湿润的红色石蕊试纸放在试管口 | 试纸未变蓝 | 该溶液中不含NH4+ |
| B | 用高锰酸钾溶液检验乙烯中混有的SO2 | 高锰酸钾溶液褪色 | 乙烯中混有SO2 |
| C | 向氯化钡溶液中通入CO2 | 得到白色沉淀 | 生成了BaCO3 |
| D | 淀粉KI溶液中滴入氯水,再通入SO2 | 先变蓝后褪色 | SO2有还原性 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用FeCl3溶液腐蚀铜线路板:Cu+Fe3+═Cu2++Fe2+ | |
| B. | Na2O2与H2O反应产生O2:2Na2O2+2H2O═4Na++4OH-+O2↑ | |
| C. | 将铁溶于稀盐酸:2Fe+6H+═2Fe3++3H2↑ | |
| D. | 向氯化铝溶液中加入过量的氨水:Al3++4NH3•H2O═AlO2-+4NH4++2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 已知甲烷的燃烧热为890.3kJ/mol,则甲烷燃烧的热化学方程式可表示为CH4(g)+2O2(g)═2CO2(g)+2H2O(g)△H=-890.3 kJ/mol | |
| B. | 已知C(石墨,s)═C(金刚石,s)△H>0,则金刚石比石墨稳定 | |
| C. | 已知中和热为△H=-57.3 kJ/mol,则1mol稀硫酸和足量稀NaOH溶液反应的反应热就是中和热 | |
| D. | 已知S(g)+O2(g)═SO2(g)△H1;S(s)+O2(g)═SO2(g)△H2,则△H1<△H2 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 除①④外 | B. | 除②外 | C. | 除⑤外 | D. | 全有关 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com