
| A. | C2H6 | B. | C4H6 | C. | C5H10 | D. | C6H12O2 |
分析 等物质的量均设为1mol,有机物CxHyOz完全燃烧耗氧量取决于(x+$\frac{y}{4}$-$\frac{z}{2}$),(x+$\frac{y}{4}$-$\frac{z}{2}$)值越大耗氧量越大,以此来解答.
解答 解:设均为1mol,则
A.消耗氧气为1mol×(2+$\frac{6}{4}$)=3.5mol;
B.消耗氧气为1mol×(4+$\frac{6}{4}$)=5.5mol;
C.消耗氧气为1mol×(5+$\frac{10}{4}$)=7.5mol;
D.消耗氧气为1mol×(6+$\frac{12}{4}$-$\frac{2}{2}$)=8mol,
故选D.
点评 本题考查有机物燃烧反应的计算,为高频考点,把握燃烧规律及消耗氧气的计算方法为解答的关键,侧重分析与计算能力的考查,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A.铝热反应 | B.燃料燃烧 | C.酸碱中和反应 | D.Ba(OH)2•8H2O与NH4Cl固体混合 |
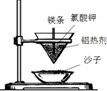 |  | 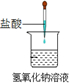 | 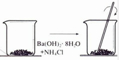 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 组分 | CO | CO2 | H2 |
| 体积分数 | 20% | 5% | 75% |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 放电时,正极反应式为Cn[AlCl4]+e-═[AlCl4]-+Cn | |
| B. | 充电时,阴极反应式为4[Al2Cl7]-3e-═Al+7[AlCl4]- | |
| C. | 放电过程中,负极每消耗1mol Al,导线中转移的电子数为3NA(NA为阿伏伽德罗常数的值) | |
| D. | 充、放电过程中,R+的移动方向相反 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
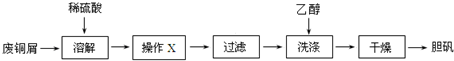
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

| 实验操作 | 实验现象与结论 |

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 元素 | X | F | |
| 电离能/kJ•mol-1 | I1 | 717 | 759 |
| I2 | 1509 | 1561 | |
| I3 | 3248 | 2957 | |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com