
 ③
③ .
. 分析 计算水、二氧化碳的物质的量,根据原子守恒确定烃的分子式,由分子式确定烃的种类,结合碳链异构确定同分异构体的种类,以此解答该题.
解答 解:10.8g H2O的物质的量为$\frac{10.8g}{18g/mol}$=0.6mol,11.2LCO2(标准状况下)的物质的量为$\frac{11.2L}{22.4L/mol}$=0.5mol,则有机物分子中N(C)=$\frac{0.5mol}{0.1mol}$=5、N(H)=$\frac{0.6mol×2}{0.1mol}$=12,故该烃的分子式为C5H12,对应的同分异构体有CH3-CH2-CH2-CH2-CH3、 、
、 ,
,
故答案为:C5H12;CH3-CH2-CH2-CH2-CH3; ;
; .
.
点评 本题考查烃燃烧有关计算、有机物分子式确定、同分异构体书写,侧重于考查的分析、计算能力的考查,难度不大,注意掌握有机物燃烧有关规律.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:实验题
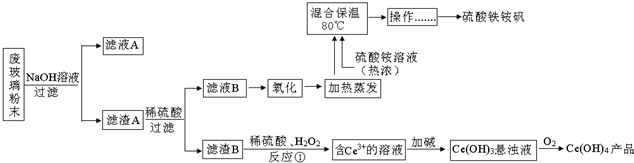

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
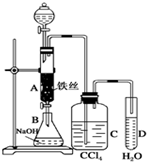 某化学课外小组用如图所示的装置制取溴苯.先向分液漏斗中加入苯和液溴,再将混合液慢慢滴入反应器A(A下端活塞关闭)中.
某化学课外小组用如图所示的装置制取溴苯.先向分液漏斗中加入苯和液溴,再将混合液慢慢滴入反应器A(A下端活塞关闭)中. .
.查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | c(CO32-)=0.01mol•L-1,c(NH4+)<c(SO42-) | |
| B. | 如果上述6种离子都存在,则c(Cl-)>c(SO42-) | |
| C. | 一定存在SO42-、CO32-、NH4+,可能存在Cl-、Na+、K+ | |
| D. | 一定存在SO42-、CO32-、NH4+、Cl-,一定不存在Na+、K+ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
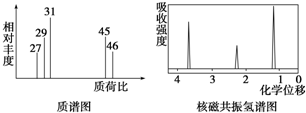
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
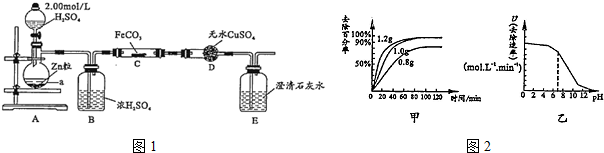
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
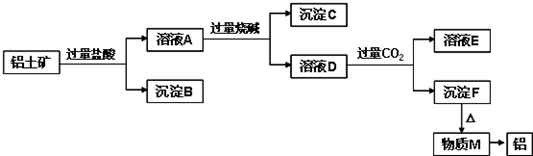
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
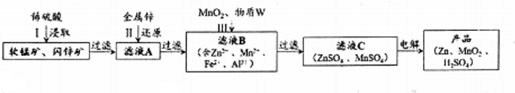
| Zn2+ | Mn2+ | Fe2+ | Fe3+ | Al3+ | |
| pH | 8.0 | 10.1 | 9.0 | 3.2 | 4.7 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1 mol AlCl3在熔融状态时离子总数为0.4NA | |
| B. | 一定量的浓硫酸与Xg Zn反应,若转移的电子为0.4 mol,则参加反应的硫酸分子数目一定等于0.4NA | |
| C. | 高温下,16.8g Fe与足量水蒸气反应,转移的电子数为0.7NA | |
| D. | 向含有0.2 mol FeCl3的两份溶液中分别滴加过量Na2S、通入过量H2S气体,则产生的沉淀比为:$\frac{0.3{N}_{A}}{0.1{N}_{A}}$ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com