
【题目】现在污水治理越来越引起人们重视,可以通过膜电池除去废水中的乙酸钠和对氯苯酚(![]() ),其原理如下图所示,下列说法正确的是
),其原理如下图所示,下列说法正确的是

A.该装置为电解装置,B为阳极
B.A极的电极反应式为 ![]() + e- = Cl- +
+ e- = Cl- + ![]()
C.当外电路中有0.1 mol e-转移时,A极区增加的H+的个数为0.1 NA
D.电子从B极沿导线经小灯泡流向A极
【答案】D
【解析】
该装置中没有电源,为原电池。原电池中阳离子移向正极,根据原电池中氢离子的移动方向可知A为正极,正极有氢离子参与反应,电极反应式为![]() + 2e-+H+ = Cl- +
+ 2e-+H+ = Cl- + ![]() ,结合原电池原理分析解答。
,结合原电池原理分析解答。
A.该装置中没有电源,为原电池,根据氢离子的移动方向可知,A为正极,B为负极,故A错误;
B.![]() + e- = Cl- +
+ e- = Cl- + ![]() 质量不守恒,A为正极,正极有氢离子参与反应,电极反应式为
质量不守恒,A为正极,正极有氢离子参与反应,电极反应式为![]() + 2e-+H+ = Cl- +
+ 2e-+H+ = Cl- + ![]() ,故B错误;
,故B错误;
C.根据电荷守恒,当外电路中有0.2mole-转移时,通过质子交换膜的H+的个数为0.2NA,而发生![]() + 2e-+H+ = Cl- +
+ 2e-+H+ = Cl- + ![]() ,则A极区增加的H+的个数为0.1NA,故C错误;
,则A极区增加的H+的个数为0.1NA,故C错误;
D.原电池中电子从负极B沿导线经小灯泡流向正极A,故D正确;
故选D。


科目:高中化学 来源: 题型:
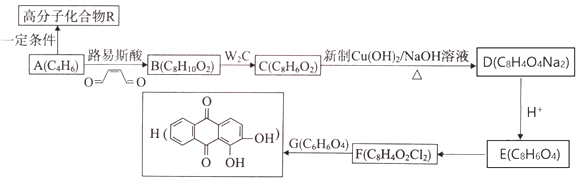
【题目】十九大报告中指出,“大力保障和改善民生,让广大人民群众病有所医、老有所养。”茜草素H( )对金黄色葡萄球菌的生长有抑制作用,一种合成茜草素的线路设计如下:
)对金黄色葡萄球菌的生长有抑制作用,一种合成茜草素的线路设计如下:
请回答下列问题:
已知: 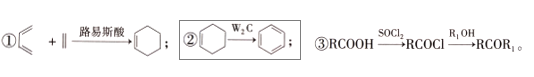
(1)H中所含官能团的名称是__________________,C的名称是_________________。
(2)A→B反应类型是_______________。C→D反应类型是_______________。
(3)写出C→D的化学方程式:______________________________________________________。
(4)G的结构简式为____________X是A的加聚产物,则其顺式结构的结构简式为__________。
(5)写出E与乙二醇的缩聚反应的化学方程式:_____________________________________。
(6)芳香族化合物Y是B的同分异构体,同时符合下列条件的Y共有_______种。
A.1 mol Y能消耗 1 mol NaOH B.Y能与FeCl3溶液发生显色反应
C.苯环上有3个取代基
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氰化钠是一种剧毒物质,工业上常用硫代硫酸钠溶液处理废水中的氰化钠。硫代硫酸钠的工业制备原理为:2Na2S+Na2CO3+4SO2===3Na2S2O3+CO2 。某化学兴趣小组拟用该原理在实验室制备硫代硫酸钠,并检测氰化钠废水处理排放情况。
I.实验室通过如图所示装置制备Na2S2O3

(1)实验中要控制SO2生成速率,可采取的措施有_____________(写出一条)。
(2)b装置的作用是_____________ 。
(3)反应开始后,c 中先有淡黄色浑浊产生,后又变为澄清,此浑浊物为__________(填化学式)。
(4)实验结束后,在e处最好连接盛__________(填“NaOH 溶液”、“水”、“CCl4”中的一种) 的注射器,接下来的操作为______________,最后拆除装置。
II.氰化钠废水处理
(5)已知: a.废水中氰化钠的最高排放标准为0.50mg/L;
b.Ag++2CN-==[Ag(CN)2]-,Ag++I-=AgI↓,AgI 呈黄色,且CN-优先与Ag+反应。
实验如下: 取20.00mL处理后的氰化钠废水于锥形瓶中,并滴加几滴KI溶液作指示剂,用1.00×10-4mol/L的标准AgNO3溶液滴定,消耗AgNO3溶液的体积为1.50mL。
①滴定时1.00×10-4mol/L的标准AgNO3溶液应用________(填仪器名称) 盛装; 滴定终点时的现象是______________。
②处理后的废水是否达到排放标准_______(填“是”或“否”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有关下列四组实验描述不正确的是

A. 加热甲装置中的烧杯可以分离SiO2和NH4Cl
B. 利用装置乙可证明非金属性强弱:Cl>C>Si
C. 打开丙中的止水夹,一段时间后,可观察到烧杯内溶液上升到试管中
D. 向丁中铁电极区滴入2滴铁氰化钾溶液,一段时间后,烧杯中不会有蓝色沉淀生成
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1) KClO3+ 6HCl (浓)=3Cl2 ↑+KCl +3H2O其中氧化剂为______;还原产物为_______;氧化产物与还原产物的质量比为_________; 浓盐酸在反应中表现出来的性质是 ________ (填写编号)
①只有还原性 ②还原性和酸性 ③只有氧化性 ④氧化性和酸性
(2)用双线桥法标出以上反应的电子转移的方向和数目___________
(3)Fe(OH)3胶体的制备:取一小烧杯,加入25 mL蒸馏水,加热至沸腾,然后向沸水中逐滴加入5 ~ 6滴___________,继续煮沸至体系呈______________,停止加热,即制得Fe(OH)3胶体。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】燃煤的烟气中含有 SO2,为了治理雾霾天气,工厂采用多种方法实现烟气脱硫。
Ⅰ.(1)“湿式吸收法”利用吸收剂与 SO2 发生反应从而脱硫。下列试剂中适合用作该法吸收剂的是_____(填字母序号)。
a. 石灰乳 b.CaCl2溶液
(2)某工厂利用含 SO2 的烟气处理含Cr2O72-的酸性废水,吸收塔中反应后的铬元素以Cr3+形式存在,具体流程如下:
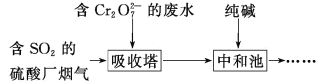
①用 SO2 处理含铬废水时,利用了 SO2 的_____性。
②吸收塔中发生反应的离子方程式为_____。
Ⅱ.石灰-石膏法和烧碱法是常用的烟气脱硫法。石灰-石膏法的吸收反应为Ca(OH)2+SO2= CaSO3↓+H2O。吸收产物亚硫酸钙由管道输送至氧化塔氧化,反应为2CaSO3+O2+4H2O =2CaSO4·2H2O。其流程如图:
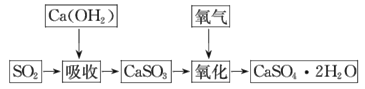
烧碱法的吸收反应为2NaOH+SO2=Na2SO3+H2O。该法的特点是氢氧化钠碱性强、吸收快、效率高。其流程如图:

已知:
试剂 | Ca(OH)2 | NaOH |
价格(元/kg) | 0.36 | 2.9 |
吸收 SO2 的成本(元/mol) | 0.027 | 0.232 |
(3)石灰-石膏法和烧碱法相比,石灰-石膏法的优点是_______,缺点是_______。
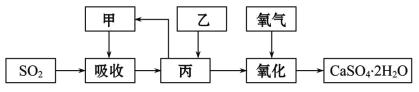
(4)某学习小组在石灰-石膏法和烧碱法的基础上,设计一个改进的、能实现物料循环的烟气脱硫方案,流程图中的甲、乙、丙各是_____、_____、_____(填化学式)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有关下列四个常用电化学装置的叙述中,正确的是
|
|
|
|
图Ⅰ 碱性锌锰电池 | 图Ⅱ 铅蓄电池 | 图Ⅲ 电解精炼铜 | 图Ⅳ 银锌纽扣电池 |
A. 图Ⅰ所示电池中,锌为负极,MnO2的作用是催化剂
B. 图II所示电池二氧化铅为正极,放电过程中硫酸浓度不变
C. 图III所示装置工作过程中,电解质溶液中Cu2+浓度始终不变
D. 图IV所示电池工作过程中,Ag2O是氧化剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述正确的是( )
A. Fe与S混合加热生成FeS2
B. NaHCO3的热稳定性大于Na2CO3
C. 过量的铜与浓硝酸反应有一氧化氮生成
D. 白磷在空气中加热到一定温度能转化为红磷
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有关分子结构如图所示,下列叙述中,正确的是 ( )
![]()
A. 除苯环外的其余碳原子有可能都在一条直线上
B. 所有的原子都在同一平面上
C. 12个碳原子不可能都在同一平面上
D. 12个碳原子有可能都在同一平面上
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com