
【题目】某温下气体反应达到化学平衡,平衡常数K=c(A)·c2(B)/[c2(E)·c(F)],恒容时,若温度适当降低,F的浓度增加,下列说法正确的是( )
A. 增大c(A)、c(B),K增大
B. 降低温度,正反应速率增大
C. 该反应的焓变为负值
D. 该反应的化学方程式为2E(g)+F(g)![]() A(g)+2B(g)
A(g)+2B(g)
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.![]() 表示放热反应,
表示放热反应,![]() 表示吸热反应
表示吸热反应
B.在化学反应中发生物质变化的同时,不一定发生能量变化
C.![]() 的大小与热化学方程式中化学计量数有关
的大小与热化学方程式中化学计量数有关
D.生成物释放的总能量大于反应物吸收的总能量时,![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】酞菁钴被广泛应用于光电材料、光动力学光敏材料等方面。酞菁钴(II)结构如图所示(Co均形成单键,部分化学键未画明)。下列说法错误的是( )
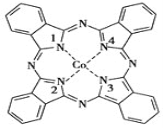
A.酞菁钴(II)中三种非金属元素的电负性大小顺序为N>C>H
B.酞菁钴(II)中碳原子的杂化方式只有sp2杂化
C.1号和3号N原子的VSEPR模型均为平面三角形
D.2号和4号N原子与Co(Ⅱ)是通过配位键结合
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲酸钙用途广泛,可用于高硫烟气脱硫助剂,也可作为制备草酸的中间体.据最新文献,氢氧化钙碳基化合成甲酸钙的反应如下:
![]() 反应1
反应1
(1)反应体系中存在以下两个竞争反应
![]() 反应2
反应2
![]() 反应3
反应3
![]() 二氧化碳与氢气直接合成甲酸的热化学反应方程式为 ______ .
二氧化碳与氢气直接合成甲酸的热化学反应方程式为 ______ .
![]() 为了更有利于生成甲酸钙,应选择的反应条件是较低的温度和 ______
为了更有利于生成甲酸钙,应选择的反应条件是较低的温度和 ______ ![]() 填编号
填编号![]() .
.
A.催化剂![]() 低压
低压![]() 高压
高压
(2)如图1是反应2和反应3,lnK与温度T的关系;同一条件时反应2的K ______ ![]() 填“大于”或“小于”
填“大于”或“小于”![]() 反应3的K,这对于 ______
反应3的K,这对于 ______ ![]() 填“反应2”或“反应3”
填“反应2”或“反应3”![]() 不利的.
不利的.
(3)以氢氧化钙初始密度为![]() 、CO的分压为
、CO的分压为![]() 条件下催化反应,以氢氧化钙转化率
条件下催化反应,以氢氧化钙转化率![]() 为坐标,时间为横坐标得到如图2;
为坐标,时间为横坐标得到如图2;

![]() 根据图象选择合适的反应温度 ______ ;理由是 ______ .
根据图象选择合适的反应温度 ______ ;理由是 ______ .
![]() 当
当![]() 为
为![]() 时,产物中甲酸钙与碳酸钙的质量比为50:1,氢氧化钙有 ______
时,产物中甲酸钙与碳酸钙的质量比为50:1,氢氧化钙有 ______ ![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下,下列各组离子在指定溶液中能大量共存的是
A. 0.1 mol·L1NaOH溶液:Na+、K+、![]() 、
、![]()
B. 0.1 mol·L1FeCl2溶液:K+、Mg2+、![]() 、
、![]()
C. 0.1 mol·L1K2CO3溶液:Na+、Ba2+、Cl、OH
D. 0.1 mol·L1H2SO4溶液:K+、![]() 、
、![]() 、
、![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】能正确表达下列反应的离子方程式为
A. 用醋酸除去水垢:2H++CaCO3=Ca2++CO2↑+H2O
B. 硫化亚铁与浓硫酸混合加热:2H++FeS=H2S↑+ Fe2+
C. 向硫酸铝溶液中滴加碳酸钠溶液:2Al3++3![]() =Al2(CO3)3↓
=Al2(CO3)3↓
D. 用氢氧化钠溶液吸收工业废气中的NO2:2NO2+2OH-=![]() +
+![]() + H2O
+ H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】滴定是一种重要的定量实验方法:
I. 常温下,用0.1000 mol/L NaOH溶液分别滴定20.00 mL 等浓度的盐酸和醋酸溶液,得到两条滴定曲线,如下图所示:
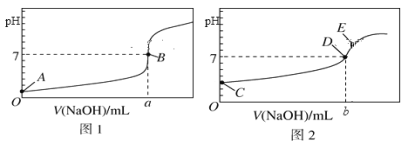
(1)滴定盐酸的曲线是图__________(填“1”或“2”)。
(2)滴定前CH3COOH的电离度为__________(电离度=![]() ×100%)。
×100%)。
(3)达到B、D状态时,反应消耗的NaOH溶液的体积a__________b(填“>”“<”或“=”);若图中E点pH=8,则c(Na+)-c(CH3COO-)的精确值为__________mol/L。
Ⅱ. 现使用酸碱中和滴定法测定市售白醋中醋酸的浓度
(1)实验步骤:
①量取10.00 mL市售白醋,在烧杯中用水稀释后转移到100 mL容量瓶中定容,摇匀得待测白醋溶液。
②用酸式滴定管取待测白醋溶液20.00 mL于锥形瓶中,向其中滴加2滴酚酞作指示剂。
③读取盛装0.1000 mol/L NaOH 溶液的碱式滴定管的初始读数。
④滴定。当___________________时,停止滴定,并记录NaOH溶液的最终读数。
⑤重复②、③、④步骤3次。
数据记录如下:
滴定次数 实验数据(mL) | 1 | 2 | 3 | 4 |
V(样品) | 20.00 | 20.00 | 20.00 | 20.00 |
V(NaOH)(消耗) | 15.95 | 15.00 | 15.05 | 14.95 |
(2)数据处理:
根据实验数据计算,可得市售白醋中醋酸的浓度为_________ mol/L
(3)误差在本实验的滴定过程中,下列操作会使实验结果偏大的是_________。
a.碱式滴定管在滴定时未用标准NaOH溶液润洗
b.碱式滴定管的尖嘴在滴定前有气泡,滴定后消失
c.锥形瓶中加入待测白醋溶液后,再加入少量水
d.锥形瓶在滴定时剧烈摇动,有少量液体溅出
e.滴定前平视读数,滴定后俯视读数
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某二元弱酸的酸式盐NaHA溶液,若pH<7,则溶液中各离子的浓度关系不正确的是( )
A. c(Na+)>c(HA-)>c(H+)>c(A2-)>c(OH-) B. c(H+)+ c(A2-)= c(OH-)+ c(H2A)
C. c(Na+)= c(HA-)+ c(H2A)+ c(A2-) D. c(Na+)+ c(H+)= c(HA-)+2 c(A2-)+ c(OH-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以下是合成一种功能高分子I的路线图。
 已知以下信息:
已知以下信息:
①RCN![]() RCOOH
RCOOH
②烃E的相对分子质量为92
回答下列问题:
(1)G中官能团的名称为__,__;
(2)反应①和⑥的反应类型分别为__,__;
(3)下列关于物质C的说法错误的是__(填字母标号)
A.可利用红外光谱法确定物质C中的官能团
B.物质C存在顺反异构体
C.物质C能与NaHCO3反应产生气体
D.物质C最多有8个原子共平面
(4)反应④的化学方程式为__;
(5)F的同分异构体中含有苯环且苯环上连有3个硝基的结构共有__种。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com