
����������Ԫ��X��Y��Z��W��ԭ��������������Xԭ�ӵ����������������ڲ��������2����Y�ǵؿ��к�����ߵ�Ԫ�أ�Z2����Y2��������ͬ�ĵ��Ӳ�ṹ��W��Yͬ���塣����˵����ȷ����
A. ZԪ�صļ�������������������Ԫ�صļ����Ӱ뾶��С��
B. Y�ļ���̬�⻯������ȶ��Ա�W��ǿ
C. Y��W�γɵĻ�����һ����ʹ���Ը��������Һ��ɫ
D. ����������Ӧˮ���������X��W��ǿ
 �������Ӧ���⼯ѵϵ�д�
�������Ӧ���⼯ѵϵ�д� �ۺ��Բ�ϵ�д�
�ۺ��Բ�ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
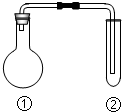 ����ѡ���еķ�Ӧ�������������ȫһ�µ��ǣ��г֡�����װ������ȥ����������
����ѡ���еķ�Ӧ�������������ȫһ�µ��ǣ��г֡�����װ������ȥ����������| ���еķ�Ӧ | ���е����� | ���� | |
| A | MnO2��Ũ������� | KI������Һ�ܿ���� | Cl2�������� |
| B | Cu��Ũ������� | ��ˮ��ɫ | SO2��Ư���� |
| C | Na2CO3�������Һ | ��������Һ����� | ���ԣ�̼����� |
| D | ��ʯ�뱥��ʳ��ˮ | ���Ը��������Һ��ɫ | ��Ȳ�л�ԭ�� |
| A�� | A | B�� | B | C�� | C | D�� | D |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ͨ������SO2��Na+��S2-��OH-��AlO2- | B�� | ͨ������CO2��K+��Ca2+��Cl-��NO3- | ||
| C�� | ͨ������Cl2��SO2��Ba2+��Cl-��K+ | D�� | ͨ������NH3��Fe3+��Cl-��Ba2+��Al3+ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
| A�� | Ԫ��X������ͬλ�� | |
| B�� | ����һ��ͬλ��������Ϊ36 | |
| C�� | ������Ϊ35��ͬλ��ԭ�ӵ���������Ϊ75% | |
| D�� | Ԫ�ص���X2��ƽ��ʽ��Ϊ71 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2017�����ʡ��ɳ�и�����ѧ�ڵ�13���ܲ������ۺϻ�ѧ�Ծ� ���ͣ�ʵ����
����ʯ(Na3 AlF6)������ˮ���㷺Ӧ��������ұ������ҵ����өʯ(CaF2)Ϊԭ������Na3 AIF6��
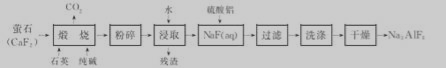
�ش��������⣺
��1��Na3AIF6Ϊ���ܼ���ұ�����Ļ�ѧ����ʽΪ ��
��2��д������ʱ�ܷ�Ӧ�Ļ�ѧ����ʽΪ________��
��3�����պ�Ĺ����ڽ�ȡǰ���з����Ŀ����____��Ϊ�ﵽ��ͬĿ�ģ����½�ȡʱ���ɲ�ȡ�Ĵ�ʩ��____��
��4��д����NaF��Һ�м�����������Һ������Ӧ�����ӷ���ʽ��____��NaF��Һ�ʼ��ԣ������ӷ���ʽ��ʾ��ԭ�� ������ڰ���ѧ����������������Һǰ�����������ὫNaF��Һ��pH�µ���5���ң�������ܲ��������� ��
��5��97.5kg��CaF280%өʯ�����ʲ�����Ԫ�أ������Ͽ�����Na3 AIF6 kg�������������е�ÿһ���������ʾ���ȫת������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2017�����ʡ��ɳ�и�����ѧ�ڵ�13���ܲ������ۺϻ�ѧ�Ծ� ���ͣ�ѡ����
�ҹ������������ӡ��������˴����Ļ�ѧ��Ӧ�������У��١���ɰ(HgS)��֮��ˮ���������ֻ��ɵ�ɰ���� �ڡ�������Ϳ��������ɫ��ͭ���������й�������ȷ����
A������ˮ���������ֻ��ɵ�ɰ��˵��ˮ�������˻�ԭ��Ӧ
B�����з�Ӧ�����ӷ���ʽΪ��2Fe+3Cu2+=2Fe3++3Cu
C�����ݢٿ�֪�¶ȼƴ��ƺ��������۸���ˮ������ֹ�ж�
D��ˮ���ܸ�������û���Ӧ���ɵ���ͭ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
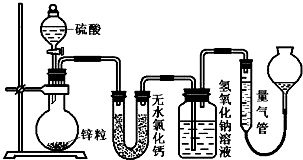
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
| ʵ���� | ��ʼŨ��/mol•L-1 | ��Ӧ����Һ��pH | |
| c��HA�� | c��NaOH�� | ||
| �� | 0.1 | 0.1 | 9 |
| �� | X | 0.2 | 7 |
| �� | 0.2 | 0.1 | 4.8 |
| �� | 0.1 | 0.2 | y |
| A�� | ʵ��ٷ�Ӧ�����Һ�У�c��HA��ԼΪ$\frac{{K}_{W}}{1��1{0}^{-9}}$mol•L-1 | |
| B�� | ʵ��ڷ�Ӧ�����Һ�У�c��HA����c��Na+��=c��A-����c��H+��=c��OH-�� | |
| C�� | ʵ��۷�Ӧ�����Һ�У�c��HA��+c��H+��=c��OH-��+c��A-�� | |
| D�� | ʵ��ܷ�Ӧ�����Һ�У�c��OH-��-c��H+��-c��HA��=0.05mol•L-1 |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com