
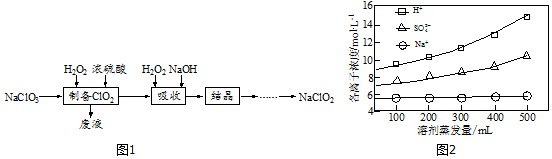
���� ��1�������̿�֪�����ơ��������⡢Ũ���ᷴӦ�Ʊ�ClO2���壬��������غ��д��
��2������ͼʾ���ܼ�����������������Ũ�Ȼ������䣬�����ӡ����������Ũ������
��3������ˮԡ�����¶ȣ�
�ڹ����������ȷֽ⣬ClO2�����ڼ�����Һ�л�ת��ΪClO3-��ClO2-��
��4��������Ϣ��NaClO2�������ȶ�����ʪ��NaClO2���ȵ�130��ֽ⣬ѡ��ʱӦע���¶Ⱥ��
��� �⣺��1�������ơ��������⡢Ũ���ᷴӦ�Ʊ�ClO2���壬��ӦΪ��2NaClO3+H2O2+H2SO4=2ClO2��+O2��+Na2SO4+2H2O��
�ʴ�Ϊ��2NaClO3+H2O2+H2SO4=2ClO2��+O2��+Na2SO4+2H2O��
��2������ͼʾ���ܼ�����������������Ũ�Ȼ������䣬�����ӡ����������Ũ������ȡ1L��Һ�������ľ���ΪNa2SO4��NaHSO4��
�ʴ�Ϊ��Na2SO4��NaHSO4��
��3��������ʱ������Ʒ�Ӧ�¶�Ϊ3�棬ѡ��3����ˮԡ��
�ʴ�Ϊ��3����ˮԡ��
���¶ȹ��ߣ�H2O2�ȷֽ���ʧ������ClO2����H2O2�����㣬�ڼ�����Һ�����������Σ���Ʒ�Ĵ��Ȼή�ͣ�
�ʴ�Ϊ��H2O2�ȷֽ���ʧ������ClO2����H2O2�����㣬�ڼ�����Һ�����������Σ�
��4����֪��NaClO2�������ȶ�����ʪ��NaClO2���ȵ�130��ֽ⣬��NaClO2��Һ��ѹ��������Һ��״��������ò�Ʒ��
�ʴ�Ϊ��ab��
���� ���⿼�������ʵ��Ʊ����漰�Թ������̵����⡢������ԭ��Ӧ���������Ŀ���ѡ�������⣬����ԭ���ǽ���Ĺؼ����Ƕ�ѧ���ۺ������Ŀ��飬��Ҫѧ���߱���ʵ�Ļ��������������������Ŀ�Ѷ��еȣ�


 Сѧ��10���ӿ������100��ϵ�д�
Сѧ��10���ӿ������100��ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 8�� | B�� | 7�� | C�� | 6�� | D�� | 5�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ����KMnO4��Һ��ͨ��SO2������Ϻ�ɫ��ʧ | |
| B�� | ���з�̪��NaOH��Һ��ͨ��SO2������ɫ��ʧ | |
| C�� | Ʒ����Һ��ͨ��SO2������ɫ��ʧ | |
| D�� | ��ˮ��ͨ��SO2������ɫ��ʧ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 1 mol����-CH3������������Ϊ9NA | |
| B�� | 26 g C2H2�ͱ������Ļ��������������Cԭ����Ϊ2NA | |
| C�� | ��״���£�B2H6��g����C2H4�Ļ������22.4 L�������ĵ�����ԼΪ16NA | |
| D�� | ��Ũ���������£�60g��������������ˮ�Ҵ���Ӧ�������������ķ�����ΪNA |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
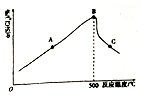 SiCl4��������Ϊ��ɫҺ�壬�ӷ�����ǿ�ҵĴ̼�����ζ����ҵ�ϣ��ᴿ�ֹ��ԭ�����£��ֹ�$��_{��}^{HCl}$SiCl4$��_{��}^{Si+H_{2}}$SiHCl3$��_{��}^{H_{2}}$Si������
SiCl4��������Ϊ��ɫҺ�壬�ӷ�����ǿ�ҵĴ̼�����ζ����ҵ�ϣ��ᴿ�ֹ��ԭ�����£��ֹ�$��_{��}^{HCl}$SiCl4$��_{��}^{Si+H_{2}}$SiHCl3$��_{��}^{H_{2}}$Si�������鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
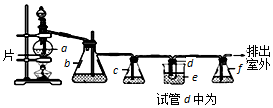
| �Ҵ� | 1��2-�������� | ���� | |
| ״̬ | ��ɫҺ�� | ��ɫҺ�� | ��ɫҺ�� |
| �ܶ�/g•cm-3 | 0.79 | 2.2 | 0.71 |
| �е�/�� | 78.5 | 132 | 34.6 |
| �۵�/�� | -130 | 9 | -116 |
 ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ����ͨ�������Һ�У�CH3COOH+NH3�TCH3COO-+NH4+ | |
| B�� | ������Һ��ͨ��������CO2��C6H5O-+CO2+H2O��C6H5OH+HCO3- | |
| C�� | �����ʵ���Cl2��FeBr2����Һ��Ӧ��2Fe2++4Br-+3Cl2�T2Fe3++2Br2+6Cl- | |
| D�� | ���Ե缫�������ͭ��Һ��2Cu2++2H2O$\frac{\underline{\;���\;}}{\;}$2Cu+O2��+4H+ |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com