
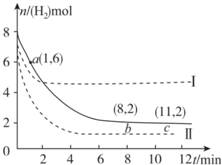
 T”ꏱ£¬6 mol CO2ŗĶ 8 mol H2³äČė2 LĆܱÕČŻĘ÷ÖŠ£¬·¢Éś·“Ó¦CO2£Øg£©+3H2£Øg£©?CH3OH£Øg£©+H2O£Øg£©£¬ČŻĘ÷ÖŠH2µÄĪļÖŹµÄĮæĖꏱ¼äµÄ±ä»ÆČēĶ¼ÖŠŹµĻßĖłŹ¾£®Ķ¼ÖŠŠéĻß±ķŹ¾½öøıäijŅ»·“Ó¦Ģõ¼žŹ±£¬H2µÄĪļÖŹµÄĮæĖꏱ¼äµÄ±ä»Æ£®ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ£Ø””””£©
T”ꏱ£¬6 mol CO2ŗĶ 8 mol H2³äČė2 LĆܱÕČŻĘ÷ÖŠ£¬·¢Éś·“Ó¦CO2£Øg£©+3H2£Øg£©?CH3OH£Øg£©+H2O£Øg£©£¬ČŻĘ÷ÖŠH2µÄĪļÖŹµÄĮæĖꏱ¼äµÄ±ä»ÆČēĶ¼ÖŠŹµĻßĖłŹ¾£®Ķ¼ÖŠŠéĻß±ķŹ¾½öøıäijŅ»·“Ó¦Ģõ¼žŹ±£¬H2µÄĪļÖŹµÄĮæĖꏱ¼äµÄ±ä»Æ£®ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ£Ø””””£©| A£® | ·“Ó¦æŖŹ¼ÖĮaµćŹ±v£ØH2£©=1 mol•L-1•min-1 | |
| B£® | ČōĒśĻߢń¶ŌÓ¦µÄĢõ¼žøıäŹĒÉżĪĀ£¬ŌņøĆ·“Ó¦”÷H£¾0 | |
| C£® | ĒśĻߢņ¶ŌÓ¦µÄĢõ¼žøıäŹĒ¼õÉŁŃ¹Ēæ | |
| D£® | T”ꏱ£¬øĆ·“Ó¦µÄ»ÆŃ§Ę½ŗā³£ŹżĪŖ0.125 |
·ÖĪö A£®øł¾Żv=$\frac{”÷c}{”÷t}$¼ĘĖć·“Ó¦æŖŹ¼ÖĮaµćŹ±ÓĆĒāĘų±ķŹ¾µÄ·“Ó¦ĖŁĀŹ£»
B£®ČēøĆ·“Ó¦”÷H£¾0£¬ÉżøßĪĀ¶ČĘ½ŗāÓ¦ĻņÕż·“Ó¦·½ĻņŅĘ¶Æ£»
C£®Čē½µµĶŃ¹Ē棬·“Ó¦ĖŁĀŹ¼õŠ”£¬“ļµ½Ę½ŗāĖłÓĆŹ±¼ä½Ļ³¤£»
D£®Ź×ĻČ¼ĘĖćĘ½ŗāŹ±ø÷ĪļÖŹµÄÅØ¶Č£¬½ų¶ų¼ĘĖćĘ½ŗā³£Źż£®
½ā“š ½ā£ŗA£®v£ØH2£©=$\frac{”÷c}{”÷t}$=$\frac{\frac{8mol-6mol}{2L}}{1min}$=1 mol•L-1•min-1£¬¹ŹAÕżČ·£»
B£®ČōøĆ·“Ó¦”÷H£¾0£¬ÉżøßĪĀ¶ČĘ½ŗāÓ¦ĻņÕż·“Ó¦·½ĻņŅĘ¶Æ£¬ŌņĘ½ŗāŹ±H2µÄĪļÖŹµÄĮæÓ¦Š”ÓŚT”ꏱ£¬ÓėĶ¼Ļó²»·ū£¬¹ŹB“ķĪó£»
C£®Čē½µµĶŃ¹Ē棬·“Ó¦ĖŁĀŹ¼õŠ”£¬“ļµ½Ę½ŗāĖłÓĆŹ±¼ä½Ļ³¤£¬µ«Ķ¼ÖŠĒśĻß·“Ó¦ĖŁĀŹ½Ļ“󣬓ļµ½Ę½ŗāŹ±¼ä½Ļ¶Ģ£¬ÓėĶ¼Ļó²»·ū£¬¹ŹC“ķĪó£»
D£®T”ꏱ£¬“ļµ½Ę½ŗāŹ±H2µÄĪļÖŹµÄĮæĪŖ2mol£¬øł¾Ż·“Ó¦CO2£Øg£©+3H2£Øg£©?CH3OH£Øg£©+H2O£Øg£©æÉÖŖ£¬Ę½ŗāŹ±£¬c£ØCO2£©=$\frac{6mol-2mol}{2L}$=2mol/L£¬c£ØH2£©=$\frac{2mol}{2L}$=1mol/L£¬c£ØCH3OH£©=$\frac{2mol}{2L}$=1mol/L£¬c£ØH2O£©£©=$\frac{2mol}{2L}$=1mol/L£¬Ōņk=$\frac{c£ØC{H}_{3}OH£©•c£Ø{H}_{2}O£©}{c£ØC{O}_{2}£©•{c}^{3}£Ø{H}_{2}£©}$=$\frac{1”Į1}{2”Į{1}^{3}}$=0.5£¬¹ŹD“ķĪó£»
¹ŹŃ”A£®
µćĘĄ ±¾Ģāæ¼²é»Æѧ·“Ó¦ĖŁĀŹ”¢Ę½ŗāŅĘ¶Æ¼°¼ĘĖćµÄĶ¼ĻóµČÖŖŹ¶£¬ĢāÄæÄѶČÖŠµČ£¬±¾Ģā×¢Ņā·ÖĪöĶ¼ĻóÖŠĒāĘųµÄĪļÖŹµÄĮæµÄ±ä»Æ£¬½įŗĻ·“Ó¦µÄĢŲµćÅŠ¶ĻĶā½ēĢõ¼ž¶ŌĘ½ŗāŅĘ¶ÆµÄÓ°Ļģ£¬ŹŌĢāÅąŃųĮĖѧɜµÄ·ÖĪö”¢Ąķ½āÄÜĮ¦¼°»Æѧ¼ĘĖćÄÜĮ¦£®


 100·Ö“³¹ŲĘŚÄ©³å“ĢĻµĮŠ“š°ø
100·Ö“³¹ŲĘŚÄ©³å“ĢĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 3£¬3 ¶ž¼×»ł¶”Ķé | B£® | 2£¬2 ¶ž¼×»ł¶”Ķé | ||
| C£® | 2 ŅŅ»ł¶”Ķé | D£® | 2£¬3£¬3 Čż¼×»ł¶”Ķé |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
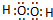 £¬WµŚŅ»²½µēĄė·½³ĢŹ½ĪŖH2O2?H++HO2-£®
£¬WµŚŅ»²½µēĄė·½³ĢŹ½ĪŖH2O2?H++HO2-£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā

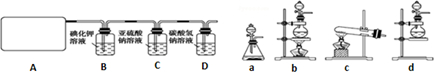
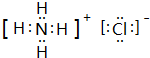 £¬IµÄ»ÆѧŹ½Mg£ØOH£©2£»
£¬IµÄ»ÆѧŹ½Mg£ØOH£©2£»²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | CuSO4+H2SØTCuS”ż+H2SO4 | |
| B£® | 2FeCl3+CuØT2FeCl2+CuCl2 | |
| C£® | .Cu2 £ØOH£©2CO3 $\frac{\underline{\;\;”÷\;\;}}{\;}$2CuO+CO2”ü+H2O | |
| D£® | 4Fe£ØOH£©2+O2+2H2OØT4Fe£ØOH£©3 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
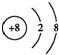 £»A”¢FĮ½ŌŖĖŲ×é³ÉµÄ»ÆŗĻĪļµē×ÓŹ½ĪŖNa+[£ŗH]-£®
£»A”¢FĮ½ŌŖĖŲ×é³ÉµÄ»ÆŗĻĪļµē×ÓŹ½ĪŖNa+[£ŗH]-£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
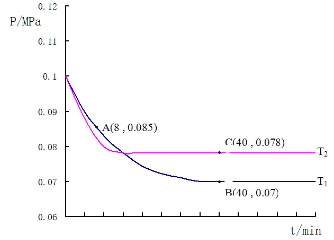 SO2¾¹ż¾»»ÆŗóÓėæÕĘų»ģŗĻ½ųŠŠ“ß»ÆŃõ»ÆŗóÖĘČ”ĮņĖį»ņÕßĮņĖįļ§£¬ĘäÖŠSO2·¢Éś“ß»ÆŃõ»ÆµÄ·“Ó¦ĪŖ£ŗ2SO2£Øg£©+O2£Øg£©?2SO3£Øg£©£®ČōŌŚT1”ę”¢0.1MPaĢõ¼žĻĀ£¬ĶłŅ»ĆܱÕČŻĘ÷ĶØČėSO2ŗĶO2£ØĘäÖŠn£ØSO2£©£ŗn£ØO2£©=2£ŗ1£©£¬²āµĆČŻĘ÷ÄŚ×ÜŃ¹ĒæÓė·“Ó¦Ź±¼äČēĶ¼ĖłŹ¾£ŗ
SO2¾¹ż¾»»ÆŗóÓėæÕĘų»ģŗĻ½ųŠŠ“ß»ÆŃõ»ÆŗóÖĘČ”ĮņĖį»ņÕßĮņĖįļ§£¬ĘäÖŠSO2·¢Éś“ß»ÆŃõ»ÆµÄ·“Ó¦ĪŖ£ŗ2SO2£Øg£©+O2£Øg£©?2SO3£Øg£©£®ČōŌŚT1”ę”¢0.1MPaĢõ¼žĻĀ£¬ĶłŅ»ĆܱÕČŻĘ÷ĶØČėSO2ŗĶO2£ØĘäÖŠn£ØSO2£©£ŗn£ØO2£©=2£ŗ1£©£¬²āµĆČŻĘ÷ÄŚ×ÜŃ¹ĒæÓė·“Ó¦Ź±¼äČēĶ¼ĖłŹ¾£ŗ²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | CH3COOH | B£® | 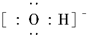 | C£® | ÉżøßĪĀ¶Č | D£® | NaOH |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com