
| A. | N2 | B. | NH3 | C. | CO2 | D. | MgCl2 |
 永乾教育寒假作业快乐假期延边人民出版社系列答案
永乾教育寒假作业快乐假期延边人民出版社系列答案科目:高中化学 来源: 题型:选择题
| A. | 苯酚在正极,发生氧化反应 | |
| B. | O2在负极,发生还原反应 | |
| C. | 反应结束后,电解液的酸度可能略有增加 | |
| D. | 正极的电极反应是C6H6O+11H2O-28e-═6CO2+28H+ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 pH=2的A、B两种酸溶液各1mL,分别加水稀释到1000mL,其溶液的pH与溶液体积(V)的关系如图所示,则下列说法正确的是( )
pH=2的A、B两种酸溶液各1mL,分别加水稀释到1000mL,其溶液的pH与溶液体积(V)的关系如图所示,则下列说法正确的是( )| A. | A、B两种酸溶液物质的量浓度一定相等 | |
| B. | 稀释后A酸溶液的酸性比B酸溶液强 | |
| C. | 稀释后的A、B溶液分别与足量NaOH溶液反应消耗碱的体积相等 | |
| D. | 若A是强酸,则B一定是弱酸,且a=5 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| X气体 | Y溶液 | 预测的现象 | 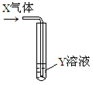 | |
| ① | CO2 | 饱和CaCl2溶液 | 白色沉淀析出 | |
| ② | SO2 | Ba(NO3)2溶液 | 白色沉淀析出 | |
| ③ | NH3 | AgNO3溶液 | 白色沉淀析出 | |
| ④ | NO2 | Na2S溶液 | 白色沉淀析出 |
| A. | 只有①②③ | B. | 只有①② | C. | 只有② | D. | ②④ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
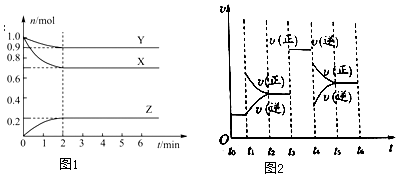
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 16gO3所含的氧原子数目为NA | |
| B. | 标准状况下,22.4L H2O所含分子数目为NA | |
| C. | 24gMg变成Mg2+时失去的电子数目为NA | |
| D. | 1 L 1mol/L的FeCl3溶液中含有Cl-的数目为NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用FeCl3溶液腐蚀铜电路板:Fe3++Cu═Fe2++Cu2+ | |
| B. | 向NH4HCO3溶液中加入足量NaOH溶液共热:NH4++OH$\frac{\underline{\;\;△\;\;}}{\;}$NH3↑+H2O | |
| C. | 向硫酸氢钠溶液中滴入氢氧化钡溶液至pH=7:Ba2++OH-+H++SO42-═BaSO4↓+H2O | |
| D. | 水电离出的c(H+)=1×10-12mol/L溶液中,可能大量共存的离子:K+、CO32-、Na+、S2- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com