
某稀硫酸和稀硝酸的混合溶液200 mL,平均分成 两份,向其中一份中逐渐加入铜粉,最多能溶解19.2 g(已知硝酸只能被还原为NO气体)。向另一份中逐渐加入铁粉,产生气体的量随铁粉质量增加的变化如图所示。下列分析或结果错误的是
A.原混合液中NO3-的物质的量为0.2mol
B.OA段产生是NO,AB段反应为2Fe3++Fe = 3Fe2+,BC段产生氢气
C.溶液中最终溶质为FeSO4
D.c(H2SO4)为5mol·L-1
科目:高中化学 来源: 题型:
向CuSO4溶液中逐滴加入KI溶液至过量,观察到产生白色沉淀CuI,蓝色溶液变为棕色。再向反应后的溶液中通入过量的SO2气体,溶液变成无色。则下列说法正确的是( )
A.通入22.4 L SO2参加反应时,有2 NA个电子发生转移
B.通入SO2后溶液逐渐变成无色,体现了SO2的漂白性
C.滴加KI溶液时,KI被氧化,CuI是氧化产物
D.上述实验条件下,物质的氧化性:Cu2+>I2>SO2
查看答案和解析>>
科目:高中化学 来源: 题型:
核电荷数为1~18的元素中,下列说法不正确的是( )
A.最外层只有1个电子的元素不一定是金属元素
B.最外层有2个电子的元素不一定是金属元素
C.原子核外各层电子数相等的元素一定是金属元素
D.最外层电子数为7的原子,最高正价为+7
查看答案和解析>>
科目:高中化学 来源: 题型:
乙烯的产量可以用来衡量一个国家的石油化工发展水平。请回答:
(1)乙烯的结构式是 。
(2)若将乙烯气体通入溴的四氯化碳溶液中,反应的化学方程式为 。
(3)可以用来除去乙烷中混有的乙烯的试剂是_________。(填序号)
①水 ②氢气 ③溴水 ④酸性高锰酸钾溶液
(4)在一定条件下,乙烯能与水反应生成有机物A,A的结构简式是 ,其反应类型是 反应(填“取代”或“加成”)。
(5)下列化学反应原理相同的是________(填序号)。
①乙烯使溴的四氯化碳溶液和酸性高锰酸钾溶液褪色
②SO2使溴水和酸性高锰酸钾溶液褪色
③SO2使品红溶液和滴有酚酞的NaOH溶液褪色
查看答案和解析>>
科目:高中化学 来源: 题型:
下列实验方案中,不能测定Na2CO3和NaHCO3混合物中Na2CO3质量分数的是
A.取a克混合物充分加热,减重b克
B.取a克混合物与足量稀盐酸充分反应,加热、蒸干、灼烧,得b克固体
C.取a克混合物与足量稀硫酸充分反应,逸出气体用碱石灰吸收,增重b克
D.取a克混合物与足量Ba(OH)2溶液充分反应,过滤、洗涤、烘干,得b克固体
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是
A.光导纤维的主要成分是硅
B. NaHCO3、Na2CO3、(NH4)2CO3三种固体受热后均能生成气体
C.Na2O2与水反应,红热的Fe与水蒸气反应均能反应生成碱
D. Na和Cs属于第IA族元素,Cs失去电子能力比Na强
查看答案和解析>>
科目:高中化学 来源: 题型:
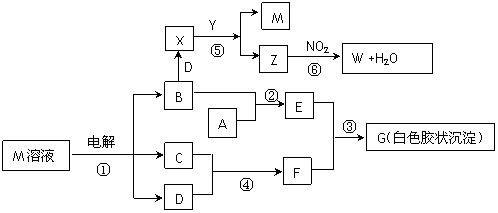 已知下图中物质M是由同一短周期的两种元素组成的离子化合物,焰色反应为黄色,阴离子元素最高正价与它的负价代数和为6。X具有漂白性,Y为碱性气体, W是对空气无污染的气体。试回答下列问题:
已知下图中物质M是由同一短周期的两种元素组成的离子化合物,焰色反应为黄色,阴离子元素最高正价与它的负价代数和为6。X具有漂白性,Y为碱性气体, W是对空气无污染的气体。试回答下列问题:
(1)写出电解M溶液①的化学方程式 。
(2)写出实验室制取Y气体的化学方程式 。
(3)若A是一种常见金属,写出反应②的化学方程式 。
(4)若A是某元素的一种常见酸性氧化物,写出反应③的离子方程式 。
(5)写出X的电子式 和Z的结构式 。
(6)写出反应⑤的化学方程式 。
(7)标准状况下反应⑥中生成11.2L W时转移的电子数 。(用NA表示阿佛加德罗常数)
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是( )
A. 1g钠投入100g水中,溶液的总质量为101g
B. 1g氧化钠投入100g水中,溶液的总质量为101g
C. 1g表面被氧化的金属钠投入100g水中,溶液的总质量为101g
D. 1g过氧化钠投入100g水中,溶液的总质量为101g
查看答案和解析>>
科目:高中化学 来源: 题型:
草酸与高锰酸钾在酸性条件下能够发生如下反应:
MnO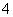 +H2C2O4+H+——Mn2++CO2↑+H2O(未配平)
+H2C2O4+H+——Mn2++CO2↑+H2O(未配平)
用4 mL 0.001 mol/L KMnO4溶液与2 mL 0.01 mol/L H2C2O4溶液,研究不同条件对化学反应速率的影响。改变的条件如下:
| 组别 | 10%硫酸体积/mL | 温度/℃ | 其他物质 |
| Ⅰ | 2 | 20 | |
| Ⅱ | 2 | 20 | 10滴饱和MnSO4溶液 |
| Ⅲ | 2 | 30 | |
| Ⅳ | 1 | 20 | a mL蒸馏水 |
(1)该反应中氧化剂和还原剂的物质的量之比为________。
(2)如果研究催化剂对化学反应速率的影响,使用实验______和_________(用Ⅰ~Ⅳ表示,下同);如果研究温度对化学反应速率的影响,使用实验______和__________。
(3)对比实验Ⅰ和Ⅳ,可以研究________________________对化学反应速率的影响,实验Ⅳ中a=________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com