
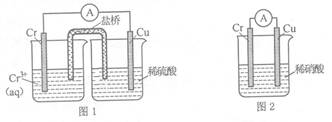
 Cr2O72—(橙色)+H2O
Cr2O72—(橙色)+H2O
 轻松课堂单元期中期末专题冲刺100分系列答案
轻松课堂单元期中期末专题冲刺100分系列答案科目:高中化学 来源:不详 题型:单选题
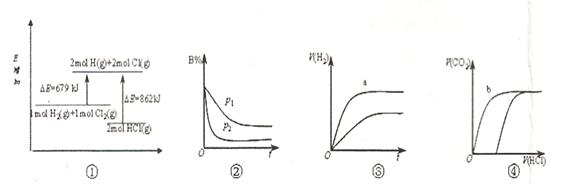
| A.①表示化学反应H2(g)+Cl2(g)=2HCl(g)的能量变化,则该反应的反应热△H=183kJ/mol |
B.②表示其它条件不变时,反应4A(g)+3B(g) 2C(g)+6D在不同压强下B%(B的体积百分含量)随时间的变化,则D一定是气体 2C(g)+6D在不同压强下B%(B的体积百分含量)随时间的变化,则D一定是气体 |
| C.③表示体积和pH均相同的HCl和CH3COOH两种溶液中,分别加入足量的锌,产生H2的体积随时间的变化,则a表示CH3COOH溶液 |
| D.④表示10mL 0.1mol/L Na2CO3和NaHCO3两种溶液中,分别滴加0.lmol/LHCl,产生CO2的体积随盐酸体积的变化,则b表示Na2CO3溶液 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
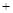 CO(g)
CO(g) CH3OH(g)
CH3OH(g)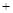 90.8 kJ
90.8 kJ CH3OCH3(g)
CH3OCH3(g)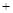 H2O(g)
H2O(g)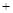 23.5 kJ
23.5 kJ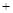 H2O(g)
H2O(g) CO2(g)
CO2(g)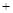 H2(g)
H2(g)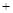 41.3 kJ
41.3 kJ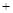 3CO(g)
3CO(g) CH3OCH3(g)
CH3OCH3(g)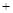 CO2(g)
CO2(g)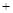 Q,其中Q
Q,其中Q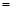 kJ;
kJ; CH3OCH3(g)
CH3OCH3(g)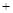 H2O(g)在一密闭容器中进行到10min时恰好达平衡,测得各组分的浓度如下:
H2O(g)在一密闭容器中进行到10min时恰好达平衡,测得各组分的浓度如下:| 物质 | CH3OH | CH3OCH3 | H2O |
浓度/(mol·L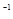 ) ) | 0.44 | 0.6 | 0.6 |
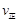 (甲醇)
(甲醇) 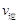 (水)(填“>”、“<”或“=”)。
(水)(填“>”、“<”或“=”)。 (CH3OH)
(CH3OH)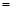 ;
;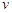 (CH3OH)
(CH3OH)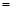 ;
;查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
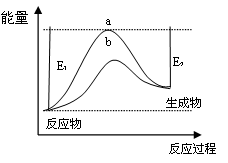
 2NH3(g) ΔH <0。400℃时,K= 0.5,某一时刻测得N2、H2和NH3三种物质物质的量分别为2mol、1mol和3mol,则该反应的v正(N2) v逆(N2)(填 “>” 、“="”" 或 “<”)
2NH3(g) ΔH <0。400℃时,K= 0.5,某一时刻测得N2、H2和NH3三种物质物质的量分别为2mol、1mol和3mol,则该反应的v正(N2) v逆(N2)(填 “>” 、“="”" 或 “<”) 浓度mol.L-1 浓度mol.L-1时间 | c(NH3) | c(O2) | c(NO) |
| 0min | 1.000 | 1.600 | 0.000 |
| 2min | 0.600 | a | 0.400 |
| 4min | 0.500 | 0.975 | 0.500 |
| 6min | 0.500 | 0.975 | 0.500 |
| 8min | 0.700 | 1.225 | 0.750 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 Fe(s)+CO2(g) ΔH>0,已知在1100℃时,该反应的化学平衡常数K=0.263。
Fe(s)+CO2(g) ΔH>0,已知在1100℃时,该反应的化学平衡常数K=0.263。
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
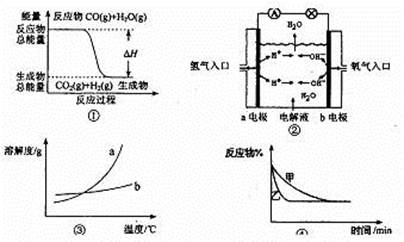
| A.图①表示化学反应中能量的变化,反应CO(g)+H2O(g)=CO2(g)+H2(g)的△H大于0 |
| B.图②为氢氧燃料电池示意图,正、负极通入气体体积之比为2:1 |
| C.图③表示物质a、b的溶解度曲线,可以用结晶方法从a、b混合物中提纯a |
D.图④表示压强对可逆反应2A(g)+2B(g)  3C(g)+D(s)的影响,乙的压强大 3C(g)+D(s)的影响,乙的压强大 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.加入醋酸钠 | B.加入ZnCl2 | C.加入铜粉 | D.加入硫酸铜溶液 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.阳极放出大量氯气 |
| B.阴极放出大量氢气 |
| C.电解液逐渐变为黄色 |
| D.电解液逐渐变为绿色 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.HCO3— → CO2 | B.S2— → K2S |
| C.Fe3+→ Fe2+ | D.MnO42—-→MnO4— |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com