
A.Cu(NO3)2=Cu2++N
| B.NaHCO3=Na++H++C
| ||||
C.Ca(OH)2=Ca2++(OH
| D.HCl=H++Cl- |
 名师指导期末冲刺卷系列答案
名师指导期末冲刺卷系列答案 开心蛙口算题卡系列答案
开心蛙口算题卡系列答案科目:高中化学 来源:不详 题型:单选题
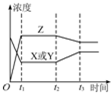
| A.增大X或Y的浓度 | B.增大压强 |
| C.降低温度 | D.升高温度 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.温度150℃、压强5.05×104Pa |
| B.温度150℃、压强4.04×105Pa |
| C.温度25℃、压强1.01×105Pa |
| D.温度0℃、压强5.05×104Pa |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.KClO3→K++Cl-+3O2- |
| B.NaHCO3→Na++H++CO32- |
| C.HS-+H2O?H3O++S2- |
| D.CH3COONH4?NH4++CH3COO- |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题

查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.①②③④ | B.②③④ | C.③④ | D.②④ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.相同条件下,pH相同的NaClO和Na2CO3溶液,物质的量浓度前者小于后者 |
| B.常温下,将CH3COONa溶液和稀盐酸混合至溶液pH=7时: c(Na+)>c(CH3COO-)>c(Cl-) >c(CH3COOH)>c(H+)=c(OH-) |
| C.向饱和Na2CO3溶液中通入足量的CO2,溶液变浑浊,由此证明了NaHCO3溶解度比Na2CO3小 |
| D.氯碱工业使用的食盐水需先除去其中的Ca2+、Mg2+、SO42-等杂质。除杂时,粗盐水中可先加入过量的BaCl2溶液,至沉淀不再产生后,再加入过量的Na2CO3和NaOH,充分反应后滤去沉淀,所得滤液中仍含有一定量的SO42- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com