
下列说法在一定条件下可以实现的是
①非金属置换金属的反应
②弱酸反应可以生成强酸
③有单质参加的非氧化还原反应
④没有水生成,也没有沉淀和气体生成的复分解反应
A.②④ B.①③④ C.①②③ D.①②③④
D
【解析】
试题分析:①非金属可以置换金属,如氢气和氧化铜在加热的条件下反应生成铜和水,H2+CuO Cu+H2O,故①正确;②弱酸反应可以生成强酸,如H2S+CuSO4═CuS↓+H2SO4,H2S是弱酸,而生成H2SO4是强酸,能发生的原因是生成的CuS沉淀难溶于H2SO4,故②正确;③有单质参加的非氧化还原反应,红磷和白磷是两种物质,当红磷转化成白磷时发生了化学反应,但单质转化成单质化合价没有发生改变,是非氧化还原反应,故③正确;④没有水生成,也没有沉淀和气体生成的复分解反应,如 Fe3++3SCN-?Fe(SCN)3)硫氰化铁为血红色物质,既不是沉淀也不是气体,故④正确,所以答案为D。
Cu+H2O,故①正确;②弱酸反应可以生成强酸,如H2S+CuSO4═CuS↓+H2SO4,H2S是弱酸,而生成H2SO4是强酸,能发生的原因是生成的CuS沉淀难溶于H2SO4,故②正确;③有单质参加的非氧化还原反应,红磷和白磷是两种物质,当红磷转化成白磷时发生了化学反应,但单质转化成单质化合价没有发生改变,是非氧化还原反应,故③正确;④没有水生成,也没有沉淀和气体生成的复分解反应,如 Fe3++3SCN-?Fe(SCN)3)硫氰化铁为血红色物质,既不是沉淀也不是气体,故④正确,所以答案为D。
考点:本题考查化学反应规律。


科目:高中化学 来源:2015届贵州省贵阳市高三年级8月摸底考试化学试卷(解析版) 题型:填空题
(9分)砷(As)广泛分布与自然界,砷与氮同主族,比氮多两个电子层。
(1)砷位于元素周期表中_____周期________族,其气态氢化物的稳定性比NH3_______(填“强”或“弱”);
(2)砷的常见酸性氧化物有As2O3和As2O5,请根据图中信息写出As2O3分解为As2O5的热化学方程式:________________________;

(3)已知:将酸滴入砷酸盐与KI混合的溶液中发生反应:AsO43-+2I―+2H+=AsO33-+I2+H2O.某研究性学习小组同学欲利用该反应原理,设计实验装置探究原电池原理,请你配合他们绘制原电池装置图,并回答下列问题:
若以石墨为电极,正极上发生的反应为______________.该电池工作时,当外电路中转移5mol电子时,则有_________molI2生成.
查看答案和解析>>
科目:高中化学 来源:2015届福建省高二上学期第二次月考化学试卷(解析版) 题型:选择题
在密闭容器中进行如下反应:X2(g)+Y2(g)  2Z(g),已知X2、Y2、Z的起始浓度分别为0.2mol/L、0.4mol/L、0.3mol/L,在一定条件下,当反应达到平衡时,各物质的浓度有可能是 ( )
2Z(g),已知X2、Y2、Z的起始浓度分别为0.2mol/L、0.4mol/L、0.3mol/L,在一定条件下,当反应达到平衡时,各物质的浓度有可能是 ( )
A.X2为0.3mol/L B.Y为0.65mol/L C.Y2为0.2mol/L D.Z为0.7mol/L
查看答案和解析>>
科目:高中化学 来源:2015届福建省高三上学期期中考试化学试卷(解析版) 题型:选择题
下列离子方程式正确的是
A、碳酸钡与足量盐酸反应:2H++BaCO3=Ba2++H2O+CO2↑
B、氯气通入蒸馏水中:Cl2+H2O=Cl﹣+ClO﹣+2H+
C、氢氧化钡溶液与稀硫酸混合:Ba2++SO42﹣+H++OH﹣=BaSO4↓+H2O
D、过量CO2通入澄清石灰水中:CO2+Ca(OH)2 =CaCO3↓+H2O
查看答案和解析>>
科目:高中化学 来源:2015届福建省高三上学期期中考试化学试卷(解析版) 题型:选择题
常温下,下列各组离子在溶液中一定能大量共存的是
A.pH=12的溶液:K+、Na+、CH3COO—、CO23—
B.0.1 mol/L的NaNO3溶液:H+、Fe2+、Cl—、SO42—
C.与铝反应产生大量氢气的溶液:Mg2+、K+、HCO3—、NO3—
D.由水电离产生的c(H+)=10-13mol/L的溶液:NH4+、Ca2+、SO32—、Cl—
查看答案和解析>>
科目:高中化学 来源:2015届福建省高三上学期第二次质量检查化学试卷(解析版) 题型:实验题
(15分)I2O5是白色固体,遇水生成碘酸(HIO3)。I2O5可用于检验并定量测定空气中的CO,在常温下发生的反应为 5CO+I2O5=5CO2+I2 (空气中其余气体不与I2O5反应)。
实验一:制取I2O5
将碘酸加热至90~110 ?C使其部分脱水,再升温至220~240 ℃并恒温4 h,使反应完全。接着慢慢冷却至室温,密封保存,即得五氧化二碘。
(1)写出碘酸制I2O5的化学方程式: 。
(2)在制得的I2O5固体中含有少量I2杂质,提纯的方法是 (填标号);
A.过滤 B.蒸发结晶 C.蒸馏 D.升华
用提纯方法用到的玻璃仪器为 (填标号)。
A.圆底烧瓶 B.烧杯 C.普通漏斗 D.酒精灯 E.玻璃棒
实验二:检验空气中CO
利用下图装置检验空气中是否存在CO。
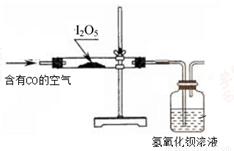
(3)能说明空气中含有CO的现象是 。
(4)倘若要从广口瓶中出现浑浊来判断空气中含有CO,请写出改进的实验方案: 。
实验三:测定空气中CO的含量
(5)将I2O5与CO反应生成的碘单质用硫代硫酸钠滴定(反应为I2+2Na2S2O3=Na2S4O6+2NaI),即可根据消耗硫代硫酸钠的量来计算空气中CO的含量。若某次实验时测得参与反应的空气体积为a mL(标准状况下),滴定过程中,共消耗v mL c mol·L-1 Na2S2O3溶液。则该空气样品中CO的体积分数是 。
(6)该实验测定出来的结果不可信,最大可能的原因是: 。
查看答案和解析>>
科目:高中化学 来源:2015届福建省高三上学期第二次质量检查化学试卷(解析版) 题型:选择题
如图所示,X、Y、Z为短周期元素,且X、Z的核外电子数之和等于Y的核外电子数,下列说法不正确的是

A.三种元素中,Z元素原子半径最小
B.X、Y 两种元素的气态氢化物能相互反应
C.Z位于元素周期表中第2周期、第ⅥA族
D.Y元素的气态氢化物与X 的最高价氧化物对应的水化物能发生氧化还原反应
查看答案和解析>>
科目:高中化学 来源:2015届福建省高三上学期期中考试化学试卷(解析版) 题型:选择题
关于pH相同的醋酸和盐酸,下列叙述不正确的是
A.取等体积的两种酸分别稀释至原溶液的m倍和n倍,结果两溶液的pH仍然相同,则m>n
B.取等体积的两种酸分别与完全一样的足量锌粒反应,开始时反应速率:盐酸大于醋酸
C.取等体积的两种酸分别中和NaOH溶液,醋酸消耗NaOH的物质的量比盐酸消耗的多
D.两种酸中c(CH3COO-)=c(Cl-)
查看答案和解析>>
科目:高中化学 来源:2015届福建省高三上学期第一次阶段考试化学试卷(解析版) 题型:选择题
下列实验现象的描述正确的是
A.氢气在氯气中燃烧,发出苍白色火焰,瓶口上方有白色烟雾
B.氧化铁溶于水生成红褐色沉淀
C.铜在氯气中燃烧,产生棕黄色烟
D.钠在空气中燃烧,发出黄色的火焰,生成白色固体
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com