
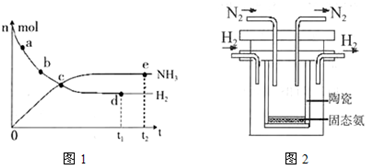
Ņ»¶ØĢõ¼žĻĀ£¬ŌŚĢå»ż¹Ģ¶ØµÄĆܱÕČŻĘ÷ÖŠ£¬ÄܱķŹ¾·“Ó¦X(g)+2Y(g)2Z(g)Ņ»¶Ø“ļµ½»ÆŃ§Ę½ŗāדĢ¬µÄŹĒ
¢ŁX”¢Y”¢ZµÄĪļÖŹµÄĮæÖ®±ČĪŖ1:2:2
¢ŚX”¢Y”¢ZµÄÅØ¶Č²»ŌŁ·¢Éś±ä»Æ
¢ŪČŻĘ÷ÖŠµÄŃ¹Ēæ²»ŌŁ·¢Éś±ä»Æ
¢Üµ„Ī»Ź±¼äÄŚÉś³Én molZ£¬Ķ¬Ź±Éś³Én molY
¢ŻČŻĘ÷ÖŠø÷ĘųĢåµÄĪļÖŹµÄĮæ²»ŌŁøıä
¢ŽČŻĘ÷ÖŠĘųĢåµÄĆÜ¶Č²»ŌŁ·¢Éś±ä»Æ
A.¢Ł¢Ś¢Ż¢Ž B.¢Ś¢Ū¢Ü¢Ž C.¢Ś¢Ū¢Ü¢Ż D. ¢Ł¢Ū¢Ü¢Ż
C
½āĪö:ŌŚŅ»¶ØĢõ¼žĻĀ£¬µ±Õż·“Ó¦ĖŁĀŹŗĶÄę·“Ó¦ĖŁĀŹĻąµČŹ±£¬ĢåĻµÖŠø÷ÖÖĪļÖŹµÄÅØ¶Č»ņŗ¬Įæ¾ł²»ŌŁ·¢Éś±ä»ÆµÄדĢ¬£¬³ĘĪŖ»ÆŃ§Ę½ŗāדĢ¬”£Ę½ŗāŹ±ø÷ÖÖĪļÖŹµÄÅØ¶Č²»ŌŁ·¢Éś±ä»Æ£¬µ«ø÷ÖÖĪļÖŹµÄÅØ¶Č²»Ņ»¶ØĻąµČ£¬¢Ł²»ÕżČ·£¬¢Ś¢ŻÕżČ·”£øĆ·“Ó¦Ē°ŗóĘųĢåĢå»żŹĒ±ä»ÆµÄ£¬ĖłŅŌŃ¹ĒæŅ²ŹĒ±ä»ÆµÄ£¬Ņņ“Ėµ±Ń¹Ēæ²»ŌŁ·¢Éś±ä»ÆŹ±£¬æÉŅŌĖµĆ÷£¬¢ŪÕżČ·”£¢ÜÖŠ·“Ó¦ĖŁĀŹµÄ·½ĻņĻą·“£¬ĒŅĀś×ćĖŁĀŹÖ®±ČŹĒĻąÓ¦µÄ»Æѧ¼ĘĮæŹżÖ®±Č£¬¼“Āś×ćÕżÄę·“Ó¦ĖŁĀŹĻąµČ£¬ÕżČ·”£»ģŗĻĘųµÄĆܶȏĒ»ģŗĻĘųµÄÖŹĮæŗĶČŻĘ÷ČŻ»żµÄ±ČÖµ£¬ŌŚ·“Ó¦¹ż³ĢÖŠ£¬ÖŹĮæŗĶČŻ»ż¾łŹĒ²»±äµÄ£¬ĖłŅŌĆܶȏ¼ÖÕŹĒ²»±äµÄ£¬¢Ž²»ÄÜĖµĆ÷”£“š°øŃ”C”£


 Š”ѧæĪŹ±ĢŲѵĻµĮŠ“š°ø
Š”ѧæĪŹ±ĢŲѵĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2004Äźøßæ¼±±¾©ĖÄÖŠČ«ÕęÄ£ÄāŹŌ¾ķ”¤»Æѧ ĢāŠĶ£ŗ021
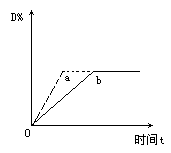
ŅŃÖŖ·“Ó¦3A(Ęų)£«B(Ęų) C(¹Ģ)£«4D(Ęų)£«Q£¬ĻĀĶ¼ÖŠa£¬b±ķŹ¾ŌŚŅ»¶ØĢõ¼žĻĀ£¬DµÄĢå»ż·ÖŹżĖꏱ¼ätµÄ±ä»ÆĒéæö£®ČōŹ¹ĒśĻßb±äĪŖĒśĻßa£¬æɲÉČ”µÄ“ėŹ©ŹĒ
C(¹Ģ)£«4D(Ęų)£«Q£¬ĻĀĶ¼ÖŠa£¬b±ķŹ¾ŌŚŅ»¶ØĢõ¼žĻĀ£¬DµÄĢå»ż·ÖŹżĖꏱ¼ätµÄ±ä»ÆĒéæö£®ČōŹ¹ĒśĻßb±äĪŖĒśĻßa£¬æɲÉČ”µÄ“ėŹ©ŹĒ
[””””]
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2013-2014ѧğ½Ī÷Ź”øÓÖŻŹŠŹ®¶žĻŲø߶žÉĻŃ§ĘŚĘŚÖŠæ¼ŹŌ»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗĢīæÕĢā
£Ø1£©ŌŚĆܱÕČŻĘ÷ÖŠ½ųŠŠĻĀĮŠ·“Ó¦£ŗM(g) + N(g) R(g) + 2L(?) £¬“Ė·“Ó¦¹ęĀÉ·ūŗĻĻĀĶ¼Ķ¼Ļń”£
R(g) + 2L(?) £¬“Ė·“Ó¦¹ęĀÉ·ūŗĻĻĀĶ¼Ķ¼Ļń”£

¢ŁT1 T2 ,Õż·“Ó¦µÄ”÷H 0”££ØĢī”°£¾”±”¢”°£¼”±»ņ”°£½”±£¬ĻĀĶ¬£©”£
¢ŚP1 P2 , LĪŖ ”££ØĢī”°¹Ģ”±»ņ”°Ņŗ”±»ņ”°Ęų”±Ģ¬£©”£
£Ø2£©ŗĻ³É°±µÄŌĄķĪŖ£ŗN2(g)+3H2(g)  2NH3(g)
2NH3(g)  H£½-92£®4 kJ£Æmol£¬øĆ·“Ó¦µÄÄÜĮæ±ä»ÆČēĶ¼ĖłŹ¾”£
H£½-92£®4 kJ£Æmol£¬øĆ·“Ó¦µÄÄÜĮæ±ä»ÆČēĶ¼ĖłŹ¾”£

¢ŁŌŚ·“Ó¦ĢåĻµÖŠ¼ÓČė“߻ƼĮ£¬·“Ó¦ĖŁĀŹŌö“ó£¬E2µÄ±ä»ÆŹĒ (Ģī”°Ōö“ó”±”¢”°¼õŠ””±»ņ”°²»±ä”±)”£¢ŚČōŌŚŅ»ĆܱÕČŻĘ÷ÖŠ¼ÓČė1molN2ŗĶ3molH2£¬ŌŚŅ»¶ØĢõ¼žĻĀ³ä·Ö·“Ó¦£¬·Å³öµÄČČĮæ 92.4kJ.£ØĢī”°£¾”±”¢”°£¼”±»ņ”°£½”±£©”£
¢Ū½«1 mol N2ŗĶ3 mol H2³äČėĢå»ż²»±äµÄĆܱÕČŻĘ÷ÖŠ£¬ŌŚŅ»¶ØĢõ¼žĻĀ“ļµ½Ę½ŗā£¬“ĖŹ±ÓūĢįøßøĆČŻĘ÷ÖŠH2µÄ×Ŗ»ÆĀŹ£¬ĻĀĮŠ“ėŹ©æÉŠŠµÄŹĒ (Ģī×ÖÄø)”£
A£®ĻņČŻĘ÷ÖŠ°“Ō±ČĄżŌŁ³äČėŌĮĻĘų B£®ĻņČŻĘ÷ÖŠŌŁ³äČėŅ»¶ØĮæH2
C£®øı䷓ӦµÄ“߻ƼĮ D£®Ņŗ»ÆÉś³ÉĪļ·ÖĄė³ö°±
¢ÜČōŌŚĆܱÕČŻĘ÷ÖŠ³äČė2molN2ŗĶ6molH2·“Ó¦“ļĘ½ŗāŹ±N2µÄ×Ŗ»ÆĀŹĪŖ40%”£ČōŅŌNH3×÷ĪŖĘšŹ¼·“Ó¦Īļ£¬·“Ó¦Ģõ¼žÓėÉĻŹö·“Ó¦ĻąĶ¬Ź±£¬ŅŖŹ¹Ęä·“Ó¦“ļµ½Ę½ŗāŹ±ø÷×é·ÖµÄĪļÖŹµÄĮæ·ÖŹżÓėĒ°ÕßĻąĶ¬£¬ŌņNH3µÄĘšŹ¼ĪļÖŹµÄĮæŗĶĖüµÄ×Ŗ»ÆĀŹ·Ö±šĪŖ mol”¢ ”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2012ÄźĖÕ½Ģ°ęøßÖŠ»Æѧ±ŲŠŽ2 2.1»Æѧ·“Ó¦ĖŁĀŹÓė·“Ó¦ĻŽ¶ČĮ·Ļ°¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
Ņ»¶ØµÄ¹ĢĢåĻõĖįŅųÖĆÓŚŅ»ČŻ»ż²»±äµÄ2LĆܱÕČŻĘ÷ÖŠ£¬ŌŚŅ»¶ØĢõ¼žĻĀ·¢ÉśČēĻĀ·“Ó¦£ŗ2AgNO3(¹Ģ) 2Ag(¹Ģ)+2NO2(Ęų)+O2(Ęų)£¬2NO2(Ęų)
2Ag(¹Ģ)+2NO2(Ęų)+O2(Ęų)£¬2NO2(Ęų) 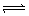 N2O4(Ęų)£¬2minÄ©£¬²āµĆ¹ĢĢå¼õÖŲ6.2g,ĒŅC(NO2)=0.04mol/L£¬ŌņĻĀĮŠĖµ·ØÕżČ·µÄŹĒ
( )
N2O4(Ęų)£¬2minÄ©£¬²āµĆ¹ĢĢå¼õÖŲ6.2g,ĒŅC(NO2)=0.04mol/L£¬ŌņĻĀĮŠĖµ·ØÕżČ·µÄŹĒ
( )
A£®2minŗóČŻĘ÷ÄŚC(N2O4)=0.04mol/L B£®2minÄŚV(O2)= 0.0125mol/(L”¤min)
C£®»ģŗĻĘųĢåµÄĘ½¾łĆܶČĪŖ3.1g/L D£®»ģŗĻĘųĢåÖŠNO2µÄĢå»ż·ÖŹżĪŖ11%
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗĶ¬²½Ģā ĢāŠĶ£ŗ²»¶ØĻīŃ”ŌńĢā
 2Ag(¹Ģ)+2NO2(Ęų)+O2(Ęų)£¬2NO2(Ęų)
2Ag(¹Ģ)+2NO2(Ęų)+O2(Ęų)£¬2NO2(Ęų) N2O4(Ęų)£¬2minÄ©£¬²āµĆ¹ĢĢå¼õÖŲ6£®2g£¬ĒŅC(NO2)=0£®04mol/L£¬ŌņĻĀĮŠĖµ·ØÕżČ·µÄŹĒ
N2O4(Ęų)£¬2minÄ©£¬²āµĆ¹ĢĢå¼õÖŲ6£®2g£¬ĒŅC(NO2)=0£®04mol/L£¬ŌņĻĀĮŠĖµ·ØÕżČ·µÄŹĒ ²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com