
| A. | 得电子能力:A>B>Cm+>Dn+ | B. | 还原性:An->Bm->C>D | ||
| C. | 原子半径:D>C>B>A | D. | 离子半径:An->Bm->Cm+>Dn+ |
分析 aAn-、bBm-、cCm+、dDn+具有相同的电子层结构,a、b、c、d不相等且n>m,属于四种不同元素的离子,且a+n=b+m=c-m=d-n,故原子序数大小顺序是d>c>b>a,结合离子所得电荷可知,A、B为非金属元素,非金属性:B>A,C、D为金属元素,金属性:C>D,且C、D位于A和B的下一周期,电子层结构相同,核电荷数越大离子半径越小,据此分析.
解答 解:aAn-、bBm-、cCm+、dDn+具有相同的电子层结构,a、b、c、d不相等且n>m,属于四种不同元素的离子,且a+n=b+m=c-m=d-n,故原子序数大小顺序是d>c>b>a,结合离子所得电荷可知,A、B为非金属元素,非金属性:B>A,C、D为金属元素,金属性:C>D,且C、D位于A和B的下一周期.
A.同周期元素的原子序数越大,非金属性越强,得电子能力越强,则得电子能力:B>A,故A错误;
B.非金属性越强,阴离子的还原性越弱,金属性越强,还原性越强,一般金属的还原性大于非金属阴离子,则还原性:C>D>An->Bm-,故B错误;
C.电子层越多,原子半径越大,电子层相同,原子序数越大,半径越小,则原子半径:C>D>A>B,故C错误;
D.核电荷数a>b>d>c,电子层结构相同,核电荷数越大离子半径越小,故离子半径:An->Bm->Cm+>Dn+,故D正确,
故选D.
点评 本题考查原子结构与元素周期律,确定元素在周期表中的相对位置是关键,注意理解掌握微粒半径的比较规律,难度中等,侧重于考查学生对基础知识的应用能力.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:解答题
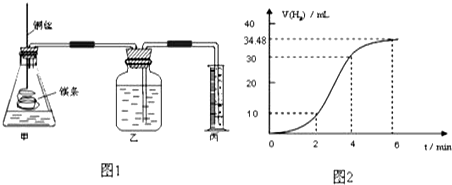
| 实验编号 | Ⅰ | Ⅱ | Ⅲ | Ⅳ |
| 10%H2O2的体积/mL | 5.0 | 5.0 | V1 | V2 |
| 20%硫酸的体积/mL | 0 | 0.5 | 1.0 | V3 |
| 水的体积/mL | 15 | 14.5 | V4 | 13.5 |
| 所需时间t/s | t1 | t2 | t3 | t4 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 含有少量硫的酒精溶液,加入大量水后形成乳白色液体,用滤纸过滤不能分离出硫 | |
| B. | 原硅酸溶液中加入硫酸铵饱和溶液,结果产生沉淀 | |
| C. | 硫酸铜溶液中加入硫化钠溶液产生黑色沉淀 | |
| D. | 用水稀释牛奶,用一束强光照射,从侧面观察,可以看到一条清晰的光路 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 振荡混合物,用分液漏斗分离 | |
| B. | 加入NaOH溶液后振荡,用分液漏斗分离;取下层液体通入CO2,待分层后分液 | |
| C. | 加水振荡后用分液漏斗分离 | |
| D. | 加稀盐酸振荡后,用分液漏斗分离 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
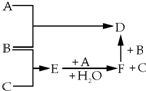 有A、B、C三种常见单质,其有关反应如图所示:已知B、E的水溶液显酸性,E在一定条件下有还原性,但不能被浓H2SO4氧化,B显黄绿色,D遇KSCN溶液显血 红色.
有A、B、C三种常见单质,其有关反应如图所示:已知B、E的水溶液显酸性,E在一定条件下有还原性,但不能被浓H2SO4氧化,B显黄绿色,D遇KSCN溶液显血 红色.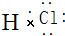 ;
;查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 第一组 | A-268.8 | B-249.5 | C-185.8 | D-151.7 |
| 第二组 | F2-187.0 | Cl2-33.6 | Br2 58.7 | I2 184.0 |
| 第三组 | HF 19.4 | HCl-84.0 | HBr-67.0 | HI-35.3 |
| 第四组 | H2O 100.0 | H2S-60.2 | H2Se 42.0 | H2Te-1.8 |
| A. | 第一组和第二组物质中一定含有共价键 | |
| B. | 第三组与第四组相比较,化合物的稳定顺序为:HBr>H2Se | |
| C. | 第三组物质溶于水后,溶液的酸性:HF>HCl>HBr>HI | |
| D. | 第四组物质中H2O的沸点最高,是因为H2O分子中化学键键能最强 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
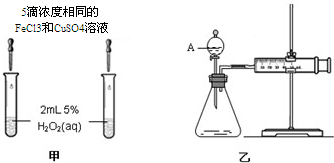
| 编号 | 操 作 | 实验现象 |
| ① | 分别在试管A、B中加入 5mL 5% H2O2溶液,各滴入1~2 滴1mol/L FeCl3溶液.待试管中均有适量气泡出现时,将试管A放入盛有5℃左右冷水的烧杯中;将试管B放入盛有40℃左右热水的烧杯中. | 试管A中不再产生气泡;试管B中产生的气泡量增大 |
| ② | 另取两支试管分别加入 5mL 5%H2O2溶液和 5mL10%H2O2溶液. | 试管A、B中均未明显见到有气泡产生 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ⅦA元素的氢化物中氟化氢的沸点最高 | |
| B. | 第三周期元素形成的简单离子的半径随原子序数的增大依次增大 | |
| C. | I2易溶于CCl4可以用相似相溶原理解释 | |
| D. | CH2=CH2分子中共有5个σ键和1个π键 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com