
 “×ĖįČÜŅŗ¼ÓĖ®Ļ”ŹĶ£¬ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ£Ø£©
“×ĖįČÜŅŗ¼ÓĖ®Ļ”ŹĶ£¬ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ£Ø£©| A£®ČÜŅŗÖŠc(H+)ŗĶc(OH-)¶¼¼õŠ” | B£®ČÜŅŗÖŠc£ØH+£©Ōö“ó |
| C£®“×ĖįµēĄėĘ½ŗāĻņ×óŅĘ¶Æ | D£®ČÜŅŗµÄpHŌö“ó |
 ÖĒ»ŪŠ”ø“Ļ°ĻµĮŠ“š°ø
ÖĒ»ŪŠ”ø“Ļ°ĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā
| A£®·“Ó¦¹ż³ĢÖŠ£¬CH3COOHµÄµēĄė³Ģ¶ČŌö“ó |
| B£®Čōa+b=14£¬Ōņ»ģŗĻŗópH=7 |
| C£®Čō»ģŗĻŗópH=5.3£¬Ōņc(Na+)< c( CH3COO£) |
| D£®Čō»ģŗĻŗóCH3COOHÓėNaOHĒ”ŗĆĶźČ«·“Ó¦£¬Ōņ»ģŗĻĒ°a+b<14 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗĢīæÕĢā
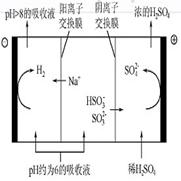
| n(SO32-)£ŗn(HSO3-) | 91£ŗ9 | 1£ŗ1 | 1£ŗ91 |
| pH | £ø.£² | 7.2 | 6.2 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā
| A£®ŹŅĪĀĻĀ£¬pH=3µÄĒā·śĖį¼ÓĖ®Ļ”ŹĶŗ󣬵ēĄė³£ŹżKa(HF)ŗĶpH¾ł¼õŠ” |
| B£®ŹŅĪĀĻĀ£¬½«Ļ”°±Ė®ÖšµĪ¼ÓČėĻ”ĮņĖįÖŠ£¬µ±ČÜŅŗpH=7Ź±£¬c(SO42£)£¾c(NH4£«) |
C£®Ļņ0.1mol/LµÄ°±Ė®ÖŠ¼ÓČėÉŁĮæĮņĖįļ§¹ĢĢ壬ŌņČÜŅŗÖŠ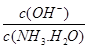 Ōö“ó Ōö“ó |
| D£®ŹŅĪĀĻĀ£¬pH=11µÄNaOHČÜŅŗÓėpH=3µÄ“×ĖįČÜŅŗµČĢå»ż»ģŗĻ£¬µĪČėŹÆČļŹŌŅŗ³ŹŗģÉ« |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗĢīæÕĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗŹµŃéĢā

²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā
| A£®Ķ¬pHĶ¬Ģå»żµÄ°±Ė®ŗĶNaOHČÜŅŗ£¬ÄÜ·Ö±šÓėĶ¬ÅضČĶ¬Ģå»żµÄŃĪĖįĒ”ŗĆĶźČ«ÖŠŗĶ |
| B£®¼ÓĖ®Ļ”ŹĶ0.10 mol?L£1µÄ°±Ė®£¬ČÜŅŗÖŠn£ØOH££©¼õŠ” |
| C£®ČōĪĀ¶Č²»±ä£¬ŌŚ°±Ė®ÖŠ¼ÓČėÉŁĮæNH4Cl¹ĢĢ壬°±Ė®µÄµēĄė¶ČŗĶµēĄėĘ½ŗā³£Źż¾ł±äŠ” |
| D£®°±Ė®ÖŠµÄĄė×ÓÅØ¶Č¹ŲĻµĀś×ć£ŗ£ŪOH££Ż£½£ŪH£«£Ż£«£ŪNH4£«£Ż |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā
| A£®øĆČÜŅŗµÄpH=4 |
| B£®ÉżøßĪĀ¶Č£¬ČÜŅŗµÄpHŌö“ó |
| C£®“ĖĖįµÄµēĄėĘ½ŗā³£ŹżŌ¼ĪŖ1”Į10-7 |
| D£®ÓÉHAµēĄė³öµÄc(H+)Ō¼ĪŖĖ®µēĄė³öµÄc(H+)µÄ106±¶ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā
| A£®¢Ł¢Ś¢Ū¢Ü | B£®¢Ś¢Ū¢Ü | C£®¢Ū¢Ü | D£®¢Ū¢Ü¢Ż |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com