
| A. | Mg(OH)2不溶于水,但能溶于浓NH4Cl溶液中 | |
| B. | 水垢中含有的CaSO4,先用Na2CO3溶液处理,使之转化为疏松、易溶于酸的CaCO3,再用酸除去 | |
| C. | 洗涤BaSO4沉淀时,用稀硫酸洗涤BaSO4沉淀比用蒸馏水洗涤损失少 | |
| D. | FeCl3溶液中混有FeCl2,常加入少量的H2O2,使Fe2+氧化为Fe3+ |
分析 平衡移动原理为:如果改变影响平衡的一个条件(如浓度、压强或温度等),平衡就向能够减弱这种改变的方向移动;
平衡移动原理适用的对象应存在可逆过程,如与可逆过程无关,则不能用平衡移动原理解释,平衡移动原理对所有的动态平衡都适用,据此进行判断.
解答 解:A.氢氧化镁存在溶解平衡,加入氯化铵后铵根离子结合氢氧根离子,促进了氢氧化镁的溶解,可用平衡移动原理解释,故A错误;
B.硫酸钙在溶液中存在溶解平衡,且硫酸钙的溶解度小于碳酸钙,加入碳酸钠溶液后钙离子与碳酸根离子结合生成更难溶的碳酸钙,最终将硫酸钙转化成碳酸钙,可用用平衡移动原理解释,故B错误;
C.硫酸钡在溶液中存在溶解平衡,硫酸根离子抑制了硫酸钡的溶解,所以用稀硫酸洗涤BaSO4沉淀比用蒸馏水洗涤损失少,可用平衡移动原理解释,故C错误;
D.FeCl3溶液中混有FeCl2,常加入少量的H2O2,使Fe2+氧化为Fe3+,利用的是双氧水的氧化性,与平衡移动原理无关,故D正确;
故选D.
点评 本题考查了化学平衡移动原理的应用,题目难度不大,明确平衡移动原理的内容为解答关键,注意明确使用平衡移动原理的前提必须是可逆过程,且与平衡移动有关.


科目:高中化学 来源: 题型:解答题
| 离子 | K+ | Na+ | NH4+ | SO42- | NO3- | Cl- |
| 浓度/mol.L-1 | 4×10-5 | 6×10-5 | 2×10-4 | 4×10-4 | 3×10-4 | 2×10-4 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 都具有强氧化性 | |
| B. | 分别露置在空气中,容器内溶质的物质的量浓度都降低 | |
| C. | 常温下都可以储存于铝制槽罐中 | |
| D. | 和碳反应中都表现出强氧化性和强酸性 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 溶液中水的离子积常数(KW)随溶液浓度的改变而改变 | |
| B. | 一般情况下,一元弱酸HA的Ka越大,表明该酸的酸性越弱 | |
| C. | 对已达到化学平衡的反应,改变压强,平衡常数(K)一定改变 | |
| D. | Ksp只与难溶电解质的性质和温度有关,而与溶液中的离子浓度无关 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 溶液中存在6种微粒 | |
| B. | c(Na+)=c(HClO)+2c(ClO-) | |
| C. | c(Na+)=c(Cl-)+c(ClO-)+c(OH-) | |
| D. | 往所得中性溶液中加入NaHCO3能放出大量气体 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 按系统命名法的名称为2-甲基-3,5-二乙基乙烷 | |
| B. | 用Na2CO3溶液能区分CH3COOH、CH3CH2OH,苯、硝基苯四种物质 | |
| C. | 等质量的甲烷、乙烯、1,3-丁二烯分别充分燃烧,所耗氧气的量依次增加 | |
| D. | 下列物质的沸点按由低到高顺序为:CH3(CH2)2CH3<(CH3)3CH<CH3(CH2)3CH3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | K+、Ca2+、Cl-、CO32- | B. | Fe2+、Al3+、NO3-、SO42- | ||
| C. | Mg2+、NH4+、CO32-、H+ | D. | Na+、Br-、ClO-、H+ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
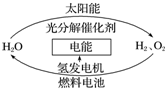 为消除目前燃料燃烧时产生的环境污染,同时缓解能源危机,有关专家提出了利用太阳能制取氢能的构想如图所示.下列说法正确的是( )
为消除目前燃料燃烧时产生的环境污染,同时缓解能源危机,有关专家提出了利用太阳能制取氢能的构想如图所示.下列说法正确的是( )| A. | 氢能源已被普遍使用 | |
| B. | H2O的分解反应是吸热反应 | |
| C. | 氢气不易贮存和运输,无开发利用价值 | |
| D. | 2 mol 液态H2O具有的总能量高于2 mol H2和1 mol O2的能量 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com