
下列有关有机化合物的认识不正确的是( )
A.油脂在空气中完全燃烧转化为水和二氧化碳
B.蔗糖、麦芽糖的分子式都是C12H22O11,二者互为同分异构体
C.在水溶液里,乙酸分子中的—CH3可以电离出H+
D.在浓硫酸存在下,苯与浓硝酸共热生成硝基苯的反应属于取代反应
 阶梯计算系列答案
阶梯计算系列答案科目:高中化学 来源: 题型:
某校化学兴趣小组探究SO2与FeCl3溶液的反应,所用装置如下图所示。
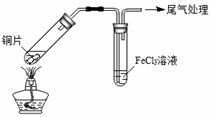
A B
(1)该小组同学预测SO2与FeCl3溶液反应的现象为溶液由棕黄色变成浅绿色,然后开始实验。
| 步骤① | 配制1 mol·L-1 FeCl3溶液(未用盐酸酸化),测其pH约为1,取少量装入试管B中,加热A。 |
FeCl3溶液显酸性的原因是 。写出装置A中产生SO2的化学方程式: 。
(2)当SO2通入到FeCl3溶液至饱和时,同学们观察到的现象是溶液由棕黄色变成红棕色,没有观察到丁达尔现象。将混合液放置12小时,溶液才变成浅绿色。
【查阅资料】 Fe(HSO3)2+离子为红棕色,它可以将Fe3+还原为Fe2+。生成Fe(HSO3)2+离子的反应为可逆反应。
解释SO2与FeCl3溶液反应生成红棕色Fe(HSO3)2+离子的原因: 。
写出溶液中Fe(HSO3)2+离子与Fe3+反应的离子方程式: 。
(3)为了探究如何缩短红棕色变为浅绿色的时间,该小组同学进行了步骤③的实验。
| 步骤② | 往5 mL 1 mol·L-1 FeCl3溶液中通入SO2气体,溶液立即变为红棕色。微热3 min,溶液颜色变为浅绿色。 |
| 步骤③ | 往5 mL重新配制的1 mol·L-1 FeCl3溶液(用浓盐酸酸化)中通入SO2气体,溶液立即变为红棕色。几分钟后,发现溶液颜色变成浅绿色。 |
用铁氰化钾溶液检验步骤②和步骤③所得溶液中的Fe2+,其现象为 。
(4)综合上述实验探究过程,可以获得的实验结论:
I.SO2与FeCl3溶液反应生成红棕色中间产物Fe(HSO3)2+离子;
II.红棕色中间产物转变成浅绿色溶液是一个较慢的过程;
III. 。
查看答案和解析>>
科目:高中化学 来源: 题型:
有物质的量浓度均为0.1 mol·L-1 的① Na2CO3溶液 ② CH3COONa溶液 ③ NaOH溶液各25 mL,,下列说法正确的是 ( )
A.3种溶液pH的大小顺序是 ③>②>①
B.若将3种溶液稀释相同倍数,pH变化最大的是②
C.若分别加入25 mL 0.1 mol·L-1盐酸后,pH最大的是①
D.若升高温度,则②的pH减小
查看答案和解析>>
科目:高中化学 来源: 题型:
通过血液中的钙离子的检测能够帮助判断多种疾病。某研究小组为测定血液样品中Ca2+的含量(100 mL血液中含Ca2+的质量),实验步骤如下:
①准确量取5.00 mL血液样品,处理后配制成50.00 mL溶液;
②准确量取溶液10.00 mL,加入过量(NH4)2C2O4溶液,使Ca2+完全转化成CaC2O4沉淀;
③过滤并洗净所得CaC2O4沉淀,用过量稀硫酸溶解,生成H2C2O4和CaSO4稀溶液;
④加入12.00 mL 0.0010 mol·L-1的KMnO4溶液,使H2C2O4完全被氧化,离子方程式为:
2MnO4- +5H2C2O4+6H+=10CO2↑+2Mn2++8H2O;
⑤用0.0020 mol·L-1 (NH4)2Fe(SO4)2溶液滴定过量的KMnO4溶液,消耗(NH4)2Fe(SO4)2溶液20.00 mL。
(1)已知室温下CaC2O4的Ksp=2.0×10-9,欲使步骤②中
c(Ca2+)≤1.0×10-5 mol·L-1,应保持溶液中c(C2O42 -)≥ mol·L-1。
(2)步骤⑤中有Mn2+生成,发生反应的离子方程式为 。
(3)若步骤⑤滴定管在使用前未用标准(NH4)2Fe(SO4)2溶液洗涤,测得血液中Ca2+的含量将 (填“偏高”、“偏低”或“不变”)。
(4)计算血样中Ca2+的含量 g/mL(写出计算过程)。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是( )
A.所有有机物都只含C、H、O、N四种元素
B.油脂水解可得到氨基酸和甘油
C.所有烷烃和蛋白质中都存在碳碳单键
D.淀粉和纤维素水解的最终产物都是葡萄糖
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)化学反应经常伴随着颜色变化,下列关于颜色的叙述正确的是________。
①鸡蛋白溶液遇浓硝酸——黄色
②淀粉碘化钾溶液遇碘离子——蓝色
③热的氧化铜遇乙醇——红色
④过氧化钠在空气中久置——淡黄色
(2)有人设计了一套实验室蒸馏石油的五个步骤,请将正确顺序的序号填入括号内。
( )将蒸馏烧瓶固定在铁架台上,在蒸馏烧瓶上塞好带温度计的橡皮塞。
( )连接好冷凝管。把冷凝管固定在铁架台上,将冷凝管下端的橡皮管和自来水龙头连接,将上端的橡皮管放在水槽内。
( )把酒精灯放在铁架台上,根据酒精灯高度确定铁圈的高度,固定铁圈,放好石棉网。
( )向蒸馏烧瓶中放入几片碎瓷片,再用漏斗向烧瓶内加原油,塞好带温度计的橡皮塞,把接收器连接在冷凝器的末端并伸入接收装置(如锥形瓶中)。
( )检查气密性(利用对固定装置微热的方法检查)。
在上述实验中温度计水银球的位置在________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关说法中,正确的是( )
A.硅单质既不能与酸反应又不能与碱反应
B.硅在自然界中以化合态存在
C.硅与NaOH溶液的反应中,硅做氧化剂
D.硅元素在地壳中的含量居第一位
查看答案和解析>>
科目:高中化学 来源: 题型:
由阿伏加德罗常数和一个水分子的质量、一个水分子的体积,不能确定的物理量有( )
A.1摩尔水的质量 B.1摩尔水蒸气的质量
C.1摩尔水的体积 D.1摩尔水蒸气的体积
查看答案和解析>>
科目:高中化学 来源: 题型:
下列反应的离子方程式书写中,正确的是 ( )
A.向Fe2(SO4)3溶液中加入少量铁粉:Fe3++Fe===2Fe2+
B.向稀硫酸中滴入少量Na2CO3溶液:2H++CO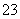 ===CO2↑+H2O
===CO2↑+H2O
C.铜放入氯化铁溶液中: Fe3++Cu===Fe+Cu2+
D.氯化铁溶液与氨水反应:Fe3++3OH-===Fe(OH)3↓
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com