
下列说法正确的是( )
A.强电解质溶液一定比弱电解质溶液的导电性强
B.强电解质的水溶液中不存在电解质分子
C.强电解质都是离子化合物,弱电解质都是共价化合物
D.不同的弱电解质只要物质的量浓度相同,电离程度也就相同
 新课标同步训练系列答案
新课标同步训练系列答案 一线名师口算应用题天天练一本全系列答案
一线名师口算应用题天天练一本全系列答案科目:高中化学 来源: 题型:
矿石中金的含量很低,金的性质又相当稳定,只能用湿法冶金——氰化法提炼,即采用稀的NaCN溶液处理已粉碎的矿石,把少量的金浸入溶液中,然后用金属锌作还原剂将金从溶液中置换析出。其反应原理为
①4Au+8NaCN+O2+2H2O 4Na[Au(CN)2]+4NaOH;
4Na[Au(CN)2]+4NaOH;
②2Na[Au(CN)2]+Zn 2Au+Na2[Zn(CN)4]。
2Au+Na2[Zn(CN)4]。
以下有关氰化法提炼金的说法中正确的是( )
A.Na[Au(CN)2]不溶于水
B.化合物Na[Au(CN) 2]中金元素的化合价为+1
C.金元素在地壳中能以化合态的形式存在
D.在提炼过程中含金元素的物质始终作氧化剂
查看答案和解析>>
科目:高中化学 来源: 题型:
请按要求写出下列化学方程式
①乙烯使硫酸酸化的高锰酸钾溶液褪色(乙烯被氧化为二氧化碳,高锰酸钾被还原为硫酸锰MnSO4)。
②甲苯在浓硫酸作催化剂的条件下与浓硝酸反应生成三硝基甲苯。
③乙醇使硫酸酸化的重铬酸钾溶液变色(乙醇被氧化为乙酸,重铬酸钾被还原为硫酸铬)。
④乙烯与氧气在银作催化剂的条件下反应生成环氧乙烷,且该反应的原子利用率为?
⑤对苯甲二甲酸与乙二醇缩聚反应生成聚酯纤维(涤纶)。
查看答案和解析>>
科目:高中化学 来源: 题型:
已知还原性A-<B-<C-,则下列反应能够进行的是
①A2+2B-=B2+2A- ②B2+2A-=A2+2B- ③B2+2C-=C2+2B- ④C2+2A-=A2+2C-
A.①③ B.②③ C.①④ D.③④
查看答案和解析>>
科目:高中化学 来源: 题型:
用18.0mol·L-1的浓H2SO4配制250mL 0.9mol·L-1的稀H2SO4,请按要求填空:
(1)实验室现有l0mL、20mL、50mL量筒,应选用 mL量筒量取浓硫酸,用量筒量取所需体积的浓硫酸后,借助玻璃棒把 沿烧杯壁慢慢加入到盛有 的小烧杯中,边加边搅拌。
(2)除上述提到的仪器外,实验中还需要用到的仪器是下列中的(填编号) 。
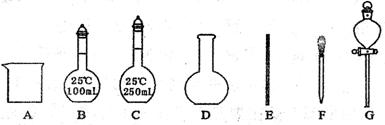
(3) 若实验中出现下列操作,对所配溶液浓度有什么影响?(填“偏高”或“偏低”或“无影响”)
① 容量瓶经蒸馏水洗净后,未干燥即进行配制溶液 。
② 定容时俯视刻度线 。
(4)此实验中玻璃棒的作用有 。
查看答案和解析>>
科目:高中化学 来源: 题型:
水的电离平衡曲线如图所示, 若以A点表示25℃时水的电离达平衡时的离子浓度,B点表示100℃时水的电离达平衡时的离子浓度,则下列说法正确的是
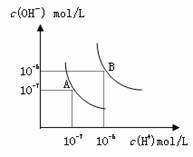
A.纯水中25℃时的c(H+)比100℃时的c(H+)大
B.100℃时某溶液中由水电离产生的c(H+)=1×10-11mol/L,则该溶液的pH可能是11或3
C.将pH=9的Ba(OH)2溶液与pH=4的稀盐酸混合,并保持100℃的恒温,混合溶液的pH=7,则Ba(OH)2溶液和盐酸的体积比为10: 1
D.25℃时,某Na2SO4 溶液中c(SO42-)=5×10-4 mol/L,则溶液中c(Na+):c(OH-)为104:1
查看答案和解析>>
科目:高中化学 来源: 题型:
在一定温度下,测得0.1 mol·L-1CH3COOH溶液的PH为3.0。则CH3COOH在水中的电离度为 ,此温度CH3COOH的电离平衡常数为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
盐是一类常用物质,下列物质可直接形成盐的是
①金属 ②碱性氧化物 ③碱 ④非金属 ⑤酸性氧化物 ⑥酸
A.只有①②③ B.只有④⑤⑥
C.只有①②③⑤⑥ D.全部
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)水的电离平衡曲线如图所示,若A点表示25°C时水的电离达平衡时的离子浓度,B点表示100°C时水的电离达平衡时的离子浓度。①100°C时1mol·L﹣1的NaOH溶液中,由水电离出的c(H+)= mol·L﹣1,KW(25°C) KW(100°C)(填“>”、“<”或“=”)。
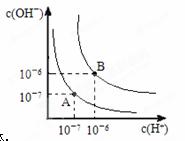 ②25°C时,向水的电离平衡体系中加入少量NH4Cl固体,对水的电离平衡的影响是 (填“促进”“抑制”或“不影响”)。
②25°C时,向水的电离平衡体系中加入少量NH4Cl固体,对水的电离平衡的影响是 (填“促进”“抑制”或“不影响”)。
(2)电离平衡常数是衡量弱电解质电离程度强弱的物理量。已知:
| 化学式 | 电离常数(25℃) |
| HCN | K=4.9×l0-10 |
| CH3COOH | K=1.8×l0-5 |
| H2CO3 | K1=4.3×l0-7、K2=5.6×l0-11 |
③25℃时,有等浓度的NaCN溶液、Na2CO3溶液、CH3COONa溶液,三溶液的pH由大到小的顺序为 。
④25℃时,等浓度的CH3COOH溶液和NaOH溶液等体积混合,混合后所得溶液显碱性,则c(Na+) c(CH3COO-)(填“>”、“<”或 “=”)。
⑤向NaCN溶液中通入少量CO2,所发生反应的化学方程式为 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com