
| A. | 电解饱和食盐水,产生黄绿色气体:2NaCl+2H2O═2NaOH+H2↑+Cl2↑ | |
| B. | 用Na2CO3溶液将水垢中的CaSO4转化为CaCO3:CO32-+Ca2+═CaCO3↓ | |
| C. | 向H2O2溶液中滴加CuSO4溶液,产生气泡:H2O2═H2O+O2↑ | |
| D. | 向苯酚浊液中滴加Na2CO3溶液,溶液变澄清: |
分析 A.电解饱和的食盐水生成氢氧化钠,氢气和氯气;
B.用Na2CO3溶液除水垢中的CaSO4生成碳酸钙和硫酸钠,CaSO4是一种微溶物书写离子方程式不拆;
C.向H202溶液中滴加CuSO4溶液生成水和氧气;
D.向苯酚浊液中滴加Na2CO3溶液生成苯酚钠和碳酸氢钠.
解答 解:A.电解饱和的食盐水生成氢氧化钠,氢气和氯气,故化学方程式为2NaCl+2H2O $\frac{\underline{\;电解\;}}{\;}$2NaOH+H2+Cl2,选项A缺少条件,故A错误;
B.用Na2CO3溶液除水垢中的CaSO4生成碳酸钙和硫酸钠,CaSO4是一种微溶物书写离子方程式不拆,故离子方程式为CO32-+CaSO4=CaCO3+SO42-,故B错误;
C.向H2O2溶液中滴加CuSO4溶液生成水和氧气,故化学方程式为2H2O2=2H2O+O2↑,选项C配平错误,故C错误;
D.向苯酚浊液中滴加Na2CO3溶液生成苯酚钠和碳酸氢钠,故离子方程式为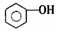 +CO32-→
+CO32-→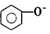 +HCO3-,故D正确,
+HCO3-,故D正确,
故选D.
点评 本题考查化学方程式的书写,为高频考点,把握发生的反应及反应生成物是什么,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 将△H<0的氧化还原反应设计成原电池,将化学能转变为电能 | |
| B. | 轮船水线以下的船壳上,嵌一定数量的锌块,保护船体不被腐蚀 | |
| C. | 在锌与稀硫酸反应的溶液中加入少量CuSO4,能加快生成H2的速率 | |
| D. | 为了保护地下钢管不受腐蚀,将它与一定电压的直流电源的负极相连 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

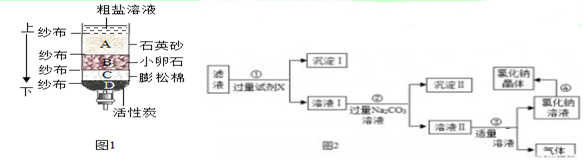
| A. | 用图甲所示装置提纯氢氧化铁胶粒 | |
| B. | 用图乙所示装置进行中和热的测定 | |
| C. | 用图丙所示装置验证温度对平衡移动的影响 | |
| D. | 用图丙所示装置除去乙醇中的乙醚 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
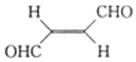
| A. | 分子中只有极性键 | B. | 分子中有σ键和π键 | ||
| C. | 该分子中三种元素的电负性:H>C>0 | D. | 该分子在水中的溶解度小于甲烷的 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 轮船的船体外侧镶嵌一定量的锌块,可以减缓轮船被腐蚀的速度,称之为牺牲阳极的阴极保护法 | |
| B. | 工业生产中,常将氯气通入澄清石灰水中,制取漂白粉 | |
| C. | 氢氧燃料电池、铅蓄电池、硅太阳能电池都利用了原电池原理 | |
| D. | 夏天雷雨过后空气特别清新是因为空气中产生了少量二氧化氮 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 实验室从海带中提取单质碘的方法是:取样→灼烧→溶解→萃取 | |
| B. | 不能通过“玻璃棒蘸取某溶液做焰色反应实验时火焰呈黄色”说明该溶液中含钠元素 | |
| C. | 配制浓硫酸、浓硝酸的混酸时,应将浓硝酸沿玻璃棒缓慢注入浓硫酸中 | |
| D. | 测氯水的pH时,可用干燥洁净的玻璃棒蘸取氯水点在pH试纸上,待其变色后和标准比色卡比较 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 放电过程 | 充电过程 |
| A | Li+向电池的正极迁移 | 化学能转化成电能 |
| B | 可以加入磷酸以提高电解质的导电率 | 阳极的电极反应式为LiFePO4-e-═FePO4+Li+ |
| C | 若正极增加7g,则有NA个电子经电解质由负极流向正极 | 阳极材料的质量不断减少 |
| D | 若有n molLi+迁移,则理论负极失去nmol电子 | 阴极的电极反应式为Li++e-═Li |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | a<7 | |
| B. | 该溶液中水电离的c(OH-)=10-amol/L | |
| C. | CH3COO-水解的百分率为$\frac{10-a}{0.1}$×100% | |
| D. | c(CH3COOH)=(l0a-14-10-a)mol/L |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com