
����Ŀ�������� J ��ij�ֽ�����ʹҩ���� A Ϊԭ�ϵĹ�ҵ�ϳ�·������ͼ�� ʾ��

��֪
����ʽ B: C8H8O2 C:C8H7NO4 D:C6H5NO3 E :C6H7NO F:C9H11NO2 H:C6H 7O3
��1��д��ͬʱ�������������� F ������ͬ���칹��Ľṹ��ʽ_____
���� a�������(a ̼���뺬����ԭ��) �� NMR �ױ��������к��б���
��2������˵������ȷ����_____
A�������� C ���������������
B�������� E �ȿ����� NaOH ��Ӧ�ֿ����� HCl ��Ӧ
C�������� F ���� FeCl3 ������ɫ��Ӧ
D�������� J �ķ���ʽΪ C18H15NO5
��3����� G��H �ĺϳ�·��(������ͼ��ʾ�����Լ���ѡ)_____
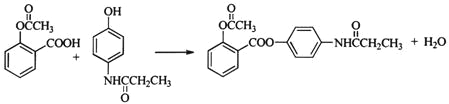
��4��д�� I+F��J �Ļ�ѧ����ʽ_____
���𰸡� 
![]() D
D 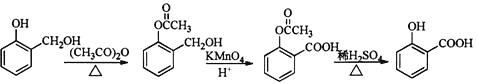
���������ɷ�Ӧ�ٵ��������֪��![]() ��HCHO�����ӳɷ�Ӧ����
��HCHO�����ӳɷ�Ӧ����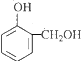 ������B�ķ���ʽ��֪����Ӧ��Ϊ
������B�ķ���ʽ��֪����Ӧ��Ϊ![]() ������������ȡ������BΪ
������������ȡ������BΪ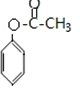 �����ݷ�Ӧ������֪��B����������Ӧ����CΪ
�����ݷ�Ӧ������֪��B����������Ӧ����CΪ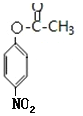 ��Cˮ������DΪ
��Cˮ������DΪ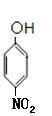 ������������Ϣ��֪��D������ԭ��Ӧ����EΪ
������������Ϣ��֪��D������ԭ��Ӧ����EΪ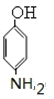 ��E������Ϣ�е�ȡ����Ӧ����FΪ
��E������Ϣ�е�ȡ����Ӧ����FΪ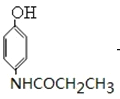 ������J��F�Ľṹ��ʽ��֪IΪ
������J��F�Ľṹ��ʽ��֪IΪ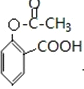 �����Կ��Է��Ƶ�HΪ
�����Կ��Է��Ƶ�HΪ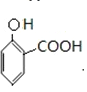 ����
���� ������������ȡ�����ɷ��������ø�������������ǻ�����������������ˮ��ɵ�
������������ȡ�����ɷ��������ø�������������ǻ�����������������ˮ��ɵ� ��
��
��1��FΪ ���������a�������(a̼���뺬����ԭ��)�а������Ȼ������� NMR�ױ��������к��б�������ͬʱ����������F��ͬ���칹���У�
���������a�������(a̼���뺬����ԭ��)�а������Ȼ������� NMR�ױ��������к��б�������ͬʱ����������F��ͬ���칹���У�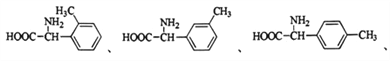
![]() ����2��A��CΪ
����2��A��CΪ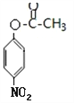 ��������C�к��������������֣���A��ȷ��B��EΪ
��������C�к��������������֣���A��ȷ��B��EΪ![]() ��E�ȿ�����NaOH��Ӧ�ֿ�����HCl��Ӧ����B��ȷ��C��FΪ
��E�ȿ�����NaOH��Ӧ�ֿ�����HCl��Ӧ����B��ȷ��C��FΪ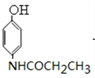 ���з��ǻ�������F����FeCl3������ɫ��Ӧ����C��ȷ��D����J�Ľṹ��ʽ��֪��J�ķ���ʽΪC18H17NO5����D����ѡD����3����
���з��ǻ�������F����FeCl3������ɫ��Ӧ����C��ȷ��D����J�Ľṹ��ʽ��֪��J�ķ���ʽΪC18H17NO5����D����ѡD����3����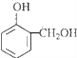 ������������ȡ�����ɷ��������ø�������������ǻ�����������������ˮ��ɵ�
������������ȡ�����ɷ��������ø�������������ǻ�����������������ˮ��ɵ�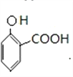 ����Ӧ�ĺϳ�·��Ϊ
����Ӧ�ĺϳ�·��Ϊ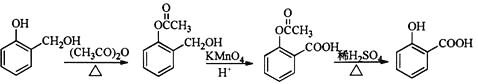
��4��� .
.



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ճ������е����������뻯ѧ��Ӧ�йأ�����������������ԭ��Ӧ�ص��ǣ�������
A.ͭ������ͭ��[Cu2��OH��2CO3]B.���Ʋ˵�����
C.����ʯ�������Խ�ǿ���긯ʴ�ٻ�D.���������������ܵı�Ĥ��Al2O3��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������и���Һ�еμ�ϡH2SO4��MgCl2��Һʱ�����а�ɫ�������ɵ���
A. Ba(OH)2 B. KOH C. Na2CO3 D. BaCl2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������ᣨH3PO2����һ�־�ϸ������Ʒ�����н�ǿ��ԭ�ԣ��ش��������⣺
��1��H3PO2��һԪ��ǿ�ᣬд������뷽��ʽ�� ��
��2��H3PO2�У���Ԫ�صĻ��ϼ�Ϊ ��
��3��NaH2PO2�����λ�����ʽ�Σ�����Һ���ԣ��������ԡ����ԡ����������ԣ���
��4��H3PO2Ҳ����ͨ�����ķ����Ʊ�������ԭ����ͼ��ʾ����Ĥ����Ĥ�ֱ�ֻ���������ӣ�������ͨ������ 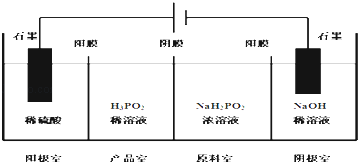
��д�������ĵ缫��Ӧʽ ��
�ڷ�����Ʒ�ҿɵõ�H3PO2��ԭ�� ��
�����ڲ��á����ҵ����������Ʊ�H3PO2 �� �������ҵ����������������ҵ�ϡ������H3PO2ϡ��Һ���棬����ȥ���������Ʒ��֮�����Ĥ���Ӷ��ϲ������������Ʒ�ң���ȱ�������ʣ������ʲ�����ԭ���ǣ� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij������Ϊ���ۺ��������������еĸ���ƷCaSO4 �� �����ڵĺϳɰ�����������������Ʊ���NH4��2SO4�Ĺ������̣��ش��������⣺ 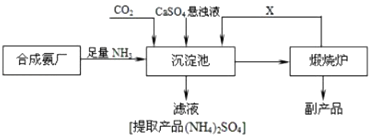
��1����ҵ�ϳɰ����赪�����Կ������������������÷�������
��2����ҵ�ϳɰ���Ӧ�Ļ�ѧ����ʽ��
��3���������з�����Ӧ����Ҫ����ʽ��
��4���������������У��й�NH3�����ü�˵����ȷ���� A���ṩ�Ƹ���Ʒ����ĵ�Ԫ��
B������CO32����Ũ�ȴٽ���Ӧ����
C������Ӧ�Ĵ���
��5������ѭ��ʹ�õ�X�� �� ����ɫ��ѧ����Դ�ۺ����õĽǶ�˵���������̵���Ҫ�ŵ��� ��
��6��д������Ƶ�����һ����; ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������пƬ�ʹ�ͭƬ����ͼ��ʽ����100 mL��ͬŨ�ȵ�ϡ������һ��ʱ�䣬�ش��������⣺
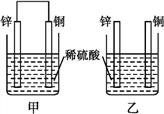
��1������˵������ȷ����____(�����)��
A���ס��Ҿ�Ϊ��ѧ��ת��Ϊ���ܵ�װ�� B������ͭƬ��û�����Ա仯
C������ͭƬ������С������пƬ������С D�����ձ���H+��Ũ�Ⱦ���С
��2�������в���1.12 L(��״��)����ʱ��������ͨ�����ߵĵ�����ĿΪ____��
��3�������в���1.12 L(��״��)����ʱ����п��ͭƬȡ�����ٽ��ձ��е���Һϡ����1 L�������Һ��c(H+)=0.1 mol��L1����ȷ��ԭϡ������c(H2SO4)=___________��
��4��Ag2O2����п���Ե�ص������������ʣ���������ҺΪ KOH��Һ����طŵ�ʱ������Ag2O2ת��ΪAg��������Znת��ΪK2Zn(OH)4��д���õ���ܷ�Ӧ�Ļ�ѧ����ʽ��________________________��
��5���Լ״���CH3OH��Ϊȼ�ϵĵ���У��������ҺΪ���ԣ������ķ�ӦʽΪ��_______________________�������ķ�ӦʽΪ��___________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����һ���¶��£���ӦA2(g)��B2(g)![]() 2AB(g)�ﵽƽ��ı�־��( )
2AB(g)�ﵽƽ��ı�־��( )
A. ��λʱ��������n molA2ͬʱ����n molAB
B. �����ڵ������ʵ�������ʱ��仯
C. ��λʱ��������2n molAB��ͬʱ����n molB2
D. ��λʱ��������n molA2��ͬʱ����n molB2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������Ԫ��X��Y��Z��ɵĻ�����Y2X��ZX2��Y2X����ˮ�γɵ���Һ����ZX2��Ӧ����һ�ֻ�����Y2ZX3����֪����Ԫ��ԭ�ӵ���������Ϊ25����Z��Y��ԭ������֮�ͱ�X��ԭ������2������1��Zԭ����2�����Ӳ㣬�����������Ǻ����������2/3�����Իش�
��1��XԪ�ص����ƣ�_______��YԪ����Ԫ�����ڱ��е�λ��_____________��ZԪ�ص�ԭ�ӽṹʾ��ͼ____________��
��2��Y2X��Ӧˮ����ĵ���ʽ____________�����д��ڵĻ�ѧ����____________��
��3��X���⻯���ͬ������⻯����۷е�����ƫ�ߵ�ԭ��___________________��
��4���õ���ʽ��ʾY2X���γɹ��̣�________________________________________
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����NA��ʾ�����ӵ�������ֵ������˵����ȷ����
A. ����£�22.4L��SO3���Ӻ���ԭ�ӵ���ĿΪNA
B. ���³�ѹ�£�200g��������Ϊ17%��H2O2��Һ�к���ԭ����ĿΪNA
C. 7.1g����������NaOH��Һ��Ӧ�Ʊ�Ư��Һת�Ƶ�����Ϊ0.1NA
D. 1.8g��D2O����NA������
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com