
 Ģ«ŃōÄܵē³Ų°å²ÄĮĻ³żµ„¾§¹čĶā£¬»¹ÓŠĶ”¢ī÷”¢ļŲ”¢ĪųµČ»ÆѧĪļÖŹ£®
Ģ«ŃōÄܵē³Ų°å²ÄĮĻ³żµ„¾§¹čĶā£¬»¹ÓŠĶ”¢ī÷”¢ļŲ”¢ĪųµČ»ÆѧĪļÖŹ£®·ÖĪö £Ø1£©ī÷“¦ÓŚµŚĪåÖÜĘŚ¢óA×壻
£Ø2£©É锢Īų”¢äåČżÖÖŌŖĖŲ¶¼ŹĒµŚ4ÖÜĘŚ·Ē½šŹōŌŖĖŲ£¬Ķ¬Ņ»ÖÜĘŚŌŖĖŲ×Ō×ó¶ųÓŅµēøŗŠŌŌö“ó£»ĘųĢ¬SeO3·Ö×ÓÖŠŠÄŌ×ÓSeµÄ¼Ū²ćµē×Ó¶ŌŹż”¢¹Āµē×Ó¶ŌŹż£¬½ų¶ųČ·¶ØĘä·Ö×Ó¹¹ŠĶ£»
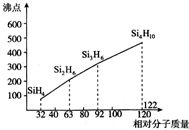
£Ø3£©¹čĶé£ØSinH2n+2£©¶¼ŹĒ·Ö×Ó¾§Ģ壬·Ö×Ó¾§ĢåµÄ·ŠµćøßµĶČ”¾öÓŚ·Ö×Ó¼ä×÷ÓĆĮ¦£¬¶ų·Ö×Ó¼ä×÷ÓĆĮ¦ÓėĻą¶Ō·Ö×ÓÖŹĮæµÄ“óŠ”ÓŠ¹Ų£»
£Ø4£©¼ĘĖćBŌ×Ó¼Ū²ćµē×Ó¶ŌŹż£¬Č·¶ØĘäŌӻƷ½Ź½£»
£Ø5£©½šŹōCuµ„¶ĄÓė°±Ė®»ņµ„¶ĄÓė¹żŃõ»ÆĒā¶¼²»ÄÜ·“Ó¦£¬µ«æÉÓė°±Ė®ŗĶ¹żŃõ»ÆĒāµÄ»ģŗĻČÜŅŗ·“Ó¦£¬ĖµĆ÷Į½ÕßÄÜ»„Ļą“Ł½ų£¬ŹĒĮ½ÖÖĪļÖŹ¹²Ķ¬×÷ÓĆµÄ½į¹ū£¬ĘäÖŠ¹żŃõ»ÆĒāĪŖŃõ»Æ¼Į£¬°±ÓėCu2+ŠĪ³ÉÅäĄė×Ó£¬Į½ÕßĻą»„“Ł½ųŹ¹·“Ó¦½ųŠŠ£»
£Ø6£©ĄūÓĆ¾łĢƷؼĘĖćĮ½ÖÖ½šŹōŌ×ÓøöŹżÖ®±Č£¬½ų¶ų¼ĘĖć¾§°ūÖŹĮ棬øł¾Ż¦Ń=$\frac{m}{V}$¼ĘĖć£®
½ā“š ½ā£ŗ£Ø1£©ī÷“¦ÓŚµŚĪåÖÜĘŚ¢óA×壬ī÷»łĢ¬Ō×ӵĵē×ÓÅŲ¼Ź½£ŗ1s22s22p63s23p63d104s24p64d105s25p1£¬
¹Ź“š°øĪŖ£ŗ1s22s22p63s23p63d104s24p64d105s25p1£»
£Ø2£©É锢Īų”¢äåČżÖÖŌŖĖŲ¶¼ŹĒµŚ4ÖÜĘŚ·Ē½šŹōŌŖĖŲ£¬Ķ¬Ņ»ÖÜĘŚŌŖĖŲ×Ō×ó¶ųÓŅµēøŗŠŌŌö“󣬹ŹµēøŗŠŌ£ŗAs£¼Se£¼Br£¬ĘųĢ¬SeO3·Ö×ÓÖŠŠÄŌ×ÓSeµÄ¼Ū²ćµē×Ó¶ŌŹżĪŖ3+$\frac{6-2”Į3}{2}$=3£¬ĪŽ¹Āµē×Ó¶Ō£¬ĖłŅŌ·Ö×Ó¹¹ŠĶĪŖĘ½ĆęČż½ĒŠĪ£¬
¹Ź“š°øĪŖ£ŗAs£¼Se£¼Br£»Ę½ĆęČż½ĒŠĪ£»
£Ø3£©¹čĶé£ØSinH2n+2£©¶¼ŹĒ·Ö×Ó¾§Ģ壬·Ö×Ó¾§ĢåµÄ·ŠµćøßµĶČ”¾öÓŚ·Ö×Ó¼ä×÷ÓĆĮ¦£¬¹čĶéµÄĻą¶Ō·Ö×ÓÖŹĮæŌ½“󣬷Ö×Ó¼ä×÷ÓĆĮ¦Ō½Ē棬ČŪ·ŠµćÉżøߣ¬
¹Ź“š°øĪŖ£ŗ¹čĶéĪŖ·Ö×Ó¾§Ģ壬ĖęĻą¶Ō·Ö×ÓÖŹĮæŌö“󣬷Ö×Ó¼ä×÷ÓĆĮ¦ŌöĒ棬ČŪ·ŠµćÉżøߣ»
£Ø4£©£©[B£ØOH£©4]-ÖŠBµÄ¼Ū²ćµē×Ó¶Ō=4+$\frac{1}{2}$£Ø3+1-4”Į1£©=4£¬ĖłŅŌ²ÉČ”sp3Ōӻƣ¬¹Ź“š°øĪŖ£ŗsp3£»
£Ø5£©½šŹōCuµ„¶ĄÓė°±Ė®»ņµ„¶ĄÓė¹żŃõ»ÆĒā¶¼²»ÄÜ·“Ó¦£¬µ«æÉÓė°±Ė®ŗĶ¹żŃõ»ÆĒāµÄ»ģŗĻČÜŅŗ·“Ó¦£¬ĖµĆ÷Į½ÕßÄÜ»„Ļą“Ł½ų£¬ŹĒĮ½ÖÖĪļÖŹ¹²Ķ¬×÷ÓĆµÄ½į¹ū£¬ĘäÖŠ¹żŃõ»ÆĒāĪŖŃõ»Æ¼Į£¬°±ÓėCu2+ŠĪ³ÉÅäĄė×Ó£¬Į½ÕßĻą»„“Ł½ųŹ¹·“Ó¦½ųŠŠ£¬Ąė×Ó·½³ĢŹ½ĪŖ£ŗCu+H2O2+4NH3•H2O=Cu£ØNH3£©42++2OH-+4H2O£¬
¹Ź“š°øĪŖ£ŗCu+H2O2+4NH3•H2O=Cu£ØNH3£©42++2OH-+4H2O£»
£Ø6£©ŌŚ¾§°ūÖŠ£¬AuŌ×ÓĪ»ÓŚ¶„µć£¬CuŌ×ÓĪ»ÓŚĆęŠÄ£¬øĆ¾§°ūÖŠAuŌ×ÓøöŹż=8”Į$\frac{1}{8}$=1£¬CuŌ×ÓøöŹż=6”Į$\frac{1}{2}$=3£¬ĖłŅŌøĆŗĻ½šÖŠAuŌ×ÓÓėCuŌ×ÓøöŹżÖ®±Č=1£ŗ3£¬
¾§°ūĢå»żV=£Øa”Į10-10cm£©3£¬Ćæøö¾§°ūÖŠĶŌ×ÓøöŹżŹĒ3”¢AuŌ×ÓøöŹżŹĒ1£¬¾§°ūÖŹĮæĪŖ$\frac{197+64”Į3}{N{\;}_{A}}$g£¬Ōņ¾§°ūĆܶȦŃ=$\frac{197+64”Į3}{N{\;}_{A}}$g”Ā£Øa”Į10-10cm£©3=$\frac{£Ø197+64”Į3£©”Į10{\;}^{-30}}{N{\;}_{A}”Įa{\;}^{3}}$g£®cm-3£¬
¹Ź“š°øĪŖ£ŗ1£ŗ3£»$\frac{£Ø197+64”Į3£©”Į10{\;}^{-30}}{N{\;}_{A}”Įa{\;}^{3}}$£®
µćĘĄ ±¾ĢāŹĒ¶ŌĪļÖŹ½į¹¹µÄ漲飬Éę¼°ŗĖĶāµē×ÓÅŲ¼”¢µēøŗŠŌ”¢·Ö×Óæռ乹ŠĶ”¢ŌӻƷ½Ź½”¢ÅäŗĻĪļ”¢¾§°ūĆÜ¶ČµÄ¼ĘĖćµČ£¬ÄѶČÖŠµČ£¬ŠčŅŖѧɜ¾ß±øŌśŹµµÄ»ł“”ÓėĮé»īŌĖÓĆÖŖŹ¶µÄÄÜĮ¦£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
 ½ĒöčĻ©ŹĒŅ»ÖÖÖ¬ÖŹ²»Ōķ»ÆĪļ£¬×ī³õ“Ó½ĒöčĻ©µÄøŹÓĶÖŠ·¢Ļֵģ¬¾ßÓŠÉśĪļŃõ»Æ»¹Ō×÷ÓĆÓėĢįøßÄÜĮæµÄŠ§¹ū£¬ÓŠĄūÓŚŌöĒæ»śĢåµÄÄĶĮ¦ÓėøÄÉĘŠÄŌą¹¦ÄÜ£¬æÉÓĆÓŚ°©Ö¢µÄ·ĄÖĪ£¬ŹĒŅ»ÖÖĪŽ¶¾ŠŌµÄ¾ßÓŠ·Ą²”ÖĪ²”×÷ÓƵÄŗ£ŃóÉśĪļ»īŠŌĪļÖŹ£¬¹ŲÓŚ½ĒöčĻ©ÓŠĻĀĮŠŠšŹö£ŗ
½ĒöčĻ©ŹĒŅ»ÖÖÖ¬ÖŹ²»Ōķ»ÆĪļ£¬×ī³õ“Ó½ĒöčĻ©µÄøŹÓĶÖŠ·¢Ļֵģ¬¾ßÓŠÉśĪļŃõ»Æ»¹Ō×÷ÓĆÓėĢįøßÄÜĮæµÄŠ§¹ū£¬ÓŠĄūÓŚŌöĒæ»śĢåµÄÄĶĮ¦ÓėøÄÉĘŠÄŌą¹¦ÄÜ£¬æÉÓĆÓŚ°©Ö¢µÄ·ĄÖĪ£¬ŹĒŅ»ÖÖĪŽ¶¾ŠŌµÄ¾ßÓŠ·Ą²”ÖĪ²”×÷ÓƵÄŗ£ŃóÉśĪļ»īŠŌĪļÖŹ£¬¹ŲÓŚ½ĒöčĻ©ÓŠĻĀĮŠŠšŹö£ŗ| A£® | ¢Ł¢Ś¢Ū | B£® | ¢Ł¢Ū¢Ü | C£® | ¢Ś¢Ū¢Ü | D£® | ¢Ł¢Ś¢Ū¢Ü |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ČĪŗĪĘųĢåµ„ÖŹŌŚ±ź×¼×“æöĻĀĢå»żŌ¼ĪŖ22.4L£¬Ōņŗ¬ÓŠ2NAøöŌ×Ó | |
| B£® | ³£ĪĀ³£Ń¹ĻĀ£¬22gŃõĘųŗĶ26g³ōŃõĖłŗ¬ŃõŌ×Ó×ÜŹżĪŖ3NA | |
| C£® | ³£ĪĀ³£Ń¹ĻĀ£¬11.2L¼×Ķé£ØCH4£©ÖŠŗ¬ÓŠµÄĒāŌ×ÓŹżĪŖ2NA | |
| D£® | ±ź×¼×“æöĻĀ£¬0.3mol¶žŃõ»ÆĢ¼ÖŠŗ¬ÓŠŃõŌ×ÓŹż0.3NA |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| »Æѧ¼ü | C-H | C=C | C-C | H-H |
| ¼üÄÜ£ØkJ•mol1£© | 414.4 | 615.3 | 347.4 | 435.3 |
| A£® | +125.6 kJ•mol”„1 | B£® | -125.6 kJ•mol”„1 | C£® | +46.1 kJ•mol”„1 | D£® | -46.1 kJ•mol”„1 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
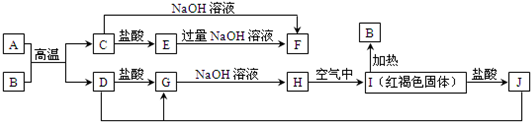
| A£® | æÉÓė»īĘĆ½šŹōÖ±½Ó·¢Éś»Æѧ·“Ó¦ | B£® | æÉČÜÓŚĖ®£¬Ņ×ČÜÓŚNaOHČÜŅŗ | ||
| C£® | ŹĒŅ»ÖÖĪŽ¶¾ĘųĢå | D£® | æÉÓĆHCNČÜŅŗÓėMnO2»ģŗĻ¼ÓČČÖĘČ” |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Cl2ĶØČėĖ®ÖŠ | B£® | Cl2ĶØČėFeCl2ČÜŅŗÖŠ | ||
| C£® | NH3ĶØČėĖ®ÖŠ | D£® | NO2ĶØČėĖ®ÖŠ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 1.0 L 1.0 mo1•L-1µÄNaAlO2 Ė®ČÜŅŗÖŠŗ¬ÓŠµÄŃõŌ×ÓŹżĪŖ2 NA | |
| B£® | ŗ¬ÓŠNAøöŌ×ÓµÄĒāĘųŌŚ±ź×¼×“æöĻĀµÄĢå»żŌ¼ĪŖ22.4 L | |
| C£® | ±ź×¼×“æöĻĀ£¬2.24 LCl2Óė×ćĮæĖ®·“Ó¦×ŖŅʵĵē×ÓŹżĪŖ0.2NA | |
| D£® | V L a mol•L-1µÄĀČ»ÆĢśČÜŅŗÖŠ£¬ČōFe3+µÄŹżÄæĪŖNA£¬ŌņCl-µÄŹżÄæ“óÓŚ3NA |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com