
中国的食盐产量居世界首位。下列实验室中的操作类似“海水晒盐”原理的是( )
A.蒸馏 B.蒸发
C.过滤 D.搅拌
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
下列溶液中c(Cl-)与50 mL 1 mol·L-1的AlCl3溶液中c(Cl-)相等的是( )
A.150 mL 1 mol·L-1 NaCl溶液
B.75 mL 2 mol·L-1 CaCl2溶液
C.150 mL 3 mol·L-1 KCl溶液
D.75 mL 3 mol·L-1 FeCl3溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
某课外小组设计了下图所示的实验装置(图中固定装置已略去),进行SO2性质的研究.
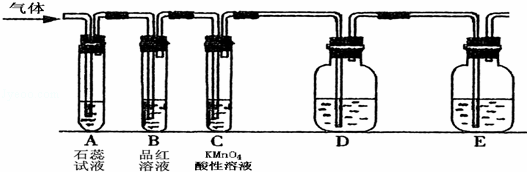
(1)从物质分类的角度,SO2属于 (填“酸性”或“碱性”)氧化物.
①图中D装置可用来验证SO2具有该性质,其中所加入的试剂是 .
②当向该装置通入SO2时,A中紫色石蕊溶液变红,用化学用语解释其原因是 .
(2)从元素化合价的角度分析,SO2具有 性.
①当向该装置通入SO2 一段时间后,可观察C中溶液褪色,说明SO2具有 性,反应的化学方程式为 .
②如验证SO2还具有另一方面的性质,可选择的药品是 .
A.过氧化氢 B. 浓硫酸 C.氯水 D.硫化钠溶液.
查看答案和解析>>
科目:高中化学 来源: 题型:
某化学兴趣小组对电化学问题进行了实验探究。
Ⅰ.利用如图所示装置探究金属的防护措施,实验现象是锌电极不断溶解,铁电极表面有气泡产生。
(1)写出负极的电极反应式:________________________。
(2)某学生认为,铁电极可能参与反应,并对产物做出假设:
假设1:铁参与反应,被氧化生成Fe2+;
假设2:铁参与反应,被氧化生成Fe3+;
假设3:____________________________________________________。
(3)为了探究假设1、2,他采取如下操作:
①取0.01 mol/L FeCl3溶液2 mL于试管中,加入过量铁粉;
②取操作①试管的上层清液加入2滴K3溶液,生成蓝色沉淀;
③取少量正极附近溶液加入2滴K3溶液,未见蓝色沉淀生成;
④取少量正极附近溶液加入2滴KSCN溶液,未见溶液变红。
据②、③、④现象得出的结论是____________________________。
(4)该实验原理可应用于防护钢铁腐蚀,请再举一例防护钢铁腐蚀的措施:________。
Ⅱ.利用如图所示装置做电解50 mL 0.5 mol/L的CuCl2溶液实验。
实验记录:
A.阳极上有黄绿色气体产生,该气体使湿润的淀粉碘化钾试纸先变蓝后褪色(提示:Cl2氧化性大于IO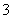 );
);
B.电解一段时间以后,阴极表面除有铜吸附外,还出现了少量气泡和浅蓝色固体。
(1)分析实验记录A中试纸颜色变化,用离子方程式解释:
①_________________________________________________________;
②_________________________________________________________。
(2)分析实验记录B中浅蓝色固体可能是________(写化学式),试分析生成该物质的原因:__________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法中错误的是( )
A.在豆浆中加入少量的石膏,能够使豆浆产生聚沉
B.温度越高,酶的催化效率越高
C.蛋白质水解生成氨基酸
D.浓硝酸能够使皮肤变成黄色,是由于浓硝酸与蛋白质发生了显色反应
查看答案和解析>>
科目:高中化学 来源: 题型:
已知某溶液中Cl-、Br-、I-的物质的量之比为2∶3∶4,现欲使溶液中Cl-、Br-、I-的物质的量之比为4∶3∶2,那么要通入Cl2的物质的量是原溶液中I-的物质的量的( )
A.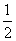 B.
B.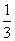
C.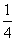 D.
D.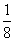
查看答案和解析>>
科目:高中化学 来源: 题型:
下列对乙烯和聚乙烯的描述不正确的是(双选) ( )
A.乙烯是纯净物,聚乙烯是混合物
B.乙烯的性质与聚乙烯相同
C.常温下,乙烯是气体,聚乙烯是固体
D.等物质的量的乙烯和聚乙烯完全燃烧后生成CO2和H2O的物质的量相等
查看答案和解析>>
科目:高中化学 来源: 题型:
完全沉淀等物质的量浓度的NaCl.MgCl2.AlCl3溶液中的Cl-,消耗等物质的量浓度的AgNO3溶液的体积比为1:1:1,则上述溶液的体积比为
A.1:1:1 B.3:2:1 C.6:3:2 D.9:3:1
查看答案和解析>>
科目:高中化学 来源: 题型:
食盐中含有一定量的镁、铁等杂质,加碘盐中碘的损失主要是由于杂质、水分、空气中的氧气以及光照、受热而引起的.已知:氧化性:IO3﹣>Fe3+>I2;还原性:S2O32﹣>I﹣3I2+6OH﹣═IO3﹣+5I﹣+3H2O;
KI+I2 KI3
KI3
(1)某学习小组对加碘盐进行如下实验:取一定量某加碘盐(可能含有KIO3、KI、Mg2+、Fe3+),用适量蒸馏水溶解,并加稀盐酸酸化,将所得溶液分为3份.第一份试液中滴加KSCN溶液后显红色;第二份试液中加足量KI固体,溶液显淡黄色,用CCl4萃取,下层溶液显紫红色;第三份试液中加入适量KIO3固体后,滴加淀粉试剂,溶液不变色.
①加KSCN溶液显红色,该红色物质是 (用化学式表示);CCl4中显紫红色的物质是 (用电子式表示).
②第二份试液中加入足量KI固体后,反应的离子方程式为 、 .
(2)KI作为加碘剂的食盐在保存过程中,由于空气中氧气的作用,容易引起碘的损失.写出潮湿环境下KI与氧气反应的化学方程式: .将I2溶于KI溶液,在低温条件下,可制得KI3•H2O.该物质作为食盐加碘剂是否合适? (填“是”或“否”),并说明理由 .
(3)为了提高加碘盐(添加KI)的稳定性,可加稳定剂减少碘的损失.下列物质中有可能作为稳定剂的是 .
A.Na2S2O3 B.AlCl3 C.Na2CO3 D.NaNO2
(4)对含Fe2+较多的食盐(假设不含Fe3+),可选用KI作为加碘剂.请设计实验方案,检验该加碘盐中的Fe2+. .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com